Диабетическая ретинопатия

Описание
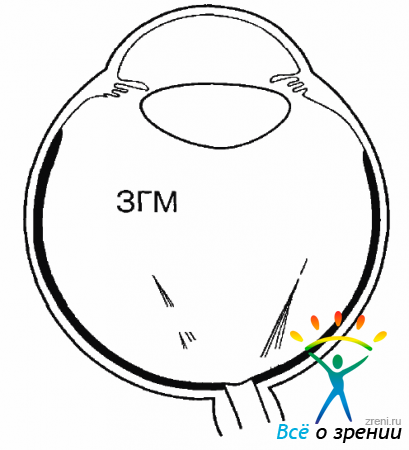
Сахарный диабет в сроки от 2 до 10 лет ведет к развитию изменений в сетчатке. У пациентов, страдающих сахарным диабетом более 10 лет, ретинопатия наблюдается в 100% случаев и является основной причиной слабовидения и слепоты при этом заболевании. Установлено, что основным фактором, вызывающим возникновение ретинопатии, служит нарушение окислительно-восстановительных процессов в сетчатой оболочке, ведущее к гипоксии ткани. Начинаясь в сетчатке в виде локальных отеков, сужения капилляров, расширения вен, появления микроаневризм, точечных кровоизлияний, очагов неоваскуляризации, процесс, прогрессируя, распространяется на прилежащее СТ. Источником кровоизлияний в СТ, как правило, приводящих к его задней отслойке, являются новообразованные сосуды сетчатки. Полная отслойка СТ, когда ЗГМ полностью отходит от заднего полюса глаза и подтягивается вперед, располагаясь во фронтальной плоскости, случается сравнительно редко. Чаще ЗГМ отслаивается частично, сохраняя связь с ДЗН, тогда конфигурация СТ напоминает конус с острой вершиной (рис. 9.1).Рис. 9.1. Частичная ЗОСТ. Острый конус
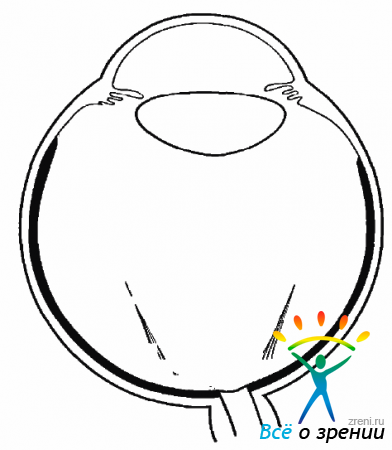
Если ЗГМ сращена не только с ДЗН, но и с макулярной зоной и сосудами в области сосудистых аркад, конфигурация СТ приобретает вид широкого конуса (рис. 9.2).
Рис. 9.2. Частичная ЗОСТ. Широкий конус
Проницаемость гематоофтальмического барьера при сахарном диабете повышена. Из кровеносного русла проникают протеины и клеточные элементы, которые осаждаются на структурах СТ. Наличие среди мигрирующих в СТ факторов роста приводит к запуску механизма клеточной пролиферации. Мембраны и волокна СТ являются тем каркасом, на котором и происходит оседание и последующее разрастание клеточных пролифератов. Это еще более усиливает процесс деструкции СТ. Особенно активно рост пролиферативной ткани идет по ЗГМ. В тех случаях, когда отслойка СТ не произошла и ЗГМ по всей поверхности прилежит к сетчатке, пролиферация может развиваться между сетчаткой и ЗГМ, продвигаясь по ее поверхности. В этих случаях могут иметь место как преретинальные кровоизлияния, гак и прорыв крови через ЗГМ в СТ с развитием в нем пролиферации.
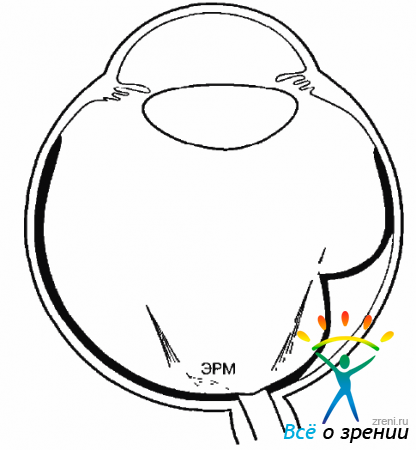
Развиваясь, пролиферативный процесс может распространяться как в СТ, так и по поверхности сетчатки в виде эпиретинальных мембран. Постепенно под влиянием вазопролиферативных факторов в пролифераты идет врастание новообразованных сосудов. Чаще всего рост сосудов происходит со стороны ДЗН и сосудистых аркад. Разрастание фиброзной ткани, конденсация и сокращение волокон СТ ведут к усилению тракций на сетчатку и могут быть причиной массивных гемофтальмов, а иногда и ОС. Тракционная ОС при пролиферативной диабетической ретинопатии (ПДР) возникает обычно на этапе фиброваскулярных и фиброзных изменений. Окруженные патологически измененными тканями, такие ОС могут длительное время оставаться стационарными. Характерная особенность таких тракционных ОС — их вогнутая конфигурация (рис. 9.3).
[banner_centerrs] {banner_centerrs} [/banner_centerrs]
Рис. 9.3. Частичная ЗОСТ. Тракционная ОС
В пролиферативный процесс уже на ранних стадиях вовлекается глия сетчатки: глиальные клетки могут мигрировать в СТ. Пролиферативный рост глиальных клеток приводит к образованию прочных витреоретинальных сращений. Развивающиеся витреоретинальные тракции могут вызвать разрыв сетчатки и появление регматогенной ОС с типичной выпуклой конфигурацией.
Хирургические методы лечения диабетической ретинопатии
Эффективными методами лечения диабетической ретинопатии являются лазеркоагуляция сетчатки и витрэктомия.
На ранних стадиях заболевания используется аргоновая лазерная коагуляция. Если патологический процесс ограничен отдельными участками, проводят фокальную лазеркоагуляцию и пределах пораженных участков: зоны неоваскуляризации, отека и кровоизлияний. Эффективность коагуляции нужно контролировать с помощью флюоресцентной ангиографии (ФАГ).
При обширных изменениях, выраженной пролиферации применяют панретинальную лазеркоагуляцию по всему глазному дну. Особенно тщательно должна подвергаться коагуляции центральная часть сетчатки. Коагуляты наносят во всех зонах кровоизлияний, отека, экссудации, начавшейся пролиферации. Необходимо провести и паравазальную коагуляцию, включая зону сосудистых аркад, где необходимо использовать сниженную мощность лазера и максимально уменьшенный диаметр коагулята. Особенно четко нужно действовать при проведении парамакулярной коагуляции, с тем чтобы не повредить фовеолярную зону и папилломакулярный пучок. Лечение следует проводить в несколько этапов и под контролем ФАГ.
Аргоновая лазерная коагуляция (АЛК) сетчатки является очень эффективным методом борьбы с пеоваскуляризацией. В зоне коагуляции новообразованные сосуды запустевают, прекращается рост новых сосудов. Закрытие новообразованных сосудов, являющихся основной причиной рецидивирующих геморрагий, приводит к прекращению кровоизлияний как в сетчатку, так и в СТ. Паравазальная АЛК снижает венозный застой и способствует исчезновению отеков сетчатки. Особенно эффективно лазерное лечение при макулярном отеке. Своевременная парамакулярная и паравазальная АЛК снимает отек и существенно повышает остроту зрения.
Закрытие новообразованных сосудов, ликвидация венозного застоя, образование в области коагуляции сосудистых шунтов между сетчаткой и хориоидеей способствуют ускорению кровотока, улучшению оксигенации и исчезновению ацидоза, прекращается рост фиброзной ткани. Своевременно проведенная панретинальная АЛК приводит к стабилизации процесса и является эффективной профилактикой ОС.
Значительные кровоизлияния, наличие плотных пролифератов, помутнение хрусталика затрудняют, а иногда делают невозможной проведение лазеркоагуляции. При выраженных тракциях на сетчатку со стороны СТ, при активной неоваскуляризации лазеркоагуляция противопоказана, так как может вызвать тяжелые осложнения: кровоизлияния, ОС, усиление пролиферации.
Витрэктомия показана при массивных, длительно нерассасывающихся кровоизлияниях, при отслойке сетчатки, захватывающей макулярную зону. Кровоизлияние на лучшем или единственном глазу, так же как и двусторонний гемофтальм, является показанием к срочной витрэктомии. Тракционная ОС, если она не захватывает макулу, не является показанием для срочной хирургии. Динамическое наблюдение, лазерное и консервативное лечение позволяют во многих случаях стабилизировать процесс и сохранять высокие функции в течение многих лет.
Срочная витрэктомия не показана в случае свежих кровоизлияний в СТ, если есть надежда на их рассасывание и проведение АЛК. Относительным противопоказанием для операции является выраженный рубеоз радужки. При тяжелой неоваскуляризации радужки от операции следует воздержаться. Прогинопоказанием к оперативному вмешательству является общее тяжелое состояние пациента. Для решения вопроса о тактике лечения, возможности проведения и выборе анестезии необходимы консультации эндокринолога, терапевта и анестезиолога.
Техника операции. Операция проводится через три склеротомических подхода в плоской части цилиарного тела с подшиванием инфузионной канюли. Если у больного имеется катаракта, ее удаление нужно начать после подшивания канюли, но без включения подачи инфузионной жидкости через малый роговичный или корнеосклеральный разрез методом лазерной или ультразвуковой факоэмульсификации. Для того чтобы не расширять разрез, целесообразно имплантировать мягкую ИОЛ, вводя ее в капсульный мешок в сложенном состоянии. Необходимо обратить внимание на сохранение задней капсулы хрустали ка и ПГМ. Интактные ПГМ и задняя капсула являются барьером для выхода в переднюю ка меру вазопролиферативных факторов. При ее сохранности значительно снижается количество таких тяжелых осложнений, как неоваскулярная глаукома и ретролентальная неоваскуляризация.
После того как имплантирована ИОЛ и произведена герметизация роговичного разреза, необходимо открыть подачу инфузионной жидкости и сделать еще два прокола через склеру и плоскую часть цилиарного тела для введения активного и пассивного инструментов. Удаление передних слоев СТ не имеет особенностей, тактика удаления задних отделов зависит от конфигурации СТ. При полной отслойке ЗГМ она смещена вперед, расположена во фронтальной плоскости и подвижна в передне-заднем направлении. В ЗГМ имеется овальное отверстие, соответствующее границе бывшего сращения с ДЗН (кольцо Вейса). Через это отверстие полости СТ перед ЗГМ и позади нее сообщаются. Удаление ЗГМ в этих случаях проходит достаточно легко, не создавая заметных тракции на сетчатку.
В тех случаях, когда ЗГМ связана с ДЗН и СТ имеет коническую конфигурацию, передняя и задняя полости не сообщаются. ЗГМ напряжена и оказывает тракциоппое действие на сетчатку. Позади ЗГМ может скапливаться значительное количество взвешенной крови. Для того чтобы избежать выхода крови в передние отделы глаза, предупредить развитие эритроцитарной глаукомы, в ЗГМ витреотомом делается небольшое отверстие, через которое витреотом проводится за мембрану, и путем включения аспирации кровь из ретровитреальной полости вымывается.
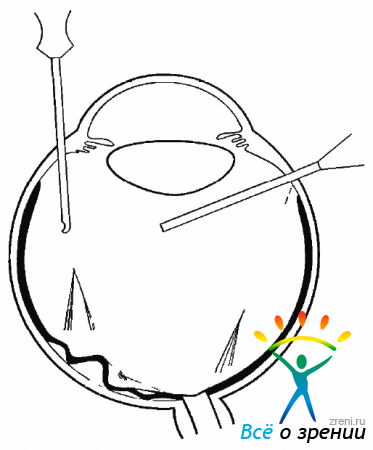
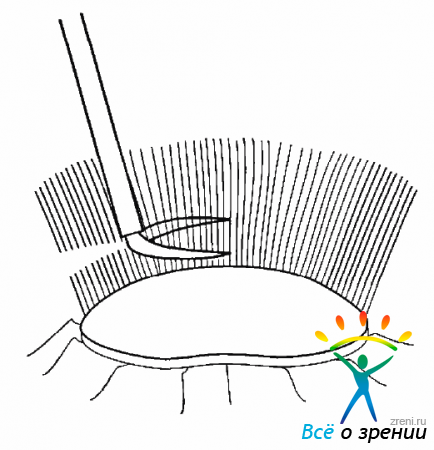
Удаление ЗГМ должно проводиться без усиления тракции при высокой частоте резания и низкой аспирации (рис. 9.4).
Рис. 9.4. Удаление ЗГМ витреотамом
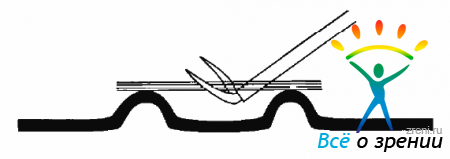
Расширяя во все стороны уже образованное отверстие, необходимо удалить мембрану максимально полно, оставив лишь узкую полоску на периферии и около ДЗН. При выраженной фиброваскулярной пролиферации удаление фиброзноизмененной мембраны у ДЗН следует проводить с предварительным ее рассечением ножницами (рис. 9.5).
Рис. 9.5. Рассечение фиброзной ЗГМ
Если при этом возникает кровотечение из новообразованных сосудов, то его необходимо остановить с помощью диатермокоагуляции.
Если ЗГМ сохраняет адгезию не только с ДЗН, по и с макулой и сосудистыми аркадами, конфигурация СТ напоминает широкий усеченный конус. Отслойка СТ в этих случаях ограниченная и довольно плоская. Образование отверстия в ЗГМ часто связано с определенными трудностями, особенно если есть ОС, гак как при этом можно поранить сетчатку.
При пилинге мембрана должна легко отходить от сетчатки. Если сетчатка начинает сдвигаться и образовывать складку, пилинг нужно немедленно прекратить. Дальнейшее отслоение следует проводить с помощью витреальных ножниц (рис. 9.11).
Рис. 9.11. Рассечение ЭРМ с помощью витреальных ножниц
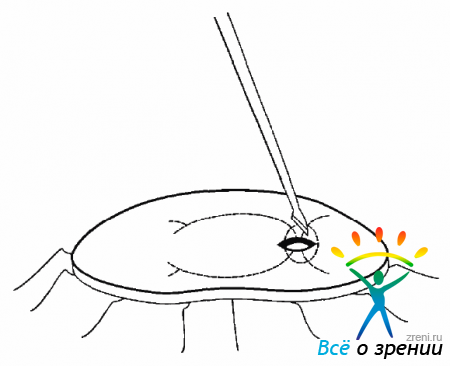
В тех случаях, когда эпиретинальные мембраны тесно спаяны с сетчаткой, их выделение может привести к разрыву сетчатки. Для того чтобы снять тангенциальные тракции, плоскостные мембраны необходимо рассечь на отдельные небольшие сегменты. В процессе фиброза мембрана, сокращаясь, собирает сетчатку в складки. Первый разрез мембраны микровитреальным ножом необходимо произвести между складками (рис. 9.12).
Рис. 9.12. Начальный разрез ЭРМ витреальным ножом
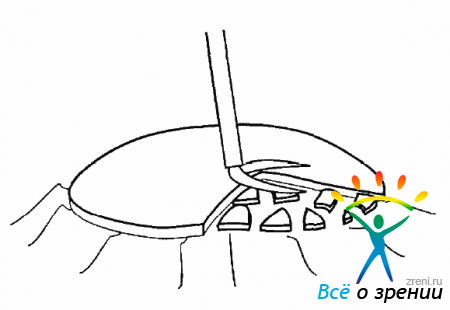
Вся дальнейшая сегментация мембраны выполняется с помощью прямоугольных витреальных ножниц. Проведя браншу ножниц через разрез под мембрану, производят первое рассечение. Расслаивая мембрану и сетчатку там, где это возможно, рассекают мембрану на отдельные сегменты (рис. 9.13).
Рис. 9.13. Сегментация ЭРМ
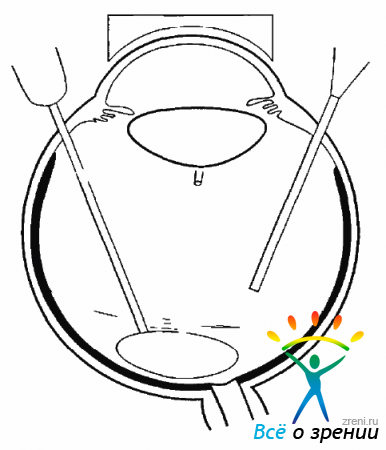
Расслоение и рассечение мембраны должно проводиться очень осторожно. Слишком активные действия могут принести к повреждению сетчатки. В процессе сегментации могут возникнуть кровотечении из сосудов сетчатки при ее повреждении или из новообразованных сосудов мембраны. Риск повреждения сетчатки существенно снижается, если проводить отслоение и сегментацию мембраны с использованием ПФОС (рис. 9.14).
Рис. 9.14. Введение ПФОС под ЭРМ
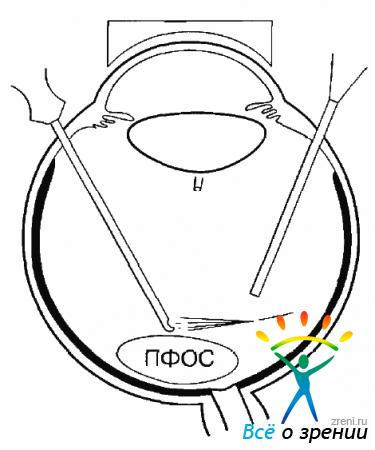
Введенное в полость СТ в количестве 1,5-2,0 мл ПФОС своим весом расправляет сетчатку и прижимает ее к хориоидее. Сетчатка становится менее подвижной, деламинация и сегментация мембраны проходят легче и безопаснее. Кроме того, сдавливая стенки сосудов, ПФОС уменьшает опасность кровотечения (рис. 9.15).
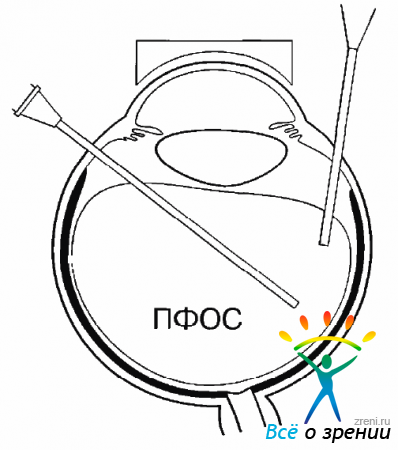
Рис. 9.15. Удаление ЭРМ витреотомом после ее отслоения от сетчатки
После удаления мембран и полной мобилизации сетчатки полость СТ заполняется ПФОС. Происходит расправление освобожденной от тракций сетчатки, и она прижимается к сосудистой оболочке.
Наличие хорошего контакта между сетчаткой и хориоидеей позволяет провести панретинальную ЭЛК (рис. 9.16).
Рис. 9.16. Проведение ЭЛК при заполнении витреальной полости ПФОС
При этом следует коагулировать все зоны неоваскуляризации. Три ряда плотно расположенных коагулятов должны окружать разрывы сетчатки. Необходимо провести коагуляцию между оставшимися фрагментами эпиретинальной мембраны, коагуляты должны окружать все зоны атрофии и дегенерации сетчатки. В зоне ретинального отека и геморрагий следует выполнять паравазальную коагуляцию. Недопустима прямая коагуляция крупных сосудов, ДЗН, макулярной зоны и папилломакулярного пучка.
В случаях, когда не было ОС, после завершения эндокоагуляции полностью удаляется ПФОС и вводится воздушно-газовая смесь. В тяжелых случаях необходимо, удаляя ПФОС, одновременно заполнить витреальную полость силиконом. Силикон может быть удален через 2-3 месяца, если сетчатка полностью прилежит, если в зоне разрыва или разрывов сформировались надежные хориоретинальные сращения и нет угрозы образования новых разрывов сетчатки.
Витреоретинальная хирургия в сочетании с лазерной коагуляцией сетчатки является высокоэффективным методом лечения диабетической ретинопатии. Витрэктомия, восстанавливая прозрачность, приводит к снижению тракции па сетчатку, особую важность при этом приобретает максимально полное удаление ЗГМ. Витрэктомия и ЭЛК создают условия для остановки пролиферативного процесса и не только улучшают функции глаза, по и позволяют сохранить их на долгие годы.
----
Статья из книги: Витреоретинальная хирургия | Захаров В. Д.


Комментариев 0