Физиология зрительной рецепции (Часть 2)

Описание
Взаимодействие родопсина с периферическими белками наружного сегмента фоторецептора
Структура родопсина.Зрительный пигмент родопсин является интегральным белком фоторецепторного диска с молекулярной массой 40 кДа. После бактериородопсина зрительный родопсин оказался вторым мембранным белком, полная аминокислотная последовательность которого была расшифрована. Эта работа была проведена коллективом авторов в рамках проекта "Родопсин", возглавляемого академиком Ю.А. Овчинниковым. Следует заметить, что, хотя бактериородопсин и был первым исследованным интегральным мембранным белком, в силу особенности строения бактериородопсиновой бляшки его структура оказалась достаточно специфичной. По существу, бактериородопсиновая бляшка - это мембранное образование с жесткой фиксацией каждой единицы белка, что совершенно нетипично для строения большинства биологических мембран. В этом смысле родопсин оказался первым типичным интегральным мембранным белком, который был подвергнут систематическим исследованиям, и представления о его структуре во многом были перенесены в исследования других мембранных белков.
Родопсин из глаз крупного рогатого скота представляет собой голипептид из 347 аминокислот. Первые представления о трехмерной структуре родопсина были получены практически одновременно методом электронной микроскопии в сочетании с малоугловым рентгеновским рассеянием и ограниченным протеолизом, проведенным при определении первичной структуры.
Оказалось, что молекула родопсина состоит из 7 трансмемб-ранных ?-спиралей (ТМ1-ТМ7) и соединяющих их 3 внутридисковых и 4 цитоплазматических петель. При этом N-концевой участок полипептидной цепи находится во внутридисковом пространстве, а С-концевой пет ид обращен в цитоплазму
Более точно трехмерная структура молекулы родопсина была определена значительно позже двумя способами. Первоначально трехмерная модель родопсина была получена методом электронной кристаллографии на двумерных кристаллах. Трехмерная модель была реконструирована из последовательности срезов на различных уровнях молекулы. В последующих работах удалось синтезировать классические трехмерные кристаллы родопсина, что позволило изучить его трехмерную структуру методом рентгеновской кристаллографии. При этом новейшие исследования полностью подтвердили результаты предшествующей работы. Интересно отметить, что результаты, полученные спустя 20 лет, не входили в противоречие и с первыми данными по ограниченному протеолизу, а лишь значительно их детализировали. Ниже мы опишем наиболее современное представление о структуре белка.
Оказалось, что ?-спирали ТМ4, ТМ6, ТМ7 расположены пер-пендикулярно к дисковой мембране, аюгда как спирали ТМ1, ТМ2, ТМЗ, ТМ5 находятся под некоторым углом к мембраье.
Кроме того ?-спиральные участки могут значительно выступать над поверхностью мембраны, сохраняя при этом свою периодическую структуру.
В молекуле родопсина можно выделить цитоплазматическую, внутридисковую и внутрчмембранную части Внутридиско вая часть молекулы родопсина состоит из N-концевого участка и трех петель, экспонированных во внутридисковое пространство. Эта часть родопсина содержит три аминокислотных остатка цистеина (Cys-110r Cys-185 и Cys-187). В нативной форме рецептора Cys-110 и Cys-187 образуют дисульфидный мостик, необходимый для поддержания правильной структуры родопсина и связывания ретиналя. Так. при замене этого дисульфидного мостика на С-185-С-187 (мутации С-110А, С 110F, C-110Y) опсин терял способность к связыванию ретиналя. При образовании мостика С-110—С-185 вместо нативного (мутация С -187А) родопсин хотя и мог связывать ретиналь, но при этом формировался пигмент с аномальным световым повепением.
N-концевой участок родопсина гликозилирован по аминокислотным остаткам Asn-2 и Asn-15. Вероятнее всего, как и в случае большинства трансмембранных белков, гликозилирование является необходимым для формирования правильной трехмерной структуры рецептора. Таким образом, внутридисковая часть молекулы играет важную роль в обеспечении структуры родопсина, хотя и не участвует в прямых взаимодействиях с периферическими белке ми и, по-видимому, мало затрагивается при фото- андуцированных изменениях родопсина, о чем речь пойдет позже.
Внутримембранная часть родопсина состоит из ретиналя и семи трансмембранных ?-спиралей, представляющих собой остов опсина. Еще в первых работал Дж. Уолда было установлено, что 11-цис-ретиналь коьалентно связан с ? -аминогруппой лизина через Шиффово основание. Сейчас показано, что это Lys-296, локализованный на спирали ТМ7.
Остатки внутри трансмембранных спиралей выполняют две основные функции:
- создают связывающий карман для 11-цис-ретиналя и регулируют его спектральные свойства;
- участвуют во внутримолекулярных взаимодействиях, которые контролируют третичную структуру белка и динамику его фотоиндуцированных изменений.
Как известно, максимум поглощения свободного ретиналя составляет 380 нм, а максимум поглощения родопсине 500 нм. Чем объясняется подобный батохромный сдвиг максимума поглощения? Б основном состоянии родопсина Шиффово основание находится в протонированной форме. Протонирование Шиффова основания увеличивает делокализацию электрона вдоль полиеновой цепи ретиналя и вызывает смещение максимума поглощения родопсина с 380 до 440 нм (Х,макс). Наблюдаемый в родопсине сдвиг Хмакс до 500 нм можно объяснить за счет слабого дальнодействующего взаимодействия между Шиффовым основанием и его противоионом Glu-113 на ТМЗ. Максимум поглощения хромофора может также варьировать в зависимости от локализации ретиналя в неполярном кармане, образуемом боковыми цепями некоторых аминокислот. Эксперименты по исследованию точных сайтов взаимодеиствия опсина с ретиналем показали, что Gly-121 на ТМЗ и Phe-261 на ТМ6 взаимодействуют с С9-метильной группой ретиналя. Таким образом, аминокислотные остатки Glu-113, Glu-121, Phe-261, Lys-296 непосредственно связываются с ретиналем, причем для регуляции спектральных свойств хромофора особенно важны Glu-113, Lys-296, a Glu-121, Phe-261 играют важную роль в эффективной активации родопсина в ответ на фотоизомеризацию ретиналя.
Как поддерживается стабильная трехмерная структура родопсина? Известно, что в отличие от глобулярных водорастворимых белков, структура которых поддерживается за счет водородных связей через молекулы воды, третичная структура интегральных мембранных белков обеспечена в основном гидрофобными взаимодействиями. Тем не менее, как оказалось, вода также играет важную роль в поддержании структуры белка.
Методами инфракрасной спектроскопии было показано наличие как минимум трех молекул воды во внутримембранном пространстве родопсина. Эксперименты с использованием мутантных форм родопсина (замена Е -113Q) показали, что одна из молекул воды находится внутри хромофор-связывающего кармана и образует водородные связи с протонированным Шиффовым основанием и его противоионом Glu-113. Вторая молекула воды соединяет ТМ2 и ТМЗ с помощью мистика, образованного водородными связями с карбоксильным карбонилом Asp-83 и с пептидным карбонилом Gly-120.
Следует отметить, что внутримембранная часть молекулы может играть и некоторую роль во взаимодействии родопсина с трансдуцином. Интересно, что ароматические аминокислоты на позиции 261 сохраняются у большинства связывающих трансдуцин рецепторов (82%). Это может свидетельствовать о важной роли ТМЗ-лиганд-ТМб взаимодейсвия в активации рецептора.
Цитоплазматическая часть родопсина состоит из 4 петель и карбоксильного концевого участка. Три петли соединяют между собой трансмембранные ? -спирали, а четвертая петля расположена между седьмой ? -спиралью и двумя пальмитированными цистеинами (Cys-322, Cys-323). На рис. 1.5 показано, что гидрофобные участки пальмитиновых кислот погружены в дисковую мембрану и таким образом прикрепляют к ней С-концевой участок родопсина. Основная роль этого участка состоит во взаимодействии с трансдуцином, на чем подробнее мы остановимся ниже.
Фотохимические превращения родопсина. При освещении родопсин обесцвечивается: из пурпурного он становится желтоватым. Собственно говоря, именно это наблюдение на изолированной сетчатке лягушки и привело Франца Болля (1876) к открытию Sehestoff, или светочувствительного вещества сетчатки, названного затем Visual purple, или зрительным пурпуром. Значительно позже зрительный пурпур был назван родопсином, что сначала обозначало зрительный пигмент палочек, содержащий в качестве хромофора альдегид витамина А1 - ретиналь,. Сравнительно недавно к семейству родопсинов были отнесены все зрительные пигменты, содержащие в качестве хромофора ретиналь,, в отличие от семейства порфиропсинов, у которых хромофор – ретиналь2. Правда, зрительный пигмент красных колбочек, содержащих в качестве хромофора ретиналь,, продолжают называть иодопсином. За счет добавочной двойной связи в (?-иононовом кольце ретиналя2 порфиропсины, как правило, поглощают в более длинноволновой области спектра, нежели родопсины. Следует подчеркнуть, что природа фотопревращений порфиропсинов и родопсинов одинакова.
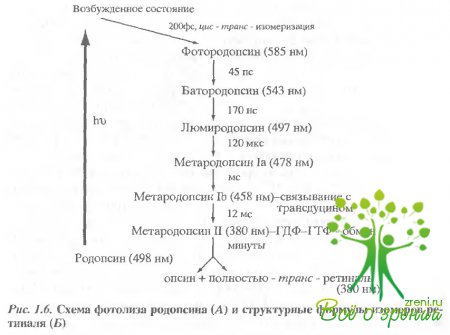
Итак, фотопревращение, или фотообесцвечивание, родопсина включает собственно фотохимическую реакцию и последующие темновые, зависящие от температуры превращения. Поскольку хромофорную группу родопсина можно рассматривать как естественную хромофорную метку внутри молекулы, то с ее помощью удается спектрально исследовать промежуточные продукты (интермедиаты) фото- и термопревращений родопсина. Франц Болль наблюдал в изолированной сетчатке лягушки, по существу, два продукта: исходный нативный (темновой) родопсин и один из последних, достаточно стабильный продукт фотообесцвечивания, так называемый индикатор желтый, или в современной терминологии метародопсин II. Затем для детального исследования фото- и термопревращений родопсина с успехом были применены методы низкотемпературной спектрофотометрии. Вслед за этим получили развитие методы быстрой лазерной спектроскопии, которые позволили при комнатной температуре подробно исследовать кинетику фотохимических и термальных реакций родопсина и, что особенно важно, обнаружить новые самые коооткоживущие промежуточные продукты в фемто- и наносекундных диапазонах. На рис. 1.6, А представлена схема фотопревращения родопсина, включая самые ранние продукты.
[banner_centerrs]
{banner_centerrs}
[/banner_centerrs]
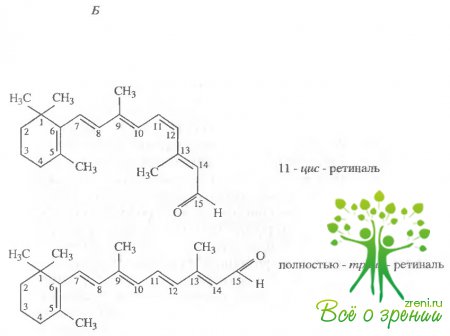
В отличие от фотоцикла бактериородопсина и фотопревращений родопсина беспозвоночных, зрительные пигменты позвоночных претерпевают при действии света необратимые превращения, или фотолиз. Речь идет о том, что на последних стадиях происходит гидролиз связи Шиффова основания ретиналя с опсином, в результате чего высвободившийся ретиналь теперь уже в полностью трансформе "уходит" из фоторецепторной клетки (рис. 1.6, Б).
Итак, при поглощении кванта света родопсин переходит в электронно-возбужденное состояние. Эта самая первая фотофизическая стадия фотопревращения занимает всего несколько фемтосекунд. Единственная фотохимическая реакция в зрении - фотоизомеризация хромофора (11-цис-ретиналя) конкурирует с тремя другими процессами, принимающими участие в релаксации синглетного возбужденного состояния родопсина в основное состояние, а именно: внутренней безызлучательной конверсией и флуоресценцией. Поэтому неудивительно, что Фотохимическая реакция цис-транс-изомеризации должна протекать достаточно быстро, чтобы эффективно конкурировать с тремя другими. Методом сверхбыстрой лазерной фемтосекундной спектроскопии было показано, что фотоизомеризация хромофора происходит в пределах 200 фемтосекунд. Считается, что изомеризация начинается, примерно, через 60 фемтосекунд после поглощения кванта. Это одна из самых быстрых химических реакций, известных в настоящее время. Кванто¬вый выход фотоизомеризации 11-цис-ретиналя равен 0.67.
Таким образом, первым фотохимическим продуктом в процессе фотолиза родопсина является так называемый фотородопсин. Поскольку образование фотородопсина происходит исключительно быстро (менее чем за 200 фс), можно предполагать, что если и могут происходить смещения аминокислотных остатков в ближайшем окружении хромофора, то лишь крайне незначительные. Поскольку цис-транс-изомеризация приводит к удлинению вытянутой полиеновой цепи ретиналя, то в ограниченном объеме хромофорного центра он должен находиться в сильно скрученной конформации. Следствием этого должно быть возрастание потенциальной энергии. Действительно, калориметрические исследования показали, что около 60% энергии поглощенного кванта (около 30 Ккал) оказываются запасенными в молекуле родопсина.
Таким образом, функциональная роль сверхбыстрой фото изомеризации хромофора состоит в том, чтобы перевести поглощенную энергию кванта света в свободную химическую энергию, запасенную в молекуле родопсина в виде его сильно скрученной конформации. Энергия эта, в свою очередь, вызовет гораздо более медленные конформационные перестройки в белковой части молекулы (олеине). Конечным же результатом этих перестроек станет образование долгоживущего продукта - мета-родопсина II, который приобретает способность взаимодействивать с транедуцином. Взаимодействие метародопсина II или, как его часто называют, активированного родопсина с транедуцином представляет собой ключевую реакцию в механизме транедукции светового сигнала.
Конформационные изменения ропсине после изомеризации 11-цме-ретиналя происходят ступенчато, что отражается на спектрах поглощения промежуточных продуктов фотолиза родопсина.
Изомеризация хромофора начинается с движения той половины полиеновой цепи 11 -цис-ретиналя, которая содержит протежированное Шиффово основание и ковалентно связана с опсином. Таким образом, первые внутримолекулярные смещения аминокислотных остатков опсина происходят вблизи Шиффова основания на стадии перехода от фото- к батородопсину (см. рис. 1.6, А). Конкурентное движение молекулы воды, связанной с протонированным Шиффовым основанием и Е -113 (Glu-113) может вызывать значительные конформационные изменения в ближайшем окружении протонированного Шиффова основания. Затем, чтобы высвободить часть напряжения все еще скрученного хромофора, вторая половина его полиеновой цепи, содержащая В-иононовое кольцо, также смещается и меняет свое взаимодействие с ближайшими аминокислотными остатками, теперь уже на стадии перехода бато- в люмиродопсин.
Отражением фотоиндуцированных конформационных изменений в опсине на стадии образования батородопсина могут служить наблюдавшиеся нами при температуре жидкого азота фотообратимые изменения сверхтонкой структуры мессбауэровской метки, связанной с родопсином в Лоторецепторной мембране.
На стадии перехода от люми- к метародопсину I дальнейшие изменения во взаимодействии с ближайшими аминокислотными остатками наблюдаются вблизи 9-й метильной группы полиеновой цепи. На этой же стадии еще сохраняется возможность фотообратимых превращений родопсина. Действительно, при температуре минус 22 °С, при которой мстародопсин I стабилен, можно наблюдать многократный спектральный фитопереход из родопсина в метародопсин I, и обратно. Интересно, что если спектральные характеристики исходного темнового и фоторегенерированного родопсина практически совпадают, то их изомерный состав, судя по результатам, полученным методом хроматографии под высоким давлением, оказывается различным: в исходном родопсине хромофором является, естественно., 11-цис-ретиналь, однако в (Ьоторегенерированном синим светом продукте это в основном - полностью-трякоретиналь. Эти и целый ряд других данных свидетельствуют о том, что, с одной стороны, произошедшие на стадии метародопсина I конформационные изменения опсина весьма значительны, но с другой стороны, судя по сохранению его способности к фоторегенерации, еще не являются необратимыми. Во всяком случае, на этой стадии все изменения конфигурации хромофора уже полностью завершены и хромофорный центр опсина находится в термодинамически стабильном состоянии. Следует отметить, что перестройки и в хромофоре, и в опсине на стадии образования метародопсина I существенны для взаимодействия с транедуцином. Так, удаление ?-иононового кольца или 9-й метальной группы ретиналя приводит к падению способности зрительного пигмента активировать трансдуцин. Интересно, что еще до стадии образования метародопсина II спектрально обнаруживается продукт, названный метародонсин Ib, который способен связывать трансдуцин, но не способен обеспечить реакцию обмена ГДФ на ГТФ.
И, наконец, метародопсин 1 переходит в следующий продукт - метародопсин II. Этот переход сопровождается увеличением и энтальпии, и энтропии, что отражает потерю специфических взаимодействий в молекуле зрительного пигмента и соответственно повышение конформационной подвижности всего белка. Наиболее выраженным отличием метародопсина I от метародопсина II является депротонирование Шиффова основания. Подробнее о конформационных изменениях на стадии образования метародопсина II см. ниже.
Метародопсин II затем медленно (в минутном диапазоне) переходит в метародопсин III, и далее происходит реакция гидролиза связи Шиффова основания. Высвободившийся полностью-транс-ретиналь активно тоанспоптируется через фоторецепторную мембрану и претерпевает дальнейшие химические изменения. Однако для физиологического акта фототранедукции образование метародопсина II является последней и ключевой стадией в многоступенчатом внутримолекулярном процессе фотопревращения молекулы зрительного пигмента.
Фотоиндуцироьанные процессы в родопсине. Основные функциональные процессы, происходящие в родопсине, сводятся к активации транедуцина и последующему возвращению родопсина в неактивное состояние. В обоих процессах ключевую роль играют цитоплазматические аминокислотные остатки. При этом для активации родопсина необходимыми являются два процесса: конформационные перестройки во внутридисковой части, вызывающие изменения в цитоплазматических петлях. Процесс деактивации родопсина связан только с цитоплазматическими петлями, где локализованы сайты фосфорилирования и связывания с арестином.
Как показали многочисленные исследования с использованием различных методов ультрафиолетовой спектроскопии, флуоресцентных меток, ЭПР-спектроскопии, фотолиз родопсина сопровождается определенными структурными перестройками в цито-плазматической части рецептора. Эти перестройки начинаются во внутридисковой часта молекулы. При поглощении фотона 11 -цис-ретиналь переходит в полностью-трокс форму, происходит депротонирование Шиффова основания и разрыв связи ретиналя и Glu-113. Это вызывает перемещение ТМЗ, а разрушение структурного микродомена ТМ2-ретиналь-ТМЗ приводит к изменению взаимного расположения ? -спиралей. Фотоактивация родопсина приводит к конформационным изменениям и в ТМ6. В результате происходит относительное перемещение спиралей ГМЗ и ТМ6 и увеличение расстояния между цитоплазматическими концами этих спиралей. Кроме того, наблюдается смещение спирали ТМ2, хотя и меньшее, чем у ТМ6. Таким образом, перемещение ? -спиралей является необходимым условием для образования активной формы родопсина. В результате этих перемещений пространственное расположение цитоплазматических петель и С-кон-цевого пептида меняется, что делает возможным связывание цитоплазматических цепей родопсина с трансдуцином и другими цитоплазматическими белками Активация трансдуцина фотолизированной формой родопсина носит сложный последовательный характер. На сегодняшний день установлено, что во взаимодействии с трансдуцином участвуют вторая, третья и четвертая цитоплаз-матические петли родопсина. О том же говорят и наши данные с использованием спиновых меток, подробно рассмотренные ниже.
Специфичность связывания родопсина с трансдуцином определяется третьей цитоплазматической петлей. Так, при замене ее N- и С-концевых участков на соответствующие участки другого трансдуцип-связывающего рецептора мутантный белок активировал не трансдуцин, а G-белок использованного в эксперименте рецептора.
Вторая цитоплазматическая петля родопсина является необходимой для перестройки трансдуцина в активную форму. Показано, что в активации трансдуцина принимают участие аминокислоты N-концевого участка этой петли - Glu-134, Val-138 и Cys- 140. Эксперименты показали, что N-концевой участок четвертой петли непосредственно связывается с ? -субъединицей трансдуцина, а замена этого участка замедляет его активацию.
В результате, можно сказать, что специфическое связывание с трансдуцином N- и С-концевых участков третьей петли и неспецифическое взаимодействие с ним N-концевых участков второй и четвертой петель играют определяющую роль в процессе активации трансдуцина родопсином. Определяющую роль в связывании трансдуцина играет отодвигание С-концевой петли. Это следует, в частности, из проведенных нами экспериментов со спиновыми метками.
Деактивация родопсина - фосфорилирование и взаимодействие с арестином. Рассмотрим молекулярные процессы, происходящие в молекуле родопсина при его деактивации. Первый этап - это реакции фосфорилирования, осуществляемые родопсинкиназой. С обнаружением родопсинкиназы был открыт новый класс киназ, фосфорилирующих связывающие G-белок рецепторы. Специфика этого класса киназ состоит в том, что они реагируют только с активированной формой рецептора.
Методом отщепления концевых пептидов эндопептидазой Asp-N Ьыло показано, что все сайты фосфорилирования находятся на С-концевом участке родопсина. Всего было обнаружено 7 потенциальных сайтов фосфорилирования, но ключевыми являются аминокислотные остатки: Ser-334, Ser-338, Ser-343, а также Thr-336. Изучение механизма активации родопсинкиназы показало сложный характер фосфорилирования родопсина. Оказалось, что отщепленный С-концевой пептид родопсина не фосфорилируется. Для активации необходимо связывание родопсинкиназы с цитоплазматической частью родопсина, отличной от сайтов фосфорилирования, и только в связанном состоянии у киназы появчяется способность к фосфорилированию субстрата, причем этим субстратом могут быть и экзогенные пептиды. При детальном рассмотрении механизмов взаимодействия родопсинкиназы с родопсином была выявлена ключевая роль цитоплазматической петли ТМ5-ТМО как основного сайта связывания киназы. Таким образом, связывание родопсинкиназы с 3-й петлей родопсина приводит к ее активации и последующему фосфорилированию сериновых и треониновых остатков С-концевого участка родопсина.
Важно отметить, что трансдуцин не может активироваться в момент, когда родопсин связан с киназой, и таким образом родопсинкиназа частично ингибирует активацию трансдуцина конкурентным способом еще до того как будет запущен основной механизм ингибирования, т.е. начнет работать арестин.
Как было сказано ранее, быстрое выключение каталитической активности родопсина в основном обеспечивается его взаимодействием с арестином. Kuhn и сотр. впервые обнаружили белок, который может связываться только с фосфорилированным родопсином, и назвали его арестин. После связывания арестина с фосфорилированным родопсином последний полностью терял способность связывать трансдуцин. Таким образом, выключение активности фосфорилированного родопсина есть результат конкуренции между арестином и трансдуцином за сайты связывания на родопсине. Детальное изучение механизма взаимодействия родопсина и арестина выявило его сложный последовательный характер. В основном состоянии молекула арестина имеет низкое сродство к активной форме рецептора. Но после первоначального взаимодействия с фосфорилированием С-концевым пептидом родопсина молекула арестина активируется и приобретает сильное сродство к цитоплазматическим петлям родопсина. Процессы активации и связывания арестина с цитоплазматическими петлями рецептора могут протекать независимо. В экспериментах, где от родопсина протеолитически отщепляли С-концевой пептид, а соответствующий фосфорилированный пептид добавляли в раствор, было обнаружено нормальное связывание арестина с рецептором, при этом специфичность активированной молекулы арестина к фотолизированной форме родопсина сохранялась.
Исследования механизмов ингибирования активации трансдуцина позволили выделить специфические сайты связывания рецептора с арестином. Удобным методом оказалось изучение конкуренции между нативной формой родопсина и пептидами, соответствующими его отдельным цитоплазматическим петлям. Оказалось, что пептиды третьей петли сильно ингибировали связывание арестина и родопсина. Некоторый ингибируютций эффект вызывали и пептиды первой петли. Аналогичные исследования проводились методом напразленного мутагенеза. Оказалось, что одиночные замещения аминокислот первой и второй петли (Asn-73 в петле I; Pro-142 и Met-143 в петле II) на аланин нарушали эффективное связывание аресгина и родопсина. Гак им образом, фесфорилированный С-концевой участок молекулы родопсина в ходе фотолиза отодвигается и, освобождаясь, вызывает активацию арестина. После этого арестин, взаимодействуя с первой, второй и третьей цитоплазматическими петлями рецептора, осуществляет конкурентное ингибирование активации трансдуцина.
Другим подходом к изучению взаимодействия родопсина с арестином и трансдуцином оказалась комбинация ограниченного протеолиза и модификация цистеинов в цитоплазматической части белка. Рассмотрим эти данные подробнее.
Конечно, основной функцией сайтов фосфорилирования С-конца родопсина является образование отрицательно заряженного домена. Но было обнаружено, что существуют сайты, которые не фосфорилируются in vivo, но при этом необходимы для активации арестина. Так, при замене Thr-340 на глутамат арестин связывался с родопсином. Кроме того, замена всех семи потенциальных сайтов фосфорилирования на отрицательно заряженные глутаматы приводила также к связыванию арестина. Это говорит о том, что С-концевой пептид выполняет дополнительную функцию в структурных перестройках арестина.
Трансдуцин - структура, взаимодействие с родопсином и фосфодиэстеразой.
В основном, неактивном, состоянии трансдуцин представляет собой гетеротример, в состав которого входят ?, ? и ?-субъединицы. Функционально и структурно в молекуле трансдуцина можно выделить два комплекса, играющих различную роль как в его активации, так и во взаимодействии с эффекторами. Первый комплекс – это ? -субъединица, связанная с гуаниновым нуклеотидом. Второй комплекс представляет собой ?-субъединицу и связанную с ней ?-субъединицу, причем, для обеспечения функционирования комплекса С-концевой пептид ?- субъединицы должен быть фарнезилиоован.
Передача сигнала от родопсина к фосфодиэстеразе обеспечивается Т?субъединицей, поэтому мы начнем рассмотрение с ее структуры.
Т?-субъелинипа состоит из 350 аминокислот и имеет молекулярную массу 40 кДа. Методами рентгеновской кристаллографии была получена детальная картина структуры Т?с разрешением 2,2 A. Т?-ГТФ состоит из 2 доме¬нов, разделенных глубокой щелью. Эта щель представляет собой структурный карман, связывающий гуанозин. Первый домен представлен аминокислотной последовательностью 1-53 и 179-350, и состоит из шести ?-листов (?1-?), окруженных пятью ?-спиралями (?l-?5). Установлено, что именно этот домен ответствен за ГТФазную активность ?-субъединицы. Аминокислотная последовательность первого домена высоко консервативна среди всех G белков и аналогична семейству Ras-белков.
Второй - высокоспиральный домен представлен аминокислотной последовательностью 59-172. и уникален для гетеротримерных G-белков. Он соединяется с ГТФазным доменом двумя полипептидами (54-58 linker 1) и (173-179 linker 2).
Домены I и II образуют такую структуру, что ГТФ и ассоциированный ион Mg2+полностью спрятаны внутри молекулы, и поэтому для обмена нуклеотидов необходимы конформационные изменения в щели между доменами 1 и II. Домен II представляет собой основную ?-спираль (?А). состоящую из 28 аминокислот, которая поддерживает 5 меньших ?-спиралей (?B-?F) через гидрофобные взаимодействия. Такая устойчивая внутренняя структура домена II может обеспечивать ему роль откидывающейся крышки при конформационных изменениях в linker 1 и linker 2, необходимых для обмена нуклеотидов.
Связывание гуаниновых нуклеотидов. Положение молекулы ГТФ в структуре субъединицы трансдуцина точно установлено Фосфатные группы ГТФ, связанные с ионом Mg2+ образуют водородные связи с амидами основной цепи (скелетными) Glu-39 Gly-41, Lys-42, Ser-43. Thr-177 и Gly-199 и с боковыми цепями Lys-42 и Arg-174. 2- и 3 гидроксильные группы сахарного кольца связаны водородными связями с карбонильными группами Lea- 171 и Arg-172. Азот гуанинового кольца связан через воду с боковыми цепями Ser-147 и Arg-172. Стабилизация гуанинового кольца обеспечивается Ван-дер-Ваальсовым взаимодействием между Lys-266 и метильной группой Thr-323. Сам же Lys-266 фиксируется солевым мостиком с Asp-146, а Thr-323 блокируются с помощью водородной связи с боковой цепью Cys-321.
Такое сложное взаимодействие приводит к тому, что гуаниновые нуклеотиды не только играют основную функциональную роль в работе трансдуцина, но и сами по себе участвуют в формировании и поддержании его структуры.
Функции трансдуцина. Как было сказано выше, для активации трансдуцина необходим обмен нуклеотидов ГДФ на ГТФ, который происходит в присутствии активной формы родопсина. Хотя точная картина взаимодействия родопсина и трансдуцина все еще неясна, некоторые аспекты этого взаимодействия изучены детально.
Установлено, что 2 пептида, входящих в состав гетеротримеоа трансдуцина, могут стабилизировать метародопсин II аналогично нативному трансдуцину. Первый пептид - это 10 С-концевых аминокислот а-субъединицы.
Второй пептид является С-концевым фосфорилированным пептидом г-субъединицы (60-71) с присоединенным к концу липидом - фарнезилом. Следует отметить, что наличие фарнезила является необходимым для обеспечения функций. Методом конкурентного ингибирования показано, что оба этих пептида могут ингибировать процесс активации трансдуцина, но способность к ингибированию для первого пептида была парадоксально низкой по сравнению со способностью к стабилизации метародопсина II.
При рассмотрении структуры этих пептидов видно, что они настолько различны, что им должны соответствовать различные сайты связывания на родопсине. Кроме того, следует отметить, что в нативном генеротримере трансдуцина участки этих пептидов разнесены на 40А, тогда как максимальный линейный размер цитоплазматической части родопсина составляет 35А. Таким образом, одновременное взаимодействие этих пептидных участков с родопсином невозможно без существенных конформационных перестроек. Предложено две модели последовательного взаимодействия трансдуцина с активным родопсином. В первом случае два родопсин-связывающих сайта взаимодействуют по очереди так, что одновременно с родопсином связан лишь один из сайтов. Предполагается, что взаимодействие первого сайта с родопсином индуцирует связывание с ним и второго сайта; таким образом, оба сайта одновременно участвуют в каталитической реакции Для такой модели конформационное сближение родопсин-связывающих сайтов является необходимым.
Наряду с участком 340-350 Т? во взаимодействии с активным родопсином участвует второй сайт на Т?, включающий петлю 305-314. Этот участок также вносит вклад в специфичность распознавания активной формы родопсина. Было показано, что пептид 311-328 обладал способностью к конкурентному ингибированию активации трансдуцина.
Замещение аминокислот показало, что ключевыми являются аминокислоты Arg-309, Asp-311, Val-312, Lys-313.
Для активации трансдуцина необходимы структурные перестройки, вызываемые каталитическим обменом нуклеотидов ГДФ на ГТФ. Сравнительный анализ трехмерных структур Т?-ГДФ и Т?-ГТФ выявил три основных области таких структур - это SwI(Ser-173-Thr-183), SwII (Phe-195-Thr-215), SwIII (Arg-227-Arg-238). Области SwI и SwII имеют структурные аналоги в Ras-белках, тогда как последовательностьSwIIIуникальна для тримерных G-белков. Рентгеновская кристаллография показала, что изменения в SwI иSwIIявляются следствием взаимодействия между ?-фосфатом ГТФ с Тhr-177 в SwI и образованием водородной связи между ?-фосфатом ГТФ и Gly-199 в SwII. В отличие от Swl и SwII, SwIII не имеет прямых взаимодействий с ГТф. Структурные изменения в этой области при обмене нуклеотидов обусловлены серией полярных взаимодействий между SwII и SwIII, которые индуцированы конформационными изменениями в SwII.
Каким образом обеспечивается активация фосфодиэстеразы? Активный Т?-ГТФ комплекс, взаимодействуя с ингибиторными ?-субъединицами ФДЭ, освобождает каталитические сайты фосфодиэстеразы на ?- и ?-субъединицах.
Исследования, проведенные методом направленного мутагенеза, выявили основные сайты взаимодействия Т? с фосфодиэстеразой. Оказалось, что Ile-208 из SwII прямо взаимодействует с эффектором, тогда как остатки Arg-201 Arg-204 и Tip-207 из SWII необходимы для конформационио-зависимого взаимодействия Т?-ФДЭ.
В активации ФДЭ участвует и SwIII-область. Авторы показали, что роль SwIII заключается не в связывании с ФДЭ?, а в активации фосфодиэстеразы При выявлении ключевых аминокислот в SwIII оказалось, что одиночное замещение Glu-232 (мутация E-232L) вызывало тот же эффект, что и замена всей области Swiil на Ala.
Рассмотрение детальной структуры SwIII позволило объяснить критическую роль Glu-232 в активации ФДЭ. Расположение Glu-232 в петле, соединяющей 64-лист и аЗ-спираль, определяет его как основное положение для передачи конформационных изменений между SwII и SwIII Рентгеновская кристаллография показала, что при связывании Т?с ГТФ-7-S Glu-232 вовлекается в прямое взаимодействие с Arg-201 и Arg-204 из SwII и опосредованное водой взаимодействие с Gly-199 из SwII. Таким образом, конформационная связь между SwII и SwIII есть главное связующее звено между связыванием Т? с ФДЭТ и взаимодействием между ФДЭТ и остатками петли а4-б6 (305-314) Т?.
Кроме описанной выше прямой активации ФДЭ через взаимодействие Т? с ФДЭ?, между Та и ФДЭ существуют и регуляторные связи. Показано, что II высокоспиральный домен Т? связывается непосредственно с каталитическими ?- и ?-субъединицами фосфодиэстеразы, причем для него существует свой сайт связывания на ФДЭ??, такой, что это взаимодействие проходит независимо от взаимодействия ФДЭ?? с ФДЭ?. Таким образом, II высокоспиральный домен играет роль модуляторной области, усиливающей эффективность активирующей способности транедуцина.
Фосфодиэстераш - структура, механизм взаимодействия с трангдуцином. Фосфодиэстераза зрительной клетки является Центральным эффект орным белком в каскаде фототранедукции.
В основном, неактивном, состоянии фосфодиэстераза представляет собой гетеротетрамер, в котооом каталитические сайты на ??-димере блокированы ?-субъединицами Активационное взаимодействие Т?-ГТФ с ФДЭ?? вызывает перемещение ?-субъединицы, в результате которого каталитические сайты на ??-субъединицах становятся доступными для цГМФ, что запускает механизм его гидролиза. Кроме того, в результате активации ФДЭ происходит высвобождение молекул цГМФ из некаталитических сайтов связывания, и таким образом запускается механизм ГТФазной регуляции. Последующее взаимодействие Т?-ГТФ с ФДЭ??играет модуляторную роль. Кинетический анализ показал, что скорость гидролиза у фоторецепторной ФДЭ более чем в 1000 раз превосходит активность других фосфодиэстераз.
Рассмотрим подробнее, как структура ФДЭ обеспечивает передачу сигнала трансдукции от трансдуцина к вторичному мессенджеру - цГМФ.
Структурный состав фоторецепторной ФДЭ уникален среди всего семейства фосфодиэстераз. ФДЭ состоит из четырех субъединиц; каталитическая часть представлена гетеродимером ??, a ее активационные сайты регулируются двумя ингибиторными ?-субъединицами. Первичная структура всех трех субъединиц была определена в работах группы Ю.А. Овчинникова.
Рассматривая каталитическую часть ФДЭ, следует отметить, что ?- и ?-субъединицы имеют близкое структурное сходство и выполняют одинаковые функции (у обеих субъединиц общие функциональные сайты), а их аминокислотная последовательность совпадает на 72%. ?-субъединица представлена последовательностью 859 аминокислот с молекулярной массой 99 кДа. б-субъединица со стоит из 853 аминокислотных остатков и имеет молекулярную массу 98 кДа. Одно из различий состоит в том, что С-концевой пептид ?-субъединицы в отличие от ?-субъединицы фарнезилирован. Эти концевые модификации обеспечивают фиксацию фосфодиэстеразы на дисковой мембране.
Каждая из каталитических субъединиц содержит ряд функциональных доменов. Это каталитический сайт связывания цГМФ, некаталитические сайты связывания цГМФ, представляющие собой две повторяющиеся области, кроме того, имеются сайты связывания ?-субъециниц и Т?. В связи с высоким сходством каталитических субъединиц структурные свойства можно рассматривать на примере любой из них.
?-субъединица так же, как и ?-субъединица, содержит в N-концевой половине гомологичные повторения аминокислотных остатков. Эти области (последовательности 89-251 и 295-464 для ?-субъединицы) являются некаталитическими сайтами связывания цГМФ. Физиологическая роль этих сайтов заключается в регулировании времени жизни активного состояния ФДЭ. В комбинации с RGS9 ФДЭТ может активировать ГТФазу Т?-ГТФ, когда некаталитические сайты связывания цГМФ свободны. Связывание цГМФ с некаталитическими сайтами понижает ГТФафазную активность, вызывая обратное связывание ФДЭТ с ФДЭ??.
Каталитический сайт связывания цГМФ, состоящий из -250 остатков (последовательность 555-790 для ?-субъединицы). расположен в С-концевой пиловине каталитических субъединиц. Элементы этого сайта сохраняются у всех ФДЭ циклических нуклеотидов. Это богатый глицином регион, который может формировать петлю для связывания циклических нуклеотидов; цинк связывающий элемент; Mg2+-связывающий регион DXXG (последовательность 590-593); и элемент NKXD (последовательность 762-765), отвечающий за специфичное связывание гуанинового кольца (аналогичная область ?-субъединицы трансдуцина участвует в связывании гуанинового кольца ГТФ), причем, в отличие от ?-субъединицы, у ?-субъединицы элемент NKXD изменяется до NKXA. Это может свидетельствовать о понижении сродства в цГМФ по сравнению с ?-субъединицей, или же ЭТОТ элемент ?-субъединицы вообще не вовлечен в связывание цГМФ.
Две ?-субъединицы связываются с димером ?? с очень высоким сродством. При этом гидролитическая активность димера ФДЭ?? ингибируется более чем в 100 раз. Соответствующие сайты связывания на ?-субъединице соответствуют последовательностям 467-491, 517-541 и 751-763. При этом если два первых участка не несут дополнительной функции, то третья область является частью каталитического домена на ар субъединицах Таким образом, ?-субъединицы непосредственно блокируют доступ цГМФ к каталитическим сайтам. Кроме того, на ??-субъединицах имеются области, отвечающие за взаимодействие с Т?.
?-субъединица состоит из 87 аминокислот и имеет молекулярную массу 11 кДа. При рассмотрении ингибирующего взаимодействия ФДЭ7 с ФДЭ?? в ?-субъединице было выявлено две основных области. Первый, центральный, поликатионный регион (последовательность 24-45) связывается с соответствующими участками на ??-субъединицах (последовательности 467-491? и 517-541 для ?-субъедчницы). Последние 5 -7 аминокислотных остатков С-концево- го участка у-субъединицы связываются непосредственно с каталитическими сайтами связывания цГМФ (последовательность 751 -763 для ?-субъединицы).
С другой стороны, у-субъединицы отвечают за активацию ФДЭ через взаимодействие с Т?-ГТФ. При этом с Т?-ГТФ связываются те же области, что и при взаимодействии с ??-димером. Таким образом, ?-субъединица является конкурентным ингибитором активности ФДЭ.
При рассмотрении аминокислот центрального поликатионного региона, отвечающих за взаимодействие с Т?, была выявлена критическая роль положительно заряженных Arg-33 и Arg-36. Вторым важным участком, реагирующим с Т?, является С-концевой участок ?-субъединицы (последовательность 46-87). Центральную роль в активации ФДЭ играет Cys-68-Tip-70. Исследование кристаллической структуры показало, что этот участок реагирует с а3/а4/б6-областыс Т?.
Другая физиологическая функция ?-субъединицы заключается в регуляции связывания цГМФ с некаталитическими сайтами связывания на ??-димере. Взаимодействие ФДЭУ с Т?-ГТФ понижает сродство цГМФ к некаталитическим сайтам связывания. Таким образом запускается описанный выше механизм регуляции ГТФафазной активности для Т?-ГТФ, в котором ФДЭТ принимает непосредственное участие.
Информация о структурных перестройках, сопровождающих активационное взаимодействие Т?-ГТФ с ФДЭТ, была получена в основном методами наблюдения резонансного переноса энергии. Для этого Cys-68 метили донорной меткой, тогда как акцепторная метка находилась среди первых семи аминокислот ?-субъединицы. Оказалось, что в растворе расстояние между донором и акцептором составило 63А, а при связывании ФДЭ? с ФДЭ?? это расстояние увеличивалось до 77А. Дальнейшее присоединение ГТФ?? не изменяло этого расстояния. Это говорит в пользу того, что взаимодействие Т? с ФДЭТ не вызывает значительных конформационных изменений в третичной структуре ФДЭГ а также подтверждает теорию активации ФДЭ, где Т? образует комплекс с голопротеином.
Арестин.Не менее интересен вопрос, каким образом молекула арестина распознает фосфорилированную форму родопсина и обеспечивает быстрое ингибирование активной формы рецептора.
Арестин состоит из 404 аминокислот. Его неактивная форма имеет двухчастичную архитектуру, состоящую из N- и С-доменов. N- и С-домены представляют собой относительно изолированные структуры, характеризующиеся высоким содержанием ? листов. Описанные домены связаны шарнироподобным соединением. В основном состоянии шарнир закрыт, т.е. оба домена максимально сближены. Кроме двух описанных доменов в молекуле арестина можно выделять С-концевой участок. В неактивной молекуле арестина он находится в заякоренном состоянии, связанном с обоими доменами.
Проведенные исследования позволили выделить ключевые участки арестина, которые отвечают за стабилизацию его основного состояния. Отщепление С-концевого участка приводило к тому, что арестин связывался с фотолизированной, но нефосфорилированиой формой родопсина. Таким образом, арестин без С-концевого пептида самопроизвольно переходит в активную форму. Аналогичный эффект наблюдался при исследовании мутантных форм арестина. Эти исследования позволили выявить основной регион, позволяющий арестину действовать как фосфатном) сенсору. Этот регион, названный полярным ядром, представляет собой необычную сеть заряженных аминокислотных остатков, находящихся глубоко внутри молекулы около точки шарнирного соединения N- и С-домечов. Зарядовый баланс в полярном ядре, образованный совокупностью ионных пар, позволяет арестину удерживать N- и С-домены сомкнутыми в базовом состоянии. Основной аминокислотой, ответственной за взаимодействие с фосфорилированным родопсином, является так называемый сенситивный триггер - Arg-175, который взаимодействует в полярном ядре со своим противоионом Asp-296. Так, при его замещении арестин мог связываться с нефосфорилированной фотолизированной формой родопсина. В целом мутации, изменяющие заряд в полярном ядре путем разрушения критических ионных пар или переустановкой зарядового баланса, приводили к тому, что арестин мог связываться с активированным нефосфорилированным родопсином. С другой стороны, комбинации мутации, которые сохраняли общий зарядовый баланс, позволяли арестину работать аналогично нативной форме. Таким образом, сохранение зарядового баланса полярного ядра является ключевым фактором, стабилизирующим неактивное основное состояние молекулы арестина.
Наиболее интересным представляется вопрос, каким образом происходит взаимодействие между фосфорилированным С-концевым пептидом родопсина и арестином, и какие структурные перестройки в молекуле арестина вызывает это взаимодействие.
Сайт связывания арестина с фосфорилированным С-концевым участком родопсина представляет собой подобие чаши, на дне которой находятся ключевые аминокислоты полярного ядра. Взаимодействие с фосфатными группами начинается еще до того как они достигнут дна чаши. Так, на уровне обода чаши находятся две положительно заряженные аминокислоты Lys-14 и Lys- 15, причем боковая цепь Lys-15 направлена внутрь чаши, а боковая цепь Lys-14 - наружу. Таким образом, для одновременного связывания фосфатных групп Lys-14 должен перевернуться. Вероятно, фосфатная часть родопсина встречается с Lys-14 и Lys-15 на ободе чаши и, продолжая двигаться внутрь, тянет за собой Lys-15 Далее либо движение Lys-15, дестабилизируя первый ?-лист, позволяет Lys-15 перевернуться, либо Lys-14 сам движется за фосфатом, и в результате происходит серьезный изгиб, а, возможно, и полное разрушение первого ?-листа. Разрушение первого ?-листа приводит к двум последствиям: позволяет занять Lys-14 и Lys-15 предпочтительные места для взаимодействия с фосфатными группами, уже достигшими дна чаши и приводит к смещению гидрофобных элементов Val-IIe-Phe в позицию, исключающую их взаимодеиствие с гидрофобными Phe-Val- Phe из С-концевого пептида. Как результат С-концевой пептид арестина перестает быть заякоренным и отходит от поверхности N-домена.
Фосфатные группы, достигнув дна чаши, непосредственно взаимодействуют с положительно заряженными аминокислотными остатками полярного ядра. Таким образом, фосфатные группы разрушают зарядовый баланс полярного ядра двумя путями. Во-первых, фосфаты взаимодействуют с Lys-14 и Lys-15, вызывая разрушение первого б-листа, что в свою очередь освобождает С-хвост арестина, и это приводит к отдалению положительно заряженного Arg-382 из полярного ядра. Во-вторых, фосфатные группы сами нейтрализуют другие положительные заряды в полярном ядре, в том числе и сенситивный триггер Arg-175, разрушая его связь с Asp-296.
В результате этих перестроек три отрицательно заряженные аминокислоты, находящиеся на оси шарнира, остаются без стабилизирующих противоионов, и их взаимное электростатическое отталкивание приводит к глобальным перестройкам, включающим движение N- и С-доменов относительно друг друга. Эти перестройки переводят аминокислоты, участвующие в связывании рецептора, в положение, соответствующее структуре цитоплазматических петель родопсина.
Сколько фосфатных групп необходимо для эффективной активации арестина? В основном состоянии расстояния между аминокислотными остатками арестина, вовлеченными в связывание с фосфатами родопсина, составляют около 15Ао (между Lys- J 5—Arg-175 - 15А, между Arg-171-Arg-175 - 14,5?). Благодаря описанным выше перемещениям Lys-15 по направлению к полярному ядру расстояние между Lys-15-Arg-175 значительно сокращается. Но сближение Arg-171-Arg-175 невозможно без разрушения ?-листа X. Таким образом, одной фосфатной группы оказывается недостаточно, чтобы достигнуть всех сайтов связывания. Количество положительных аминокислотных остатков, вовлеченных во взаимодействие с фосфатами (Lys-14 и Lys-15 на ободе чаши, Arg-171, Arg-175 и Lys-176 - в полярном ядре), также подтверждает эту точку зрения. Эксперименты по прямому связыванию показали, что на одну молекулу арестина требуется по крайней мере две фосфатные группы.
Статья из книги: Молекулярные механизмы зрительной рецепции | Каламкаров Г.Р., Островский М.А..



Комментариев 0