Посттравматическая офтальмогипертензия и глаукома (Часть 1)

Содержание:
Описание
↑ ЭТИОПАТОГЕНЕЗ
В настоящее время не существует четкого общепринятого понятия посттравматической глаукомы (ПГ). По данным литературы, одни авторы (Р. А. Гундорова, А. А. Малаев, А. М. Южаков; Р. А. Гундорова, А. В. Степанов) под ПГ понимают вторичную глаукому, возникающую после механических повреждений органа зрения, другие авторы к ПГ относят также послеожоговую глаукому. В некоторых работах из вторичной глаукомы выделяется послеоперационная глаукома.
Учитывая такую разноречивость мнений ученых, мы обратились к различным источникам в поисках понятия травмы. В книге В. В. Волкова и В. Г. Шиляева «Общая и военная офтальмология» подчеркивается, что всякое нарушение функций или структуры органа зрения в ответ на воздействие извне физических или химических факторов следует рассматривать как повреждение глаза, его травму в широком смысле слова.
В энциклопедическом словаре медицинских терминов под травмой понимается нарушение целости и функций тканей (органа) в результате внешнего воздействия. Е. К. Гуманенко травму рассматривает как общий результат взаимодействия человеческого организма в целом с окружающими факторами в экстремальных ситуациях при конкретных условиях внешней среды и оказания медицинской помощи. Понятие «травма» включает два компонента: повреждение (морфологический компонент) и состояние раненого (функциональный компонент).
Повреждение — результат воздействия ранящих агентов, поражающих факторов (термический, химический, радиационный и др.) либо окружающих предметов на конкретные ткани, органы или системы человеческого организма.
Таким образом, учитывая понятие «травма», можно считать, что ПГ вызывается не только механическим, включая операционное, повреждением глаза, но и любым поражающим фактором (термическим, химическим, радиационным, СВЧ-полем и др.), приведшим к нарушению функций или структуры органа зрения.
В отечественной и зарубежной литературе под глаукомой, в том числе и посттравматической, понимается симптомокомплекс, включающий предложенную еще в 1857 г. Грефе систему признаков, но с изменением акцентов и значимости каждого признака в соответствии с современными достижениями науки.
Так, В. В. Волков, развивая механическую концепцию патогенеза глаукомы, которая опирается на морфологические исследования А, С. Новохатского, полагает, что глаукома — это прежде всего специфическое нарушение зрительных функций как результат сдавливания, а затем и атрофии зрительно-нервных волокон в склеральном канале вследствие прогибания решетчатой пластинки.
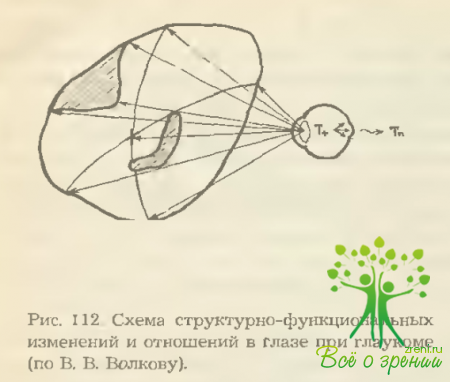
В 1974 г. В. В. Волков предложил свою теорию происхождения экскавации и зрительных нарушений при глаукоме, основанную на изменении соотношения внутриглазного и внутричерепного давления, составляющего в норме, по данным экспериментальных исследований В. В. Волкова, Р. И. Коровенкова, 2:1. Автор полагает, что экскавация образуется не только за счет повышения уровня давления в глазу, но, хотя и реже, также за счет снижения его в полости черепа, что встречается при артериальной гипотонии.
А. П. Нестеров полагает, что глаукома, особенно вторичная, возникает прежде всего из-за ухудшения оттока водянистой влаги из глаза. Ее сущность заключается в повышении внутриглазного давления (ВГД), а поражение зрительного нерва является отдаленным последствием болезни.
Повышение ВГД после травмы глаза, не сопровождающееся характерными изменениями в состоянии диска зрительного нерва (ДЗН), а также центрального и периферического полей зрения, следует расценивать как посттравматическую офтальмошпертензию. В. В. Волков и соавт. подчеркивают, что единственным надежным дифференциально-диагностическим признаком офтальмогипертензий неглаукоматозной и глаукоматозной природы является переносимость их глазом.
По данным В. К. Скрипки и Г. Е. Венгер и соавт., в ближайший после травм глаза период вторичная глаукома выявляется в 12-33 случаев, а в отдаленные сроки— уже в 27-50% случаев. В. К. Скрипка считает, что после контузии глазного яблока ПГ развивается почти в 2 раза чаще, чем после проникающего ранения. Р. А. Гундорова и соавт. полагают, что проникающее ранение чаще приводит к развитию вторичной глаукомы.
ПГ является одной из основных причин слепоты и инвалидности при глазном травматизме— до 35,7%. Важность проблемы обусловлена социальной значимостью этого заболевания, поражающего людей работоспособного возраста.
В настоящее время в литературе нет единого взгляда на механизм повышения внутриглазного давления при ПГ. Некоторые авторы повышение офтальмотонуса в ранние сроки после травмы глаза связываю с сосудисто-нервными нарушениями.
[banner_centerrs] {banner_centerrs} [/banner_centerrs]
В связи с этим Г. Е. Венгер и соавт. выделяют три фазы развития ПГ:
- I — фаза ранних функциональных реактивных изменений в ответ на перенесенную травму;
- II — фаза компенсации;
- III — фаза поздних деструктивных изменений в глазу, развивающихся вследствие травмы.
Безусловно, важную роль в патогенезе ПГ имеет механический фактор. Так, Р. А. Гундорова и соавт. полагают, что местные
механические факторы все же играют решающую роль в развитии ПГ.
К. БИа и соавт. считают, что ПГ может развиться при поражении периферическими синехиями более половины радужно-роговичного угла. В. К. Скрипка отмечает, что тяжелые ожоги (IV степени) лишь у 5 из 12 исследуемых сопровождались повышением ВГД, а после прободных ранений ПГ наблюдалась у 30-40 % пострадавших. По наблюдениям Л. Б. Сухининой, лишь в двух глазах из 12 с посттравматической офтальмогипертензией развивается глаукома.
По данным литературы, при анализе возможных причин развития ПГ наиболее часто называют передние синехии, к которым нередко приводят проникающие ранения глазного яблока. ПГ возникает при этом в 30~64% случаев.
Второй из наиболее распространенных причин ПГ считают травму хрусталика. Она приводит к развитию вторичной глаукомы в 30-40% случаев. В зависимости от особенностей травмы хрусталика ПГ может быть факоморфической, факолитической и факотопической.
Более 25 лет назад установлен неизвестный ранее механизм образования витреохрусталикового, а в афакичном глазу — витреоцилиарного блоков. Причиной этих блоков является скопление внутриглазной жидкости в ретровитреальном пространстве, что ведет к развитию заднего витреального блока, отягощающего течение глаукомы и превращающего ее в «злокачественную».
Одной из причин возникновения ПГ являются внутриглазные кровоизлияния. Так, в 17% случаев травматической гифемы наблюдал повышение ВГД на 5-6-й день.
Ряд авторов связывают развитие ПГ после контузии глазного яблока с травматической рецессией радужно-роговичного угла.
В части случаев причиной развития ПГ может быть разрастание в ПОЛОСТИ глаза после травмы соединительной ткани, блокирующей радужно-роговичный угол или область зрачка в виде ретрокорнеальных, предзрачковых, зрачковых и позадизрачковых пленок. Развитие вторичной глаукомы после проникающего ранения глаза может быть обусловлено также врастанием эпителия в переднюю камеру по раневому каналу.
По данным Н. Ф. Бобровой, развитие ПГ при травматической аниридии наблюдается в 43—45 % случаев.
Имеются многочисленные сообщения о развитии вторичной глаукомы при длительном пребывании в глазу металлических инородных тел, а также после кератопластики.
Изложенное выше позволяет сделать вывод, что ПГ является полиэтиологичным заболеванием. Как показали наблюдения А. В. Степанова, патогенез и особенности клинического течения глаукомы не зависели от вида предшествующей травмы: проникающее ранение или контузия больше определялось тяжестью и особенностями травмы, травматическими изменениями глазного яблока, течением раневого процесса.
Многообразие клинических форм, полиэтиологичность и полипатогенетичность ПГ затрудняют выбор единой классификации заболевания. Так, Р. А. Гундорова и А. В. Степанов предлагают следующую патогенетическую классификацию посттравматической глаукомы.
- Адгезивная форма.
- Пролиферативная форма:
- фиброзно-пролиферативная;
- эпителиально-пролиферативная;
- кистозно-пролиферативная.
- фиброзно-пролиферативная;
- Геморрагическая форма.
- Факогенная форма.
- Факотопическая форма.
- Витреотопическая форма:
- передний витреальный блок;
- задний витреальный блок.
- передний витреальный блок;
- Металлозная форма.
- Ангулярная форма:
- гониоадгезивная;
- рецессионная.
- гониоадгезивная;
- «Неотягощенная глаукома».
А. В. Степанов с целью патогенетически ориентированного микрохирургического лечения ПГ считает целесообразным условное выделение трех патогенетических групп:
- глаукома «увеального» генеза (50,4 %);
- глаукома «неопролиферативного» генеза (6,9 %);
- глаукома «эктопического» генеза (42,7 %)
Д. С. Кроль и соавт. предлагают свою патогенетическую классификацию вторичной травматической глаукомы:
1. Вид:
- контузионная;
- раневая;
- комбустионная;
- послеоперационная;
- первичная скрытопротекающая, спровоцированная травмой
2. Форма:
- закрытоугольная;
- открытоугольная;
- открытоугольная с блокированным углом передней камеры (УПК).
3. Время развития:
- ранняя;
- поздняя.
4. Генез (при возможности определения):
- факогенная;
- витреотопическая;
- гемогенная;
- ангулярная.
5. Стадия (при возможности определения)
- начальная;
- развитая;
- далеко зашедшая;
- терминальная.
6. Уровень ВГД:
- нормальный;
- умеренно повышенный;
- высокий.
7. Состояние зрительных функций:
- стабилизированное;
- дестабилизированное.
Мы полагаем, что, несмотря на различные патогенетические механизмы возникновения вторичной и первичной глаукомы, вторичная глаукома имеет те же формы, стадии и степень стабилизации зрительных функций, что и первичная. С этой точки зрения наиболее полной как по форме, так и по содержанию можно считать патогенетическую классификацию вторичной травматической глаукомы, предложенную Д. С. Кролем. Т. А. Мясниковой, Ю. А. Труниной. Однако надо иметь в виду возможность сочетания разных механизмов и причин, вызвавших ПГ, поскольку это требует индивидуализации в диагностике и комбинациях хирургических вмешательств.
↑ ДИАГНОСТИКА
Общепризнанно, что эффективной профилактикой слепоты от глаукомы, в том числе посттравматической, является ее ранняя диагностика, которая позволяет своевременно начать лечение и тем самым сохранить зрение на долгие годы.
За рубежом диагностика глаукомы основывается на оценке прежде всего состояния ДЗН, центрального и периферического полей зрения, уровня офтальмотонуса. В. В. Волков и соавт., развивая механическую концепцию прогрессирования экскавации, подчеркивают, что наиболее важным проявлением глаукомы как болезни следует признать утрату зрительных функций по определенному типу и предлагают по закону соответствия структуры и функции принять за морфологическую основу диагноза «глаукома» состояние ДЗН, его офтальмоскопическую картину.
Существующие сегодня доказательства в пользу преимущественно механического генеза глаукоматозной атрофии ДЗН представляются довольно убедительными. Пожалуй, самым ярким из них является факт обратимости в некоторых случаях экскавации ДЗН. В последние 10~15 лет в отечественной и зарубежной литературе много внимания уделяется этому вопросу.
В соответствии с двумя основными механизмами в генезе глаукоматозной экскавации возникло представление о существовании двух типов экскавации — первичной (степень прогибания — одно из проявлений дестабилизации глаукоматозного процесса) и вторичной (зона атрофии — признак его выраженности).
Смешанная экскавация, являясь сочетанием первичной и вторичной, несет в себе потенциальную возможность частичной обратимости, т. е. уменьшения размеров за счет ослабления прогибания решетчатой пластинки после снижения уровня офтальмотонуса.
Наиболее важными характеристиками экскавации ДЗН при глаукоме В. В. Волков и соавт. считают:
- отношение максимального диаметра экскавации к диаметру ДЗН;
- наличие асимметрии в размерах экскавации парных глаз;
- склонность к дальнейшему ее расширению, особенно по вертикали.
Если наличие асимметрии в размерах экскавации парных глаз всеми авторами признается важным диагностическим признаком, то в отношении нормативов размеров экскавации, по данным литературы, полного согласия нет.
По наблюдениям В. В. Волкова, А. И. Журавлева, И. JI. Симаковой, размеры экскавации 0,4—0,5 при наличии асимметрии уже определяют I стадию глаукомы, конечно, если они подтверждены также специфическими нарушениями в центральном поле зрения.
С целью исследования истинных размеров ДЗН и экскавации И. Л. Симаковой и соавт. было разработано устройство для измерения объектов глазного дна. Устройство использовано И. Л. Симаковой с целью измерения максимального и минимального диаметров как ДЗН, так и экскавации в здоровых глазах и в глазах с открытоугольной глаукомой.
Разработанная методика служит для более точного измерения при офтальмоскопии плоскостных параметров объектов глазного дна, в том числе и ДЗН, в абсолютных величинах с учетом длины переднезадней оси глазного яблока и степени аметропии.
По данным некоторых зарубежных авторов, а также наших исследований, возникновение нарушений в поле зрения зависит не столько от формы и величины экскавации, сколько от состояния кольца нервной и глиальной тканей ДЗН вокруг экскавации, названного нами нейроретинальным пояском (НРП), а его площадь — индексом сохранности площади, занимаемой в ДЗН продолжающими функционировать зрительно-нервными волокнами.
При оценке глаукомы полезно учитывать не только соотношение Э/Д, т. е. экскавации к диску, но и площадь НРП. Последняя нами рассчитана в относительных единицах по величине соотношения Э/Д и в абсолютных единицах по измерениям диаметров ДЗН и экскавации, полученных с помошью специального устройства.
В современных зарубежных и отечественных публикациях пристальное внимание уделяется глубине экскавации. Обычно она оценивается опосредованно по ходу и изгибу сосудов на диске, параллаксу его деталей при небольшом смещении светового пучка относительно поверхности ДЗН. А. С. Новохатский указывает, что в здоровых глазах центр диска западает в пределах 0,7_2,0 дптр, т. е. на 0,23—0,66 мм. G. L. Portney фотограмметрическим способом определил, что в норме глубина экскавации составляет 0,18—0,58 мм, а при глаукоме она увеличивается до 0,58-0,88 мм.
Безусловно, наиболее точные результаты морфометрии ДЗН получены с помощью ретинального анализатора (ретинального томографа) фирмы «Humphrey» или «Rodenstock». Так, J. Dandona и соавт., занимаясь топографическим картографированием глазного дна с помощью ретинального анализатора «Humphrey», определили глубину экскавации в здоровых глазах в пределах лишь 165,6 ± 8,7 мкм, а при глаукоме — 305 ± 49,4 мкм
В ранней диагностике глаукомы в последние годы все большее значение придают результатам злектрофизиологического исследования органа зрения. О значимости флюоресцентной ангиографии ДЗН с этой целью мнения авторов разноречивы.
Согласно исследованиям М. В. Волковой и Е. А. Егорова, ранние изменения ДЗН при начальной глаукоме встречаются по крайней мере в 2/3 всех наблюдений. В последнее время все больше высказываний в пользу того, что самые ранние изменения при глаукоме возникают в ДЗН. По данным Л. П. Козловой, Н. А. Листопадовой, Т. В. Романовой, при начальной глаукоме изменения в поле зрения опережают изменения в ДЗН в 40-48 % случаев.
До сих пор в широкой практике отечественной офтальмологии при исследовании поля зрения наибольшее внимание уделяют проверке периферических его границ. Хотя уже убедительно показано, что для начальной стадии глаукомы характерно возникновение небольших изменений прежде всего в парацентральных участках поля зрения при нередко нормальных периферических его границах.
Сегодня ведущая роль в ранней диагностике глаукомы по праву принадлежит центральной статической периметрии, методики которой подробно описаны в отечественной литературе.
В клинике офтальмологии ВМедА последние 25 лет для исследования центрального поля зрения используется множественная центральная статическая периметрия (МЦСП-60 точек) в модификации В. В. Волкова и соавт., а для диагностики глаукомы — прибор Волкова—Сухининой—Тер-Андриасова «Глаукотестер-2» (рис. 113).
На экране прибора по принципу множественной центральной статической периметрии определяют порог различения яркости в 6 наиболее чувствительных при глаукоме точках. Казалось бы, при очень малом количестве исследуемых точек нельзя исключить возможность ошибочно-отрицательных результатов центральной статической периметрии.
Однако положительный результат этого исследования был высоко достоверен, особенно при нагрузочной вакуум-периметрической пробе (ВПП).
Как показал с 1973 г. наш клинический опыт, основанный на результатах нескольких десятков тысяч исследований, КПП, а затем ВПП Волкова—Сухининой—Тер-Андриасова оказалась надежным дифференциально-диагностическим тестом, позволившим по определенной схеме выделять преглаукому из разного рода других неглаукоматозных офтальмогипертензий, а кроме того, судить о стабилизации глаукоматозного процесса при уже выявленном заболевании.
В последние годы в клинике офтальмологии ВМедА в ранней диагностике глаукомы широко используется цветовая кампиметрия в виде комплекса компьютерных методик, разработанных в Московском НИИ глазных болезней им. Гельмгольца Л. И. Нестерюком и А. М. Шамшиновой.
В отечественных публикациях за последние годы многими авторами отмечаются высокая чувствительность и специфичность визоконтрастометрии (ВКМ) в ранней диагностике глаукомы. Так, А. М. Шамшинова и соавт. отмечают, что снижение контрастной чувствительности (КЧ) предшествовало изменениям в полях зрения и остроте зрения.
Как показали исследования И. Л. Симаковой, чем больше стадия глаукомы, тем ниже располагается вся кривая видеограммы. Автором также отмечается, что использование сине-белых решеток в начальной и развитой стадиях глаукомы никаких преимуществ перед черно-белыми не имеет. Применение при ВКМ зеленого фильтра или таблиц с решетками зеленого цвета позволяет в более ранние сроки выявить изменения, характерные для ПГ.
Н. А. Листопадова и Э. В. Хадикова провели сравнительную оценку некоторых компьютерных методик исследования зрительных функций при ранней диагностике глаукомы и пришли к выводу, что наиболее чувствительными методами являются компьютерная кампиметрия (66 %), статическая пороговая периметрия (48 %) и ВКМ (40 %).
По нашим наблюдениям, ВКМ признана высокочувствительной и специфичной методикой как в ранней диагностике глаукомы, так и в оценке стабилизации глаукоматозного процесса после оперативного лечения. Но при комбинации глаукомы с иной глазной патологией специфичность ВКМ заметно снижается.
Сегодня уже очевидно, что тонометрия и тонография, а также исследования структур переднего отдела глаза, в частности путем биомикрогониоскопии, не могут быть отнесены к основным приемам ранней диагностики преглаукомы и глаукомы.
По данным И. Л. Симаковой, в отдаленные сроки наблюдения в 15 % случаев во II стадии ив 25% случаев в III стадии глаукомы распад зрительных функций продолжался, несмотря на, казалось, достигнутую после операции стойкую офтальмонормотонию.
Гониоскопические и тонографические исследования при ПГ, на наш взгляд, важнее, чем при первичной глаукоме. Их применяют для уточнения локализации и характера нарушения гидродинамики, чтобы выбрать адекватное консервативное, лазерное или хирургическое лечение.
↑ ЛЕЧЕНИЕ
Учитывая сложность лечения и тяжелые исходы ПГ, практически все авторы указывают на важность и необходимость проведения профилактических мероприятий. Важнейшим профилактическим мероприятием ПГ после проникающих ранений глаза является своевременная и рациональная хирургическая обработка раны (удаление внутриглазных инородных тел, крови, добавление антиглаукоматозного компонента, если рана идет через лимб). В настоящее время, с развитием витреальной хирургии, необходимо производить отсасывание стекловидного тела и тогда, когда иридохрусталиковую диафрагму надо сместить кзади, предотвратить тампонаду базальной колобомы радужки стекловидным телом.
При контузиях глазного яблока предупреждение ПГ заключается в ранней противовоспалительной терапии, в своевременной ликвидации болевого синдрома, внутриглазных кровоизлияний. Для устранения посттравматической гифемы или гемофтальма можно использовать ферменты.
При выявлении ПГ лечение ее обычно начинают с назначения мистических средств и препаратов, угнетающих секрецию внутриглазной жидкости.
К современным гипотензивным препаратам в офтальмологии относятся:
I. Препараты, уменьшающие приток внутриглазной жидкости:
- р-блокаторы:
- неселективные (тимолол малеат, левобунолол и др.);
- селективные (бетаксолол или бетоптик);
- неселективные (тимолол малеат, левобунолол и др.);
- а2-адреноагонисты (клофелин, апраклонидин, бромонидин);
- ингибиторы карбоангидразы (ацетазоламид, метазоламид, диакарб, дорзоламид или трусопт).
II. Препараты, увеличивающие отток внутриглазной жидкости:
- простагландины (латанапрост, унопростоун);
- адренергические препараты (адреналин, эпинефрин,
III. Комбинированные препараты: тимпило, фотил.
Следует помнить о возможности инвертного типа кривой суточной тонометрии при ПГ и учитывать этот факт при назначении режима инстилляций. Перечисленные выше препараты можно комбинировать, но из разных групп, а р-блокаторы следует менять через 2—3 месяца из-за развития синдрома привыкания.
Необходима также медикаментозная коррекция гемоциркуляторных и метаболических нарушений. Эффективность проводимой терапии должна оцениваться исследованием центрального и периферического полей зрения, состояния ДЗН, частотно-контрастных характеристик, офтальмотонуса в динамике, а также результатами ВПП Волкова—Сухининой—Тер-Андриасова. По данным Р. А. Гундоровой и соавт., только консервативного лечения ПГ обычно недостаточно, оно эффективно лишь в 11,5% случаев.
А. В. Степановым очень четко обозначены задача, пути ее достижения, показания и противопоказания при хирургическом лечении ПГ.
Задача хирургического вмешательства при ПГ — нормализация ретенции внутриглазной жидкости.
Эта задача может быть достигнута следующими путями:
- устранением посттравматических изменений, нарушающих нормальную ретенцию внутриглазной жидкости;
- дополнительной активизацией ретенции внутриглазной жидкости;
- снижением уровня секреции внутриглазной жидкости.При определении показаний к хирургическому лечению глаукомы необходимо четко сформулировать цель предстоящей операции. Это может быть — улучшение зрительных функций, сниженных из-за сопутствующих изменений преломляющих сред глаза;
- сохранение или улучшение имеющихся зрительных функций за счет нормализации офтальмотонуса при отсутствии изменений преломляющих сред в оптической зоне;
- сохранение удовлетворительной косметики травмированного глаза при терминальной и далеко зашедшей глаукоме.



Комментариев 0