Работа операционной медицинской сестры
Содержание:
Описание
Операционная является «душой» глазного отделения. В глазной операционной проходит ответственная и напряженная работа по возвращению зрения людям, потерявшим ото. Успех этой работы в большой мере зависит от «случайностей» и «мелочей», которые в значительной степени могут быть предусмотрены операционной медицинской сестрой. От постановки работы, устройства операционной, оборудования, качества инструментария, асептики при проведении операции зависит уровень и успех работы отделения.Какими деловыми качествами должна обладать хирургическая операционная медицинская сестра, обще-известно. Все эти качества должны быть присущи и глазной операционной медицинской сестре.
Среди требований, предъявляемых к глазной операционной медицинской сестре, на первое место следует поставить поддержание асептики в операционной на высоком уровне, так как малейшая погрешность асептики по отношению к инструментарию, перевязочному материалу и др. может привести к роковому исходу — к гибели глаза после операции. Это не трудно понять: глаз представляет собой закрытую полость, заполненную стекловидным телом, которое является хорошей средой для развития микробов. Операционная медицинская сестра является опорой заведующего отделением.
↑ Особенности устройства и оборудования глазной операционной
Требования общей хирургии к устройству операционной полностью применимы и для глазной операционной. Основным условием для асептического проведения операции является устройство отдельной операционной для асептических операций и другой — для гнойных операций.

Большое значение в работе глазной операционной имеет хорошее освещение операционного поля. Во время операций в операционной не должно быть яркого естественного освещения. Рекомендуется также стекла того окна, от которого падает свет на операционный стол, делать матовыми. В некоторых операционных часть окон окрашивают в черный цвет, что особенно важно для офтальмоскопии при операциях по поводу отслойки сетчатки, удалении инородных тел из глаза и в других случаях. Для создания хорошего освещения операционного поля целесообразно использовать широко распространенные в настоящее время бестеневые лампы, висящие над столом, или с боковым освещением.
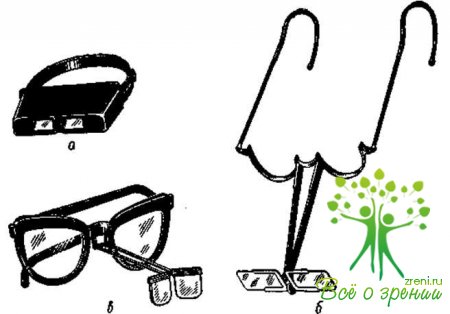
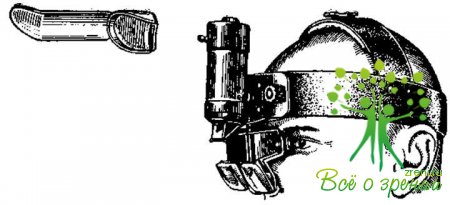
В операционной должны быть гигантский электромагнит, ручной постоянный магнит Кальфа — Бродского, новая модель ручного магнита (рис. 25), глазной диатермокоагулятор (рис. 26), разные модели бинокулярных луп (рис. 27, а, б, в), криоманипуляторы, диафаноскоп, гониолинза (рис. 28), офтальмоскоп, лобный бинокулярный офтальмоскоп (модель А. И. Горбаня, рис. 29), набор криоаппликаторов для удаления инородных тел и опухолей глаза (Р. А. Гундорова) (рис. 30), электронный локатор для диагностики внутриглазных инородных тел (рис. 31), баллон с углекислотой для экстракции катаракты, орбитальный шпатель-световод (А. Ф. Бровкина), приборы для фотокоагуляции при отслойке сетчатки, пинцет с вмонтированным световодом (Р. А. Гундорова), микрокаутер с питанием от батареи в ручке инструмента (М. М. Краснов), маска Рославцева и др.
Все эти приборы должны находиться в отдельной комнате, входящей в операционный блок, или в предоперационной и в случае необходимости их вносят в операционную. Приведем краткое описание криоманипуляторов, а также двух новых приборов-инструментов.
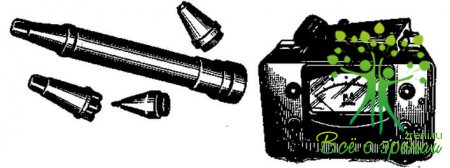
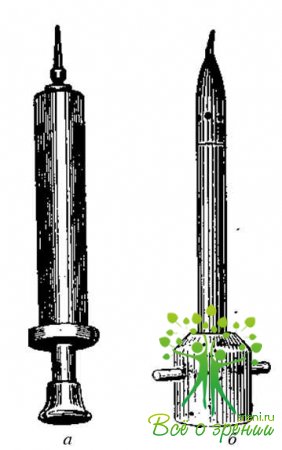
Криоманипуляторы (рис. 32). Криоманипуляторы — инструменты для воздействия на глаз низкой температуры, отличающиеся друг от друга по принципу охлаждения, по методу подведения к прибору охлажденного агента. По способу охлаждения различают инструменты, работающие на жидком газе, фреоне, хлорэтиле, углекислоте, термоэлектрические. Наибольшее распространение получили криоманипуляторы, которые охлаждаются с помощью углекислоты.
Криоманипулятор Зумбулидзе (рис. 32, а). Это двадцатиграммовый болгарский нейлоновый шприц для инъекций, в цилиндр которого вмонтирован медный стержень длиной 8 см, диаметром 5 мм. На стержень навинчивают медный хромированный наконечник. Шприц заполняют снегом угольной кислоты, в результате чего охлаждается стержень и наконечник.
Основным преимуществом криоманипулятора Абрамова и Пимашина (рис. 32, б) является то, что при пользовании им исключается примораживание радужки во время экстракции катаракты.
Орбитальный шпатель-световод (рис. 33) дает возможность осветить ткани, в частности опухоль в глубине орбиты. Он состоит из пластмассового корпуса черного цвета, в котором помещен источник света и набор шпателей-световодов, состоящих из полиметилкрилата.
Наконечник светится ярко. Стерилизуют в растворе диоцида 1:500.
Использование шпателя при поднадкостничной орбитотомии очень важно для исследования костных стенок у вершин орбиты.
Пинцет с вмонтированным световодом (рис. 34) дает возможность освещать область расположения ос-колка и четко его видеть при введении пинцета в переднюю камеру и стекловидное тело в процессе удаления инородного тела из глаза.
В предоперационной должен быть список антибиотиков, которые можно вводить под конъюнктиву, в переднюю камеру, стекловидное тело, и их дозировка1 (табл. 1). В крупных операционных имеются подвесные бестеневые лампы с телевизионной установкой, установка для кондиционирования воздуха.
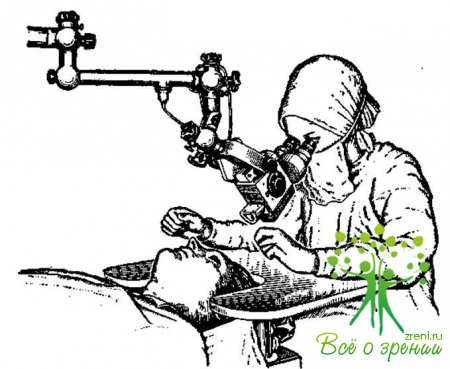
В последние годы в практику работы офтальмохирурга все больше входит производство операций под операционным микроскопом (рис. 35). Операционный микроскоп дает возможность видеть глаз в большом увеличении, что чрезвычайно важно, так как операции могут быть выполнены более тщательно. Для работы под операционным микроскопом требуется тонкий, так называемый микрохирургический инструментарий (см. с. 150), набор которого имеется во многих клиниках нашей страны.
От операционной медицинской сестры требуются тщательный уход за глазным инструментарием и осторожное с ним обращение. Чтобы проникнуться общехирургическими принципами, глазной операционной медицинской сестре полезно поработать в хирургическом отделении.
↑ Подготовка перевязочного материала и белья
Во время операций на глазу для ограничения операционного поля удобно пользоваться простынями с круглым отверстием диаметром 6—8 см. Края этого отверстия Должны быть тщательно обшиты. Отверстие нужно вырезать не в середине простыни, а ближе к ее краю, приблизительно на границе внутренней и средней трети, соответственно правому и левому глазу. Для операции по поводу косоглазия и птоза в простыне делают два отверстия, одно из них закрывают откидной салфеткой в виде клапана.
Примечание. 1. В 1 мг обычно содержится 1000 ЕД. 2. В скобках в графе «Под конъюнктиву» указано количество вводимого раствора. 3. В стекловидное тело вводят 0,1 мл раствора с соответствующим количеством антибиотика.
При пользовании перчатками следует к рукавам халата пришить трикотажные нарукавники, что более удобно для оператора, чем завязывание рукавов халата тесемками. При отсутствии таковых некоторые рекомендуют пришивать к рукавам халата одну длинную тесемку вместо двух, что дает возможность хирургу завязывать рукава самому.
Для работы в операционной используют такой же перевязочный материал, как и для перевязок: ватно-марлевые подушечки, палочки с туго намотанной ватой и др. Методика приготовления указанного перевязочного материала была описана в главе III. Остановимся только на приготовлении ватных тампонов, имеющих форму сигарет, которые применяются для осушивания операционного поля при операциях на глазном яблоке. Методика их приготовления следующая. Вату смачивают водным раствором бриллиантового зеленого 1:5000 или раствором оксицианата 1:5000, отжимают, расслаивают и рвут на куски величиной с ладонь. Далее закладывают края в лоскуте ваты и последний туго скатывают на стекле. Концы тампона обрезают ножницами. Указанные тампоны имеют длину 4—5 см. Толщина их бывает разной. Тонкие ватные тампоны используются во время операции пересадки роговицы, экстракции катаракты и др., толстые —при операции на слезных путях. Хорошо скатанные тампоны при высушивании раны не прогибаются.
Лучше скатывание «сигарет» производить не пальцами на стекле, а при помощи деревянной доски с ручкой, что значительноускоряет приготовление тампонов (рис. 36) и делает их более устойчивыми к прогибанию. Перед употреблением тампоны укладывают в биксы и стерилизуют в автоклаве. Подавая «сигарету», следует держать ее посередине, а не за концы, которые соприкасаются с раной.
Некоторые офтальмохирурги пользуются бумажными фильтрами от сигарет, кусочками синтетической губки, которые фиксируют пинцетом. Можно не высушивать рану, а промывать ее балансированным раствором. Для этого раствор набирают в резиновую грушу, в которую вставляют микропипетку.

Для стерилизации перевязочного материала лучше пользоваться малыми биксами, материал которых может быть использован на протяжении 1 дня.
Следует еще раз подчеркнуть, что перевязочный материал для глазных операций должен быть изготовлен только из гигроскопической ваты. Для магнита и рукоятки от диатермии должны быть сшиты мешочки, оставляющие незакрытыми только наконечник. Наконечники подвергаются кипячению. На методах стерилизации перевязочного материала мы останавливаться не будем, так как они известны из общей хирургии.
↑ Стерилизация глазного инструментария
Существуют разные способы стерилизации глазного инструментария: сухим жаром, текучим паром, с использованием различных дезинфицирующих веществ и др. Остановимся на некоторых из них.
1. Нережущий инструментарий, в разобранном виде кипятят в 1—2% растворе соды (бикар-бонат натрия) в течение 30 мин с момента закипания воды. Вода должна быть дистиллированной. Стерилизатор перед заправкой инструментами моют щеткой в горячей воде с мылом и гидрокарбонатом натрия, после чего насухо вытирают.
Рекомендуется опускать инструменты в кипящую воду, что предохраняет их от ржавчины.
Добавление гидрокарбоната натрия имеет двоякое значение. Во-первых, гидрокарбонат натрия предохраняет инструменты от окисления, т. е. от появления ржавчины. Кроме того, щелочь (гидрокарбонат натрия) повышает температуру кипения воды. При этом споры микробов разбухают и скорее погибают. Таким образом, добавление 1—2% раствора гидрокарбоната натрия значительно повышает антимикробное действие кипящей воды. Образующуюся накипь очищают механически, вытирая салфеткой. Раствор гидрокарбоната натрия, приготовленный на дистиллированной воде, накипи не дает. Если в стерилизатор во время стерилизации помещают добавочные инструменты, надо продлить время кипячения.
Для производства гнойных операций необходимо выделить специальный инструментарий. Инструменты, бывшие в соприкосновении с гнойной раной, моют водой, затем щеткой или марлевой салфеткой в 5% растворе лизола. После 10-минутного пребывания в лизоле инструменты кипятят в течение часа и повторяют кипячение на следующий день.
П. С. Плитас рекомендует инструменты после гнойных операций заливать раствором следующего состава:
[banner_centerrs] {banner_centerrs} [/banner_centerrs]
Rp. Acidi carbolici liq.
Liq. ammonii caust. ?? 50,0
Aq. destill. 1000
Этот раствор хорошо смывает кровь и гной и предохраняет инструменты от ржавчины.
Режущий глазной инструментарий кипятить нельзя, так как при кипячении он притупляется. В настоящее время известно несколько способов стерилизации режущего инструментария.
Техника заливки режущего инструментария 96° спиртом такова: на дно стерилизатора или лотка укла-дывают металлическую подставку с отдельными гнездами в поперечном направлении, затем раскладывают глазной инструментарий так, чтобы его режущий край находился выше, а ручка ниже.
Инструменты укладывают в ряд, причем так, чтобы они не касались друг друга. Трепаны без защитных колпачков нужно положить между ручками инструментов. При отсутствии металлических подставок под инструменты можно подложить алюминиевую палочку. Сверху лоток покрывают крышкой.
Особое внимание требуется при стерилизации трепанов, так как малейший удар по режущей коронке трепана делает его тупым.
Иглы для инъекций и для швов можно кипятить, но роговичные иглы лучше стерилизовать в спирту, так как режущий кончик иглы от кипячения легко притупляется.
Наилучшими являются так называемые атравматические иглы. Последние отличаются от обыкновенных тем, что у них нет ушка, а конец нити вделан в задний цилиндрический конец иглы и составляет как бы ее продолжение. Этим избегают травматизации тканей при продергивании ушка иглы.
Способ Баккала. Режущий инструментарий помещают в 1% раствор бриллиантового зеленого, растворенного в 96° спирту. По наблюдениям автора, при этом происходит уничтожение не только обычной микрофлоры, но даже споросных культур сибирской язвы, столбняка и сенной палочки.
Техника заливки инструментария по способу Баккала такова: инструмент помещают в эмалированную ванночку на два поперечных ватных валика и заливают бриллиантовым зеленым на 15 мин, затем стерильным пинцетом инструменты переносят в другую стерильную ванночку с 96° этиловым спиртом, в который и переходит краска. Перед употреблением инструмент вытирают насухо с целью удаления с него окрашенного спирта. При этом режущие инструменты не портятся и не притупляются.
Стерилизация инструментов в растворе диоцида. Инструменты заливают раствором диоцида 1:1000 не менее чем на 5 мин. Обязательно добавляют антикоррозийный препарат НДА (нитрит-дициклогексиламмоний) в количестве 1 г на 1 л раствора диоцида (0,1% раствор). В случае необходимости инструменты хранят в этом растворе более длительно в закрытой посуде.
Метод сухой газовой стерилизации, принятый в Институте глазных болезней им. В. П. Филатова. Сущность метода заключается в стерилизации инструментов в парах параформа.
Параформ (СН2Оn)—белый порошок, насыпают его в коробку с дырочками. Эту коробку помещают в стерилизатор, который после загрузки инструментами закрывают наглухо крышкой на сутки. Метод в основном используется для стерилизации термолабильных инструментов, а также таких, которые нельзя заливать спиртом: кератопротезов, гониоскопов, тонких мелких игл и др.
Стерилизация стеклянной посуды (бутылки, пузырьки, пипетки и др.) может производиться в автоклавах, а также в электрическом шкафу при температуре 150°С в течение 2 ч. Для кипячения стеклянной посуды достаточно 5—10 мин.
↑ Приготовление и стерилизация материала для швов
Приготовление и стерилизация шелка. В офтальмологии используют шелк следующих размеров: № 000 — роговичный, 10 нулей для микрохирургических операций, № 1—2— конъюнктивальный, № 3 — эписклеральный.
Чем толще шелк, тем выше его номер. Существует много способов приготовления и стерилизации материала для швов.
Рассмотрим методику приготовления шелка, принятую в Институте глазных болезней им. В. П. Филатова.
Для стерилизации шелк наматывают на стеклянные катушки или предметные стекла без сильного натяжения, после чего опускают в 0,5% кипящий водный раствор бриллиантового зеленого и кипятят.
Время кипячения для шелка разных номеров разное. Шелк № 0 и 1 кипятят в течение 1 мин, № 2 — 2 мин, № 3 — 3 мин. После кипячения шелк вынимают стерильным корнцангом, укладывают в стерильную банку, заливают 96° спиртом. Через сутки он готов к употреблению, которое допускается после бактериологического контроля. Смену спирта производят 1 раз в 3 нед. По такой методике приготовляют также швы из нейлона. Время кипячения 1 мин.
Уздечные швы готовят из катушечных ниток № 30 и 20. Обрабатывают их так же, как и шелк. Однако кипятить их следует не более 3 мин, так как при более длительном кипячении нитка рвется.
Приготовление и стерилизация кетгут а. Аптечный кетгут сматывают кружочками, связывают толстой ниткой и опускают в стерильную банку, содержащую 1% водный раствор бриллиантового зеленого. Затем банку устанавливают в термостат на 2 сут при температуре 37°С. При этом кетгут разбухает, пропитывается бриллиантовым зеленым, проросшие споры погибают.
Через сутки водный раствор бриллиантового зеленого сливают и вместо него наливают 96° спирт, после чего банку вновь устанавливают на сутки в термостат. Через сутки спирт заменяют новым.
После бактериологического контроля кетгут готов к употреблению. На банке, в которой находится шовный материал, должна быть этикетка с указанием даты его приготовления.
Приготовление и стерилизация волоса. Наилучшим шовным материалом при пластических операциях является конский волос. Конский волос не оставляет следов на коже, не вызывает раздражения. Ткани, сшитые конским волосом, хорошо заживают.
Имеется несколько способов приготовления конского волоса. Приведем способ Асса.
Волос тщательно моют щеткой с зеленым мылом несколько раз в горячей воде, просушивают, промыва-ют для обезжиривания бензином, спиртом или эфиром, затем стерилизуют путем повторного кипячения в дистиллированной воде в течение 5 дней (первый день 40 мин, последующие 4 дня по 20 мин). От кипячения в других растворах, например в растворе сулемы или гидрокарбоната натрия, волос становится ломким.
После стерилизации волос хранят в сухом виде в стерильной банке. Перед операцией волос снова кипя-тят в течение 15—20 мин и до употребления сохраняют в горячей воде, вследствие чего он становится го-раздо мягче и не рвется. Высушенный волос более ломок и легче рвется при завязывании.
Приготовление и стерилизация лесы «Сатурн». Применяемая в ряде случаев в качестве шовного материала леса «Сатурн» представляет собой прозрачную гладкую нить из полиамидной смолы. Она значительно прочнее шелка, кетгута и волоса. Ее легко вдеть в автоматическое ушло иглы. Стерилизуют путем кипячения в растворе сулемы (1:1000) в течение 2 мин (В. М. Чередниченко). После кипячения хранят в том же растворе.
Приготовление швов из капрона. Капрон стирают в 7 водах с мылом, просушивают стерильным полотенцем, затем накатывают на катушки и опускают в 0,5% раствор нашатырного спирта на полчаса, затем перекладывают в стерильную банку, заливают 70° спиртом и 2% раствором формалина и так сохраняют.
При операции на роговице, особенно под операционным микроскопом, применяется супрамид 10:0, нейлон 8:0, виргинский шелк толщиной 10:0. Последний стерилизуют в 1% растворе бриллиантового зеленого в течение часа. Супрамид и нейлон кипятят в течение 20 мин.
Приготовление биологических швов. В последнее время разработан метод приготовления швов из сухожилий хвостов взрослой крысы.
Извлеченные из хвоста крысы сухожилия расчленяют на тонкие нити, которые стерилизуют. Швы из сухожилий являются хорошим шовным материалом, они тонки, эластичны, хорошо завязываются, не прорезают ткань. Разрывная прочность их составляет 0,5—1,5 кг, длина 8—15 см, диаметр 0,1—0,2 мм (Н. Б. Никулина). В настоящее время биологические швы изготовляют фабричным путем.
Приготовление растворов. Для операционной из аптеки выписывают стерильные капли. Многие лекарственные вещества для закапывания могут быть в операционной в запасе. К ним относятся такие, которые в аптеке после стерилизации закупоривают «под обкатку». Приводим список таких веществ и допустимые сроки их хранения: 1% раствор атропина — 1 год, дикаин (до 1% раствора)—8 мес, 1% раствор новокаина— 1 год, 1—2% раствор пилокарпина—1 год, 0,25% раствор скополамина—1 год, 3% раствор йодида калия — 6 мес, 0,25% раствор сульфата цинка — 4 мес.
Для закапывания применяют некоторые медикаменты в высокой дозировке, например 1% раствор атропина, что больше терапевтической дозировки в 10 раз, поэтому во избежание ошибки в Институте глазных болезней им. В. П. Филатова такие растворы окрашивают в постоянные для данного вещества цвета: дикаин — водным раствором бриллиантового зеленого из расчета 2 капли 1% раствора на 100 г дикаина, а 1% раствор атропина — в красный цвет фуксином: 4 капли 1% раствора фуксина на 100 мл атропина. Окраску капель производят в аптеке до их стерилизации. Флюоресцеин разливают в ампулы, которые стерилизуют в автоклаве. Чтобы ампулы не лопались, в них нужно оставлять мало воздуха.
Приводим рецепт и способ приготовления флюоресцеина.
Rp. Fluoresceini 0,1
Natrii carbonici 0,3
Aq. destill. 10,0
Способ приготовления. К 10 мл 3% горячего раствора бикарбоната натрия добавляют 0,1 г флюоресцеина, затем фильтруют. Перед операцией ампулу опускают в кипяток, обожженной пилкой надрезают шейку ампулы и содержимое ее набирают в шприц с длинной иглой. В случае необходимости путем поворота поршня из шприца закапывают в глаз 1—2 капли флюоресцеина.
Кроме обычных растворов (2% раствор новокаина, физиологического раствора и др.), заготовляют раствор Рингера — Локка и балансированный солевой раствор для промывания передней камеры глаза. Балансированный раствор по своему составу приближается к камерной влаге. Широко применяется в Институте глазных болезней им. В. П. Филатова и в других учреждениях.
Раствор Рингера-Локка
Rp.: Natrii chlorati 9,0
Natrii hydrocarbonatis
Calcii chloridi
Kalii chloridi ?? 0,2
Glucosae 1,0
Aq. destill. 1000,0
M. Sterilisetur!
Раствор BSS (балансированный солевой раствор)
Rp.: Natrii chlorati 2,45
Kalii chlorati 0,375
Calcii chlorati 0,24
Magnesii chlorati
Hexahydrati ?? 0,15
Natrii acetici 1,95
Natrii citrati dehydrati 0,85
Aq. destill. ad. 500,0
M. Sterilisetur!
↑ Обработка рук хирурга
Из многочисленных способов, предложенных для обработки рук хирурга, широко применяются модификации метода Фюрбрингера и Спасокукоцкого. Большинство офтальмохирургов пользуются методом обработки рук по С. И. Спасокукоцкому в модификации' И. Г. Кочергина. Он состоит в следующем. В проточной воде моют руки мылом и двумя щетками в течение 10 мин, затем текучей струей 1 °/о раствора аммиака из кружки, снабженной трубкой с зажимом. Подвешивают кружку выше головы. Раствор аммиака каждый раз готовят заново. После высушивания рук с помощью стерильной салфетки их обрабатывают 70° спиртом, а концы пальцев дополнительно йодной настойкой. На высохшие от спирта руки надевают стерильные перчатки, которые протирают спиртом.
Некоторые хирурги моют руки в тазу, который предварительно обжигают. Таз наполняют свежеприготовленным раствором аммиака (25 мг на 5 л воды). Руки моют в течение 3 мин 2 раза со сменой раствора.
В 1934 г. В. П. Филатов совместно с С. А. Баккалом предложил метод стерилизации рук хирурга, кото-рым пользуются многие окулисты.
Сначала приготовляют так называемый зеленый тальк, т. е. тальк, обработанный бриллиантовым зеле-ным. Для этого 100 г талька, просеянного через марлю, смешивают со 100 мл 0,5% раствора бриллианто-вого зеленого в 70° спирту до получения кашицеобразной массы, окрашенной в зеленый цвет. Указанную массу помещают в тигелек и ставят на небольшой огонь, все время помешивая шпателем. По мере испа-рения спирта зеленая кашицеобразная масса все более густеет и превращается в зеленый порошкообразный тальк. Порошок просеивают через сито и насыпают в банку. На приготовление зеленого талька уходит око-ло часа, так как испарение спирта должно происходить очень медленно. При этом важно не пережечь тальк, так как неправильно приготовленный тальк теряет свою бактерицидную силу. Обычно тальк имеет зеленый цвет. Если его пережечь, то тальк становится серым вследствие разложения бриллиантового зеленого. Зеленый тальк обладает высокими бактерицидными свойствами.
Обработка рук хирурга производится следующим способом. После мытья мылом и просушивания полотенцем руки смазывают жидкостью следующего состава:
Rp. Glycerini puri
Aq. destill.
Spiritus aethylici ?? 25,0
Далее руки посыпают зеленым тальком и надевают чистые, но нестерильные перчатки. Затем перчатки сверху тщательно смазывают 1% раствором бриллиантового зеленого, который убивает не только вегетативные формы микробов, но и споры. После того, как зелень на перчатках просохнет, на что уходит 1—2 мин, хирург надевает стерильный халат, перчатки натягивает на манжеты халата. После этого руки повторно обрабатывают 1% раствором бриллиантового зеленого, и хирург приступает к операции — руки его стерильны. Повторное смазывание бриллиантовым зеленым производят потому, что при надевании халата хирург сам заправляет манжеты под перчатки и может в это время нарушить их стерильность.
В промежутках между операциями перчатки отмывают от крови водой с мылом или в растворе сулемы, а затем снова протирают марлей, увлажненной 1% раствором бриллиантового зеленого. Этот способ стерилизации рук имеет большие преимущества, так как внутри перчаток находится стерильный тальк с бриллиантовым зеленым, обладающий бактерицидными свойствами, то по мере накопления «перчаточного сока» в нем растворяется анилиновая краска, которая и стерилизует «перчаточный сок». Поэтому даже при случайном повреждении перчатки можно не опасаться загрязнения раны микробами. Поскольку при этом способе перчатки предварительно не стерилизуют, они хорошо сохраняются. С кожи рук и инструментов бриллиантовый зеленый смывают тампоном, смоченным в 3% растворе перекиси водорода.
В последнее время в Институте глазных болезней им. В. П. Филатова был модифицирован этот способ следующим образом. Вместо зеленого талька руки обрабатывают церигелем. Церигель — бесцветная вязкая жидкость с запахом спирта. Он обладает значительной антибактериальной активностью, не раздражает кожу. На сухую кожу рук наносят 3—4 г церигеля и растирают так, чтобы препарат покрыл кожу рук и межпальцевые промежутки. Руки высушивают на воздухе в течение 2—3 мин, после чего они покрываются тонкой стерильной пленкой церигеля, которая стерилизует кожу рук. Далее надевают перчатки, которые обрабатывают бриллиантовым зеленым, как было описано выше.
Церигель применяют также и как самостоятельный метод подготовки рук хирурга перед операциями.
Уход за перчатками осуществляют следующим образом. После окончания операционного дня перчатки выворачивают наизнанку, моют с мылом с обеих сторон, просушивают и опускают в раствор «Баккалин 2» на 10 мин. Далее перчатки просушивают, выворачивают на лицевую сторону и смазывают 1% раствором бриллиантового зеленого. Состав «Баккалина 2» следующий:
Rp. Chinosoli 2,0
Brilliantgrimi 1% 3,0
Aetheri sulfurici 15,0
Spiritus aethylici 200,0
Aq. destill. 70,0
Во избежание окрашивания рук надо при повторных операциях перчатки всегда надевать с той же сто-роны. Перчатки перед подачей хирургу необходимо проверить. Чаще всего они повреждаются в пальцах от уколов иглами. В местах проколов получается интенсивная зеленая окраска. Чтобы проверить целость перчатки, ее берут двумя руками за манжет и перекручивают. При этом перчатка раздувается и обнару-живаются места нарушения ее целости. Это еще лучше заметно, если раздутую перчатку опустить в воду. Тогда из места прокола будут выходить пузырьки воздуха.
Отверстия в перчатке заклеивают резиновым клеем. Для заплаты используют старую непригодную пер-чатку. Заплаты приклеивают с изнанки.
При отсутствии резинового клея его можно приготовить путем растворения старых перчаток в небольшом количестве бензина. Растворение продолжается 10—12 дней. При производстве внутриглазных операций заклеенными перчатками пользоваться нежелательно. Индивидуальные перчатки должны быть у каждого хирурга. Их хранят в целлофановых пакетах. Для чистых и гнойных операций перчатки должны быть разные.
Обеззараживание рук диоцидом состоит из трех этапов.
Первый этап: руки моют стерильной салфеткой, обильно смоченной в растворе диоцида 1 :5000, нагре-том до температуры 40°С в течение 3 мин.
Второй этап: руки высушивают стерильным полотенцем.
Третий этап: в течение 2 мин руки обрабатывают салфеткой, обильно смоченной в 96° этиловом спирте.
Для обработки рук, загрязненных гноем, применяют раствор диоцида 1:2500.
Многочисленными исследованиями установлено, что асептичность рук, обработанных диоцидом, сохраняется не менее 2 ч.
Обработка рук ритосептом. Методика обработки рук такова. Вначале руки моют стерильными щетками с мылом в течение 2 мин. Затем их просушивают стерильным полотенцем, обрабатывают стерильной салфеткой, смоченной раствором ритосепта, 2 раза по 2 мин. Между операциями руки снова обрабатывают раствором ритосепта 1 раз в течение 3 мин. Ритосепт выпускают во флаконах емкостью 250 и 1000 мл.
Обработка рук дегмином. Дегмин обладает сильным бактерицидным действием в отношении грам-положительных и грамотрицательных бактерий. Применяется в виде 1% раствора на дистиллированной воде. Раствор можно хранить в течение года.
Методика обработки рук. Руки моют в теплой воде с мылом без щеток в течение 3 мин, затем протирают тампоном, смоченным в растворе дегмина (2 раза по 3 мин). Далее руки вытирают насухо стерильным полотенцем и надевают стерильные перчатки.
↑ Подготовка к операции и проведение операционного дня
В настоящем разделе мы не касаемся вопросов стерилизации материала, халатов, дезинфекции операционной и других сторон подготовки работы в операционной, что известно каждой операционной медицинской сестре. Рассмотрим лишь те особенности работы медицинской сестры, которые являются специальными для глазной операционной.
Накануне операционного дня медицинская сестра получает список операций, подписанный заведующим отделением. Соответственно списку заготовляет перевязочный материал, как это описано на стр. 175 и вы-писывает свежие растворы.
В некоторых операционных вместо новокаина проводниковую и инфильтрационную анестезию проводят 1% раствором тримекаина. Для анестезии перед внутриглазными операциями достаточно 2 мл. Тримекаин в 2 раза активнее новокаина, в связи с чем его анестезирующее действие держится дольше, чем при анестезии новокаином. Тримекаин не разлагается при стерилизации и хранении.
Инструментарий отбирают согласно списку, помещенному в конце данной главы. Со временем весь инструментарий, необходимый для той или иной операции, запоминают, однако для того, чтобы чего-нибудь не забыть, всегда полезно заглянуть в список.
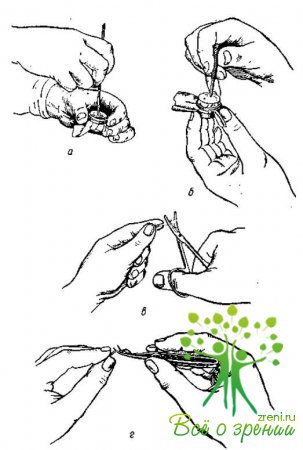
Если у медицинской сестры нет уверенности в остроте того или иного режущего инструмента, необходимо проверить его в этом отношении. Для испытания остроты инструмента существуют барабанчики с натянутой тонкой замшей или вощеной бумагой. Хорошо отточенный острый край ножа или трепан прорезает замшу без всякого сопротивления (рис. 37, а, б). Остроту ножниц проверяют обычным путем: ножницы должны разрезать ватные волоконца, а не тянуть их за собой (рис. 37, а, г). Тонкая, смоченная водой вощаная бумага должна резаться ровно так же проверяют остроту пинцет-ножниц Веккера (рис. 37,г). Лезвия режущих инструментов нужно осмотреть через лупу или через микроскоп.
При отборе инструментария следует учитывать не только инструменты, необходимые для проведения операции, но и инструменты, которые могут понадобиться для борьбы с возможными осложнениями, возникающими во время операции.
Необходимо подобрать тонкие иглы длиной 12— 15 мм для подконъюнктивальных инъекций, 20—25 мм для подкожных и 30—35 мм для ретробульбарных инъекций. Иглы длиннее 35 мм для рстробульбарных инъекций не должны применяться, так как длина передне-заднего размера орбиты взрослого человека 40 мм, а у людей с мелкой глазницей не превышает 35 мм.
Стерилизацию инструментария производят так, как было указано на с. 96. Соответственно заготовляют растворы, необходимые во время операции.
Нужно заготовить баночки с фиксирующими жидкостями (жидкость Ценкера), формалин для макроскопических препаратов, удаленного глаза, опухоли и др.
После того как медицинская сестра обработала руки, надела стерильный халат, косынку и маску, она приступает к приготовлению операционного стола в следующем порядке.
Сначала набирают в стерильные шприцы с тупой иглой окрашенный раствор дикаина и атропина, наливают новокаин и физиологический раствор, укладывают нережущий, а затем и режущий инструментарий. Перепутать дикаин или атропин с новокаином невозможно, так как растворы дикаина и атропина окрашены в разные цвета и шприцы, содержащие их, снабжены затупленными иглами.
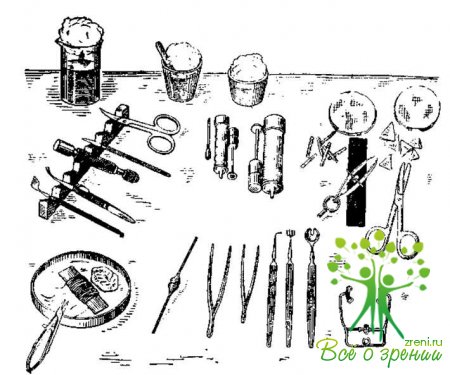
Медицинская сестра готовит два стола. На одном укладывает инструментарий, необходимый для не-скольких последующих операций, на другом — для данной операции. На столе должен быть порядок (рис. 38). Режущие инструменты укладывают на валик или на подставку с подразделениями для каждого из них. Чтобы не перепутать физиологический раствор с новокаином, в стаканчик с физиологическим раствором вставляют пипетку. Растворы следует покрывать салфеткой для предохранения от воздушной инфекции.
Все инструменты вытирают от спирта марлевой салфеткой. Заготовляют нитки на иглах. Чтобы нитка не выскользнула из ушка иглы и с целью придания ей большей гибкости, нитку нужно окунуть в воду — лучше в кипящую, чем достигается еще и дополнительная стерилизация материала для шва. Биологические швы и синтетические швы нельзя опускать в кипяток.
Как известно, инструменты подают хирургу так, чтобы к нему была обращена рукоятка инструмента, а не его острие. Например, ножницы подают вперед кольцами, скальпель — рукояткой и т. д. Во время операции медицинская сестра не только подает хирургу инструменты, но и принимает из его рук ненужные ему инструменты.
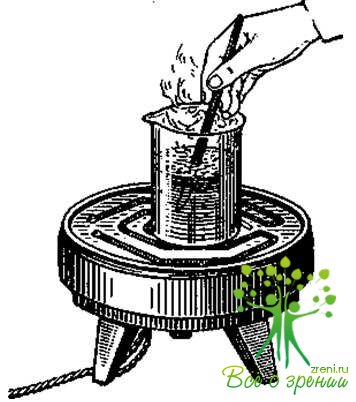
Перед подачей инструмента, который вводят внутрь глаза, она окунает последний в бурлящий кипяток (рис. 39). За короткий срок пребывания в кипятке инструмент не успевает притупиться. Операционная медицинская сестра должна следить за тем, чтобы ни один инструмент не был введен в полость глаза без предварительного опускания в кипящую воду.
Нельзя опускать в кипяток инструмент, не протертый от крови или кортикальных масс, так как в кипятке сворачивается белок и на ноже остается ржавый осадок. Вытирать режущий инструмент надо путем промакивания, чтобы не затупить марлей его режущий край.
Опускать нож в кипяток следует осторожно, чтобы не сломать его кончик, так как незамеченное своевременно медицинской сестрой или хирургом такое повреждение ножа может послужить причиной осложнений во время операции.
Операционный стол медицинской сестры должен быть хорошо освещен. Медицинская сестра, нуждающаяся в очках, должна работать в них, что позволяет ей свободно вдевать нитку в иглу и осуществлять постоянный контроль за инструментами, подаваемыми хирургу. Необходимо следить за тем, чтобы на концах инструмента, который вводят внутрь глаза, не было волокон ваты, волосков и др.
Подавая шприцы с новокаином при пластических операциях, экзентерации орбиты и др., нужно подсчитать количество новокаина.
После операции инструментарии отмывают от крови мыльной водой, особенно в замках, насухо вытирают марлевым тампоном и укладывают в инструментальный шкаф.
По окончании операционного дня медицинская сестра должна пополнить список инструментария для каждой операции теми инструментами, которые были затребованы хирургом, хотя по стандартному списку они не числятся. Удаленные глаза, опухоли в баночках с фиксирующей жидкостью передают в лабораторию.
Периодически 1—2 раза в месяц производят бактериологический контроль за работой операционной: берут посевы с перевязочного и шовного материала, смывы с рук хирурга и др.
↑ Уход за инструментарием
При уходе за режущим инструментарием от операционной медицинской сестры требуется большая тщательность и осторожность. Новые инструменты, полученные со склада, освобождают от бумаги, инструмент протирают бензином, ацетоном или эфиром для снятия масляного налета. При очистке игл их ушко надо протереть ниткой, смоченной в бензине.
Для того чтобы операции проходили без осложнений, инструментарий должен быть очень острым. Самые мелкие зазубрины на остром крае, видимые только в микроскоп (0,03—0,04 мм), делают инструментарий негодным к употреблению. За трепанами необходим особенно тщательный уход. После употребления трепан осторожно высушивают тонкой «сигаретой» и да него надевают защитный колпачок. При наличии в операционной нескольких комплектов трепанов для пересадки роговой оболочки их следует маркировать.
Операционная медицинская сестра должна знать, какое назначение имеет тот или другой режущий инструмент. Если нож используется не по прямому назначению, он должен быть выделен от остальных аналогичных ножей. Различные ножницы также должны иметь свое назначение. Нельзя остроконечные ножницы, предназначенные для расширения роговичной раны, для отрезания склерального диска и других моментов операции на глазном яблоке, использовать для снятия швов, конъюнктивальные ножницы — для разрезов кожи и т. д. Операционная медицинская сестра должна знать, какой нож и сколько раз был в употреблении.
К. Фельгаген в своем руководстве указывает, что нужно на рукоятке ножа помечать каждое его употребление. При тщательном уходе один нож, если он сделан из высококачественной стали, можно использовать до 10 раз. Хороший уход за режущим инструментарием дает возможность пользоваться им в течение многих лет.
По внешнему состоянию инструментария, его остроте, способу хранения можно судить о качестве работы операционной медицинской сестры.
↑ Хранение инструментария
Для глазных операций, как уже было указано, очень важно иметь безупречный инструментарий. Глазной инструментарий значительно нежнее хирургического и меньше его по размеру. Чтобы инструментарий не портился, его нужно правильно хранить. Хранить режущие инструменты нужно в сухом помещении, в стеклянных хирургических шкафах.
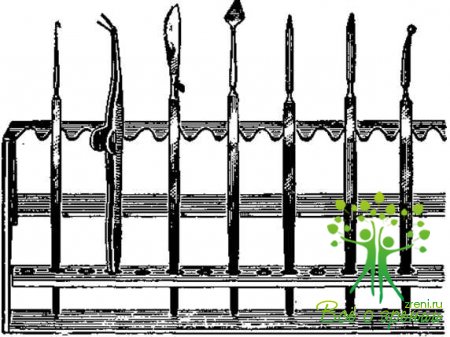
Режущий инструментарий укладывают на специальные металлические подставки, в отдельные гнезда острием кверху (рис. 40).
Укладывать инструментарий желательно таким образом, чтобы в одном ряду находились все ножи Грефе, далее — копьевидные ножи, затем — цистотомы и др. При наличии порядка в инструментальном шкафу легко в срочных случаях быстро найти нужный инструмент.
Режущий инструментарий, полученный из заточки и еще не бывший в употреблении, складывают в коробки со специальным местом для каждого инструмента. Внимательная медицинская сестра знает каждый инструмент, отмечает ножи, бывшие и не бывшие в употреблении, бывшие и не бывшие в заточке. Инструментарий, нуждающийся в заточке, складывают отдельно.
В инструментальном шкафу нельзя держать йод, кетгут, обработанный йодом, формалин, раствор хлор-амина, так как пары этих веществ вызывают окисление стальных инструментов.
↑ Подготовка к взятию глаз трупа и их хранение
В операционной всегда должен быть готов бикс с инструментами для энуклеации трупных глаз. В бикс, кроме инструментария для энуклеации (см. с. 136), вкладывают стерильные бюксы с притертыми пробками для энуклеированных глаз, стерильные просушенные перчатки, сухой шприц с длинной иглой (длина 12 см) для взятия крови из сердца (с целью производства реакции Вассермана), 1—2 сухие пробирки. Подчеркиваем, что шприц для взятия крови и пробирки должны быть сухими, так как при наличии влаги в пробирке возможен гемолиз крови, и тогда, не имея данных о реакции Вассермана, нельзя будет использовать глаз для пересадки роговицы.

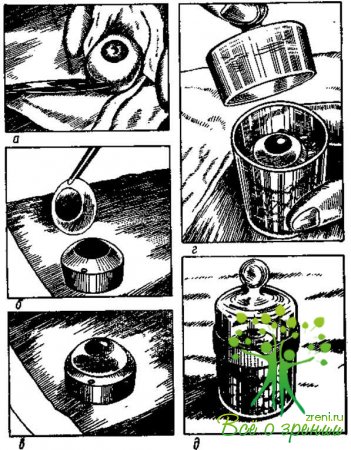
После того как в глазное отделение будут доставлены бюксы с глазами, их устанавливают в холодильник при температуре не выше +4°С для сохранения в течение не более 3 дней. Бюксы должны быть герметично закрыты. Глаз в бюксе должен лежать роговицей кверху (рис. 41). Перед началом пересадки роговицы бюксы с глазами приносят в операционную.
↑ Методы длительной консервации роговицы, склеры, слизистой оболочки, взятой с губы
Для сохранения роговицы на длительный срок пользуются ее высушиванием при помощи силикагеля. Метод этот был предложен французским ученым Payrau в 1959 г. Силикагель — вещество, жадно впитывающее влагу.
После обезвоживания роговица может сохраняться длительно и пригодна для пересадки в течение нескольких лет.
В нашей стране применяются различные модификации этого метода, имеющие целью сохранение формы и кривизны роговицы: модификация Г. П. Попова (1964) (Институт глазных болезней им. В. П. Филатова), Пермской (Н. Г. Гольдфельд), Куйбышевской (В. К. Степанов), Красноярской (Н. И. Васильев, В. И. Лазаренко) глазных клиник и др.
Модификация Пермской глазной клиники. Глазное яблоко погружают на 1—2 мин в раствор стрептомицина, содержащий 100 000 ед/мл. Далее выкраивают роговично-склеральный лоскут, который освобождается от сосудистого тракта (рис. 42, а, б, в, г, д). Лоскут помещают на алюминиевый блок, имеющий форму протеза Балтина с подставкой, и вкладывают в бюксу с силикагелем. Когда роговично-склеральный лоскут укладывают на поверхность протеза, саму роговицу вмещают в отверстие, имеющее диаметр роговицы, а склера лежит на кольце. Бюксу запечатывают парафином и хранят при комнатной температуре. Высушивание роговицы происходит со стороны эпителия и эндотелия.
При таком способе наилучшим образом сохраняется форма и кривизна роговицы.
Силикагель перед употреблением рассыпают в чашки Петри и прокаливают при температуре 120°С в течение часа для повышения его адсорбционной способности. В таком виде в бюксах роговица, окруженная силикагелем, сохраняется при комнатной температуре длительный срок — до 3 лет и более.
Вся работа по обезвоживанию донорских роговиц осуществляется одной из операционных медицинских сестер клиники. Осмотр глаза до засушивания роговицы производит врач. Данные о роговицах, подвергшихся обезвоживанию, заносят в специальный журнал, в котором записывают все сведения, касающиеся донора и состояния роговицы.
Методика эта очень проста. Она испытана в Пермской глазной клинике более чем на 1000 роговицах человека и животных. Роговица, обезвоженная силикагелем, пригодна только для послойной пересадки.
↑ Методика консервации склеры над силикагелем
После срезания роговицы удаляют все содержимое глаза, остается склера, которую разрезают на полоски, или целиком заворачивают в целлофан, помещают в бюксу над силикагелем и закупоривают. Так же можно заготовлять и широкую фасцию бедра. Склера, обезвоженная силикагелем, применяется для пломбирования при отслойке сетчатки. Она может сохраняться в течение 2—3 лет.
↑ Способ длительной консервации трупной слизистой оболочки, взятой с губы (Г. В. Легеза)
Наилучшим способом длительной консервации слизистой оболочки с губы является сохранение ее в жидкости Белякова 31-Е. Такие лоскуты слизистой оболочки сохраняют прозрачность, эластичность и пригодны для пластических операций в течение 4 лет.
↑ Техника извлечения стекловидного тела из трупных глаз
Вначале глаз дважды промывают в водном растворе бриллиантового зеленого 1 :2000, затем опускают в раствор антибиотиков. Далее его заворачивают в небольшую марлевую салфетку, не касаясь роговицы, и, умеренно сдавливая, берут в левую руку. Правой рукой после смазывания склеры 3% раствором йода производят прокол толстой иглой, насаженной на шприц, и отсасывают стекловидное тело. Несколько капель его высевают в пробирку с питательной средой для бактериологического контроля. Дальше стекловидное тело над пламенем горелки разливают в ампулы по 1 мл, последние запаивают.
Хотя объем глаза равен 6—7 мл, однако из одного трупного глаза можно взять не более 2,5 мл чистого стекловидного тела.
При использовании стекловидного тела должны быть учтены те же условия (реакция Вассермана, результат вскрытия), что и для пересадки роговицы.
Методика приготовления консервированной и автоклавированной плаценты для имплантации с лечебной целью по методу Филатова
Методика приготовления разных тканей для имплантации в деталях изложена в инструкции по тканевой терапии. Наиболее доступной тканью является плацента. Плаценту берут в родильных домах от здоровой роженицы в ближайший час после родов. Для этого медицинская сестра относит в родильное отделение стерильную банку и сдает ее дежурной акушерке. Полученную плаценту 4—5 раз ополаскивают дистиллированной водой, чтобы освободить ее от крови и слизи. Желательно затем один раз ополоснуть плаценту водным раствором бриллиантовым зеленым 1:300, после чего ее вкладывают в банку, соблюдая при этом правила асептики.
Банку с плацентой сохраняют в холодильнике при температуре +4°С в течение 6—8 дней. По истечении этого срока консервированную плаценту измельчают в асептических условиях стерильными ножницами на небольшие кусочки и помещают в стеклянные трубки длиной 15 см и диаметром 2 см. С нижнего конца трубку закрывают ватно-марлевым тампоном или пробкой от бутылочки с пенициллином, на которую надевают резиновый колпачок. Можно использовать имеющиеся в продаже резиновые соски. Затем трубку наполняют плацентой, причем верхний край ее остается на 2 см незаполненным. С верхнего конца трубку также закрывают ватно-марлевым тампоном и завязывают. Далее ее помещают в автоклав, где плаценту автоклавируют в течение часа при 1,5 атм и температуре 120°С. Срок годности автоклавированной плаценты одни сутки.
Имплантацию плаценты производят из металлического нагнетательного винтового шприца ФЗС (рис. 43), который заряжают следующим образом. На стерильном столе стеклянную трубку с плацентой освобождают от пробок и вставляют в цилиндр шприца. Стерильной стеклянной палочкой ткань выталкивают в шприц. В цилиндр шприца вводят поршень на стержне с винтовой нарезкой и завинчивают крышку шприца, также имеющую винтовую нарезку. Головку иглы ввинчивают в канюлю шприца.
При вращении ручки поршня по часовой стрелке тканевая масса в виде жгутика выходит из иглы. Это является показателем того, что шприц готов для производства имплантации.
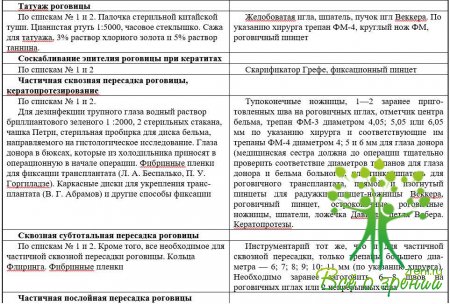
↑ Приготовление туши и других материалов для татуажа
Материалом для татуажа являются китайская тушь, сажа, полученная из копоти камфорного масла, хлорное золото и хлорная платина. Многие окулисты предпочитают пользоваться сажей по следующим соображениям: сажу для татуажа легко приготовить, крупинки ее под микроскопом малы и равномерны, после татуажа, сажей раздражение глаза незначительное.
Сажу для татуажа приготовляют следующим образом. Фитиль из ваты смачивают 20% раствором камфорного масла, зажигают и густо закапчивают тарелку. Образовавшуюся сажу счищают в тигелек, куда закапывают дистиллированную воду и глицерин из расчета 2—3 капли глицерина на 10 капель воды. Образовавшуюся массу растирают и укладывают в баночку или набирают в ампулы.
Тушь должна быть консистенции сметаны. Стерилизуют тушь в автоклаве при температуре 120°С в течение часа. При татуаже палочкой китайской туши последнюю также стерилизуют в автоклаве. Перед операцией ее разводят, растирая с раствором цианистой ртути 1:5000 на часовом стеклышке до консистенции сметаны.
При пользовании для татуажа хлорным золотом заготовляют 3% его раствор, а также 5% раствор тани-на, который применяется для восстановления хлорного золота.
Раствор танина должен быть приготовлен непосредственно перед операцией.
↑ Документация работы операционной
Ведение операционного журнала глазной операционной производится по таким же правилам, как и ведение общехирургического операционного журнала.
В журнале регистрации материала для тканевых имплантаций содержатся следующие сведения:
Дата взятия плаценты.
Фамилия роженицы и номер ее истории болезни.
Дата начала консервации плаценты.
Результаты реакции Вассермана.
В журнале учета трупных глаз для пересадки роговицы имеются следующие графы:
Фамилия умершего, пол, возраст, номер трупа.
Дата и час смерти.
Причина смерти.
Дата и час взятия материала.
Результаты реакции Вассермана.
Данные патологоанатомического исследования.
Кроме того, ведется и другая документация по учету сильнодействующих лекарств, результатов бакте-риологического контроля операционной, журнал для регистрации материала, направленного на гистологическое исследование, учета консервированного стекловидного тела и др.
↑ Перечень наиболее часто употребляемого глазного инструментария
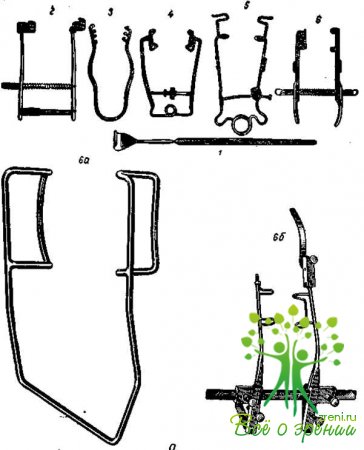
Нережущий инструментарий (рис. 44)
Векоподъемники, векорасширители, ранорасширители (рис. 44, а)
Векоподъемник Демарра (1).
Ранорасширитель Аксенфельда для слезного мешка (2).
Ранорасширитель Финзена (3).
Векорасширитель Аксенфельда (4).
Векорасширитель Грефе (5).
Векорасширитель пружинный (6).
Векорасширитель проволочный (6, а).
Блефаростат (6, б)1.
Имеет преимущество при полостных операциях, так как векорасширитель не давит на глаз.
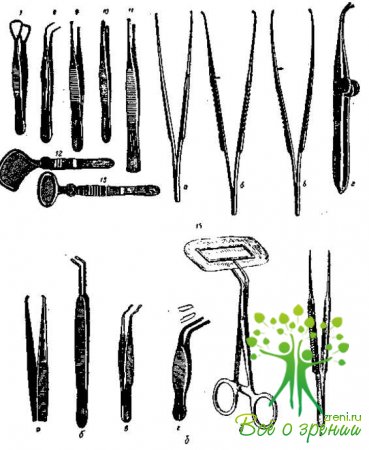
Пинцеты (рис. 44, б)
Пинцет Беллярминова (для выдавливания трахоматозных зерен) (7).
Пинцет для фиксации сухожилия мышцы (8). Пинцет Поляка (для наложения роговичных швов) (9).
Пинцет эпиляционный (10).
Пинцет фиксационный (11).
Пинцет Снеллена для операций на веках (12).
Пинцет-зажим для удаления халязиона (13).
Пинцеты прямой и изогнутые (14, а, б, в).
Пинцет Арруга (14, г).
Пинцет фиксационный Эльшнига (15, а).
Капсульный пинцет Швейгера (15,б).
Капсульный пинцет Эльшнига (15, в).
Капсульный пинцет Фукса (15, г).
Пинцет Израэльсона для взятия слизистой оболочки с губы (15, д).
Пинцет Пофика для наложения роговичных швов (15, е).
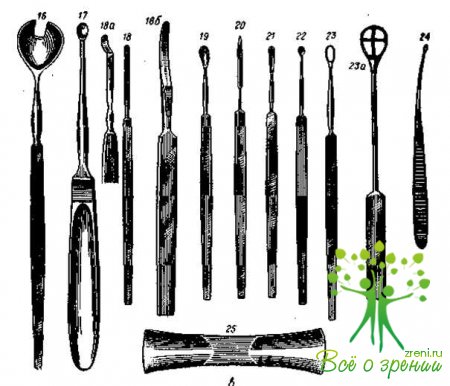
Ложечки, петли, Шпатели, пластинки (рис. 44, в)
Ложка Вельса для энуклеации (16).
Ложка для эвисцерации глаза (17).
Шпатель для циклодиализа (18, 18, а).
Шпатель для расслаивания обезвоженной роговицы (Н. Г. Гольдфельд) (18,б).
Ложечка овальная тупая (Давиэля) (19).
Шпатель для радужки (20).
Ложечка Давиэля для экстракции катаракты (21).
Ложечка для удаления халазиона (22).
Петля Вебера для экстракции катаракты (23).
Петля с сеткой для экстракции катаракты (23, а).
Ложечка острая для операции на слезном мешке (24).
Пластинка Егера (25).
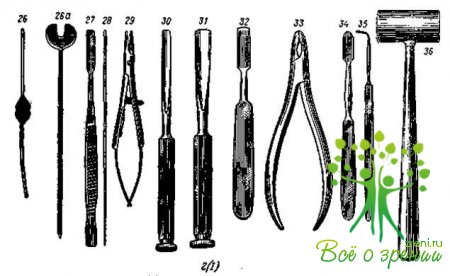
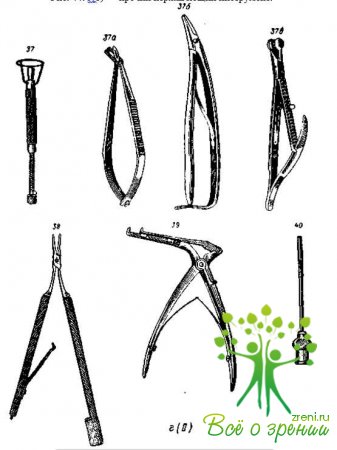
Прочий нережущий инструментарий (рис. 44, г)
Зонд Боумена (26).
Зонд желобоватый (26, а).
Долото прямое (27).
Зонд конический для слезных путей (28).
Иглодержатель. (29).
Долота желобоватые (30, 31).
Распаратор (32).
Кусачки костные (33).
Элеватор (34).
Крючок для косоглазия (35).
Молоток (36).
Отметчик для центра бельма (37).
Кусачки Тельнихина — Шнаудигеля (37, а).
Иглодержатели Занда и Матье (37, б, в).
Держатель для бритвенных лезвий (38).
Кусачки Цителли (39).
Игла-шпатель (40).
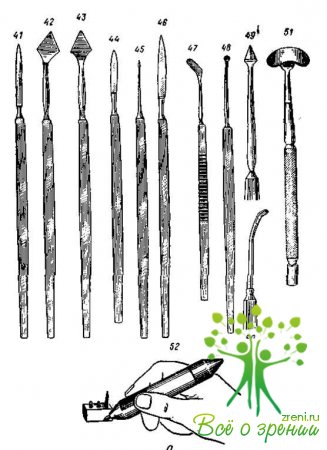
Режущий инструментарий (рис. 45)
Ножи (рис. 45, а)
Нож Грефе (41).
Нож копьевидный остроконечный (42).
Нож копьевидный тупоконечный (43).
Скальпель брюшистый (44).
Игла для удаления инородных тел (45).
Скальпель остроконечный (46).
Нож-скарификатор Грефе (47).
Нож круглый ФМ (48).
Нож-копье для парацентеза (49).
Синехиотом Аксенфельда (50).
Нож для срезания слизистой оболочки губы. Легеза (51).
Нож-магнит. Лебехова для удаления магнитных осколков из прозрачного хрусталика (52).
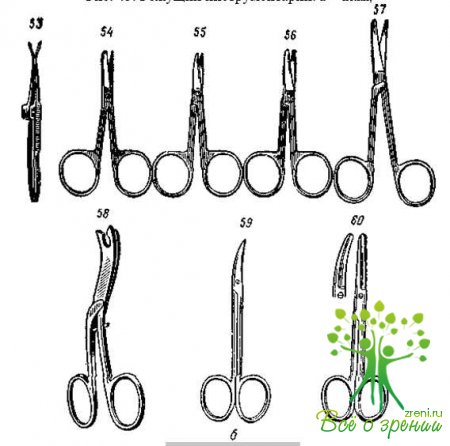
Ножницы (рис. 45, б)
Пинцет-ножницы Веккера для иридэктомии (53).
Ножницы роговичные с одной острой и одной затупленной браншей — 2 пары для разреза в правую и левую стороны (54) (Это необходимо во избежание ранения радужки или хруста лика во время разреза).
Ножницы остроконечные прямые (55).
Ножницы тупоконечные прямые (56).
Ножницы для энуклеации (57).
Ножницы Миминашвили для энуклеации (58)
Ножницы остроконечные изогнутые (59).
Ножницы для тенотомии Ландольта (60).
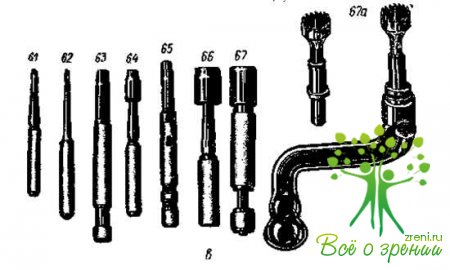
Трепаны (рис. 45, в)
Трепан для задней склерэктомии ФМ-3 (61).
Трепан для задней склерэктомии, входящий в набор для антиглаукоматозной операции (62).
Трепан ФМ-4 для трепанации роговицы донора (63).
Трепан ФМ-3 для трепанации бельма (64).
Трепан ФМ-5 для послойной пересадки роговицы (65).
Трепаны для субтотальной пересадки роговицы (66, 67).
Трепан-фреза Бакина для дакриоцисториностомии (67, а).
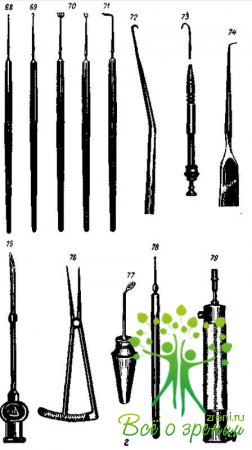
Прочий инструментарий (рис. 45, г)
Цистотом (68). Крючок для радужки (69).
Крючки острые (70).
Игла Ома (71).
Ретрактор для радужки (72) (Применяется при операции экстракции катаракты с круглым «рачком")
Гарпунный крючок для удаления катаракты, вывихнутой в стекловидное тело (Горячев) (73).
«Гарпун»— применяется при иссечении глубоких слоев роговицы во время операции послойной пересадки, иногда при выведении хрусталика из раны (74).
Игла Цур — Неддена для отсасывания стекловидного тела (75).
Циркуль с измерительной линейкой (76).
Эризофак (77). Гониотом Брошевского (78).
Электрофреза в собранном виде (79).
По предложению Л. А. Беспалько роговичную иглу готовят из круглой сосудистой иглы № 3, которую укорачивают до 5 мм. Эписклеральную иглу делают из режущей иглы № 3. При этом ее изгибают и укорачивают. Такая игла пригодна для операции дакриоцисториностомии, при отслойке сетчатки.
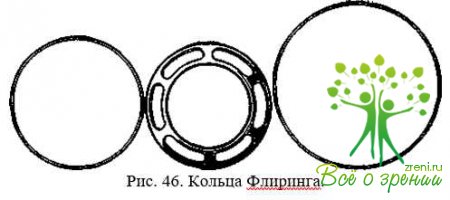
Кольца Флиринга должны быть разного диаметра — от 14 до 20 мм, толщина кольца 0,3 мм. Пришивают к эписклере перед операцией для профилактики выпадения стекловидного тела (рис. 46).
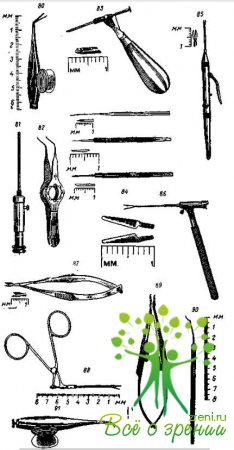
Микрохирургический инструментарий (для операций под операционным микроскопом) (рис. 47)
Пинцет шарнирный для удаления инородного тела из передней камеры (80).
Присасывающий пинцет для удаления мелких пла¬вающих немагнитных осколков из стекловидного тела (Лебехов, Зумбулидзе) (81).
Пинцет для радужки (82).
Секатор Цибиса для рассечения тяжей в стекловидном теле (83).
Ножи для операций на стекловидном теле (84): а) нож Якобсона, б) нож Гоаба, в) нож Гольдмана.
Ножницы для операций на стекловидном теле (85).
Ножницы Мак-Клина для иридокапсулэктомии (86).
Ножницы Ваннаса (87).
Ножницы для сфинктера зрачка (88).
Иглодержатель Костровьехо (89).
Расширитель шлеммова канала (90).
Пинцет-ножницы Веккера (91).
↑ Перечень инструментов, медикаментов и других предметов для наиболее часто производимых операций
↑ Все операции (список № 1)
Медикаменты: 1% спиртовой раствор бриллиантового зеленого для обработки операционного поля, 0,5% раствор дикаина, 1—2% раствор новокаина, 0,25% раствор новокаина для разведения пенициллина, физиологический раствор, 30% раствор альбуцида, раствор адреналина 1:1000 в ампулах, флуоресцеин в ампулах, альбуцид и белый стрептоцид в порошке. Заготовляют раствор Рингера—Локка и балансированный солевой раствор для промывания передней камеры глаза.
При операциях на слезном мешке, пластических операциях необходимо иметь средства для остановки кровотечения: тромбин в ампулах, гемостатическую губку, гемостатическую пасту или кровоостанавливающую марлю.
Гемостатическая губка применяется либо в виде кусочков, либо ее растирают в порошок. Ее наносят на кровоточащее место и прижимают к ране. Сохраняют в сухом затемненном месте при комнатной температуре.
Состав гемостатической пасты (приготовляется на желатиново-глицериновой основе):
Окись цинка 10 г
Хлорида кальция 5 г
Белого стрептоцида 5 г
Желатина 25 г
Глицерина 50 г
Дистиллированной воды 50 мл
Инструментарий. Анатомические, хирургические и кровоостанавливающие пинцеты, материальные ножницы, скальпели, иглодержатель, кожные и конъюнктивальные иглы, шприцы одно-, двух-, пяти- и десятиграммовые, а также иглы к ним разного размера. Зонды для остановки кровотечения, спиртовка.
Шовный материал. Все номера шелка, кетгута и др. должны быть заготовлены заранее и принесены в операционную в день операции, биологические швы, синтетические швы.
↑ Операции на глазном яблоке (список № 2)
Для операции на глазном яблоке требуется все, что указано в списке № 1. Кроме того, заготовляют 1% раствор атропина, 1% раствор пилокарпина, раствор фосфакола 1:5000. Раствор стрептомицина разводят непосредственно перед операцией 0,25% раствором новокаина. Под конъюнктиву вводят 100 000 единиц стрептомицина или в другом разведении. Трепан ФИ-3 2 мм для задней склерэктомии (на случай возникновения экспульсивного кровотечения), осколок лезвия, лезвиедержатель. Необходимы иглы для уздечных швов, роговичные иглы и иглодержатель, фиксационный пинцет, векорасширитель, векоподъемники Демарра, канюля для промывания передней камеры, глазные сетки, которые накладывают по окончании операции, микрохирургический инструментарий по указанию хирурга.
Далее будут указаны только те инструменты, медикаменты, перевязочный материал и другие предметы, которые требуются дополнительно для каждой из приведенных операций.
В СССР для протезирования применяются имплантаты из лавсана, полиэтилена, силиконового каучука, фторопласта-4, полиметилметакрилата. Силиконовый каучук, лавсан и фторопласт-4 выдерживают автоклавирование.
В последние годы во многих клиниках послойный трансплантат не пришивают швами, а укрепляют клеем, что укорачивает операцию и улучшает ее исходы. Наилучшим является клей, приготовленный из лиофилизированной плазмы.
Методика приготовления лиофилизированной плазмы. Для применения в клинике и экспериментальной работе лиофилизированная плазма из большой ампулы рассыпается в стерильные и тщательно просушенные пенициллиновые бутылочки в количестве 0,15—0,2 г на одно употребление. Бутылочки закупоривают пастой или парафином для предохранения от избыточной влажности, которая не должна превышать 0,5%. Плазма, пригодная для склеивания, Должна быть сыпучей и не прилипать к стенке бутылочки.
Клей приготовляют следующим образом. В ступку насыпают 0,15 г плазмы, добавляют 0,5 мл физиологического раствора, смесь растирают пестиком. Образуется нежная однородная масса, клейкость которой увеличивается после 15—20-минутного выжидания.
Клей имеет желтоватый цвет, что зависит от наличия в плазме пигментов — липохромов, особенно билирубина.
1 - Стеклянные крючки приготовляют путем изгиба стеклянной палочки для мази над пламенем горелки.
Способ применения ацетилхолина для введения в переднюю камеру глаза. Содержимое ампулы 0,2 г разводят в 20 мл физиологического раствора и тщательно перемешивают.
В переднюю камеру вводят 0,1 мл раствора при помощи тонкой тупоконечной иглы, надетой на шприц емкостью 1 мл.
Способ разведения хемотрипсина. 1 ампулу хемотрипсина (10 мг) разводят на 50 мг физиологического раствора. 0,1 мл раствора набирают в шприц емкостью 1 мл и на тонкой изогнутой тупоконечной игле вводят в заднюю камеру глаза на 2 мин, после чего с помощью такой же иглы промывают физиологическим раствором.
В некоторых клиниках небольшие, хорошо адаптированные раны роговицы не зашивают, а склеивают так называемым биологическим клеем, состоящим из компонентов крови человека: сухой, лиофилизированной Плазмы, фибриногена и тромбина.
При травмах с зиянием краев раны нередко сочетают биологические швы с приклеиванием. Последнее позволяет сократить число швов и избежать лишнего травмирования прозрачной ткани роговицы. Биологический клей очень хорошо переносится глазом, но является менее прочным, чем синтетический.
Из срочных операций в вечернее и ночное время чаще всего производят операцию первичной обработки раны и магнитную операцию удаления инородного тела. Для указанных операций должны быть отобраны самые высококачественные инструменты, которые выделяются из инструментария, применяемого для плановых операций.
Мы привели список необходимого инструментария для наиболее часто производимых операций. Указанный список не является исчерпывающим, а может быть рекомендован в качестве основного. Накануне операционная медицинская сестра согласовывает список инструментария с хирургом и по требованию последнего пополняет его.
Мы надеемся, что приведенные списки инструментария помогут медицинской сестре проконтролировать себя при подготовке к операции, особенно в начале ее работы в качестве операционной медицинской сестры глазного отделения.














Комментариев 0