Токсоплазмоз глаз (Часть 2)

Описание
Заболевание глаз клинически протекает как острое, подострое или хроническое воспаление (главным образом сетчатки и сосудистой оболочки) и характеризуется рецидивирующим течением. Рецидив приобретенного токсоплазмоза глаз, как и врожденного, обусловлен длительной персистенцией возбудителя в тканях глаза и периодическим освобождением токсоплазм из цист.
В тканях глаза при этом могут развиваться воспалительные процессы по типу реакции гиперчувствительности немедленного типа (клинически в форме остро протекающего воспаления) или, но типу реакции гиперчувствительности замедленного типа (в форме вяло текущего, хронического воспаления).
При приобретенном токсоплазмозе глаз наблюдается поражение всех оболочек глаза, зрительного нерва и наружных мышц глазного яблока. Однако, как и при врожденной токсоплазмозной инфекции глаз, чаще наблюдается заболевание увеального тракта и сетчатки.
Клинические и экспериментальные исследования свидетельствуют, что поражение конъюнктивы век и глазного яблока при токсоплазмозной инфекции наблюдается и при экзогенном заражении, и при эндогенном распространении инфекции. Клинически конъюнктивит может протекать как катаральный, фолликулярный или язвенный.
Конъюнктивиты при экспериментальном токсоплазмозе, по нашим наблюдениям, могут иметь специфическую природу, о чем свидетельствует выделение паразитов методом биопроб из отделяемого конъюнктивальных мешков. A. Ansari, A. Minou (1948) наблюдали ребенка, у которого на фоне высокой температуры развился фолликулярный конъюнктивит. В соскобах с конъюнктивы глаз были обнаружены токсоплазмы.
Изолированное поражение роговицы и склеры при токсоплазмозе глаз встречается редко. Как правило, клинически оно протекает в форме кератосклерита, кератоувеита, кератосклероувеита. Кератиты могут быть поверхностными и глубокими. Н. И. Шпак (1965) обнаружил токсоплазмы в роговице при экспериментальной токсоплазмозной инфекции.
Мы наблюдали 2больных с односторонним глубоким ареактивно протекавшим кератитом и значительным снижением остроты зрения больного глаза. Противотоксоплазмозное лечение привело к клиническому выздоровлению и полному восстановлению зрительных функций.
Поражение сосудистого тракта при токсонлазмозной инфекции глаз может наблюдаться в форме переднего, заднего и генерализованного увеита (панувеита). Передний увеит (ирит, иридоциклит) изолированно наблюдается редко. При этом обычно экссудативно-пластическое воспаление выражено умеренно, могут наблюдаться преципитаты на эндотелии роговицы (как мелкие, так и крупные овальной формы), узелки и новообразованные сосуды в радужке.
Течение болезни рецидивирующее. S. Duke-Elder (1953) наблюдал больную, у которой ранее на одном глазу диагностировался хориоретипит. Затем в этом же глазу развился узелковый ирит. Впоследствии слепой глаз был энуклеирован и при гистологическом исследовании в сетчатке обнаружены токсоплазмы.
Наиболее часто приобретенный токсонлазмоз глаз клинически проявляется задним увеитом, который может быть односторонним и двусторонним. По данным М. Saari (1975, 1976), задние увеиты токсоплазмозной этиологии составляют 23,4%, по материалам А. Ф. Калибердиной (1979) —39,1%всех увеитов. Н. И. Шпак (1978) установил токсоплазмозиую этиологию эндогенных увеитов в 18,6% случаев.
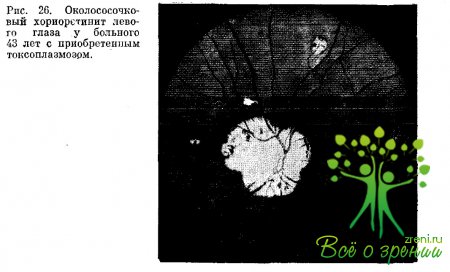
Задний увеит чаще протекает в форме очагового хориоретинита. В редких случаях задний увеит имеет распространенный характер (эндофтальмит). Локализация очагового хориоретинита бывает различной: чаще центральной, реже периферической и околососочковой (рис. 26). По наблюдениям Н. Werner (1976) и др., околососочковый хориоретинит в 90—95% случаев имеет токсоплазмозиую этиологию. Очаги хориоретинита чаще бывают одиночными, реже множественными.
Очаговое воспаление сосудистой оболочки и сетчатки может иметь острое, неострое и хроническое течение. При остро протекающем очаговом хориоретините воспалительный экссудативно- пролиферативный очаг серо-желтою или зеленовато-серого цвета, имеет нечеткие границы и доминирует в стекловидное тело.
Воспалительные очаги имеют округлую, овальную или неправильную форму, обычно их размеры равны 1—2 PD. Вследствие токсического поражения сосудов сетчатки и хориоидеи воспалительные хорио ретинальные очаги во многих случаях окружены интраретинальными, субретинальными и интрахориоидальными кровоизлияниями.
Как правило, в воспалительный процесс вовлекается стекловидное тело, и его помутнение более выражено в зоне, прилегающей к хориоретинальному очагу. Может возникнуть экссудативная отслойка сетчатки.
Для хориоретинитов токсоплазмозной этиологии типично длительное течение — от нескольких месяцев до года. Исходом острого, подострого и хронического очагового хориоретинита является образование рубцово-атрофического очага с отложением ретинального пигмента. В ряде случаев в зоне расположения очагов появляются новообразованные сосуды сетчатки или субретинальная неоваскулярная мембрана.
Могут развиться осложненная катаракта, вторичная глаукома, вторичная хориоретинальная дистрофия (обычно центральной локализации), кистозный отек желтого пятна (так называемая кистозная макулопатия), тракционная отслойка сетчатки. Эндофтальмит токсоплазмозной этиологии заканчивается организацией экссудата стекловидного тела и может привести к субатрофии глазного яблока.
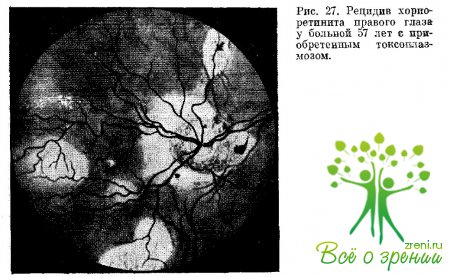
При рецидиве заднего увеита новый хориоретинальный очаг появляется обычно у границы со старым очагом (рис. 27) или вблизи него, иногда в другом, непораженном глазу. При наличии новообразованных сосудов сетчатки или субретинальной неоваскулярной мембраны могут наблюдаться рецидивирующие ретинальные кровоизлияния.
По данным ряда авторов, у больных задним увеитом методом микроскопирования удавалось обнаружить токсоплазмы во влаге передней камеры глаза, в субретинальной жидкости, сетчатой и сосудистой оболочках, а также методом биопроб на лабораторных животных выделить их из субретинальной жидкости, стекловидного тела, сетчатки и сосудистой оболочки.
Поражение глаз при приобретенном токсоплазмозе может наблюдаться также в форме геперализованного увеита с вовлечением в воспалительный процесс всего сосудистого тракта. При этом характерны острое начало заболевания, смешанная инъекция глазного яблока, крупные преципитаты на эндотелии роговицы, экссудат во влаге передней камеры, помутнение стекловидного тела, хориоретинальные очаги на глазном дне.
В ряде случаев наблюдается экссудативная отслойка сетчатки. Течение заболевания длительное и рецидивирующее. Исходом генерализованного увеита могут быть осложненная катаракта, вторичная глаукома, неоваскуляризация в зоне рубцующихся хориоретинальных очагов, вторичная хориоретинальная дистрофия, тракционная отслойка сетчатки. По наблюдениям ряда авторов при гистологическом исследовании энуклеировапных глаз в сетчатке больных панувеитом обнаруживаются токсоплазмы.
Некоторые исследователи наиболее типичным проявлением приобретенного токсоплазмоза глаз считают центральный экссудативный ретинит. У больных центральным экссудативным ретинитом были выделены токсоплазмы из цереброспинальной жидкости и из влаги передней камеры глаза.
При приобретенном токсоплазмозе глаз могут наблюдаться нейроретинит, неврит зрительного нерва с исходом в атрофию зрительного нерва. В случае приобретенной токсоплазмозной инфекции глаз могут отмечаться также поражение сосудов сетчатки: перифлебит, тромбоз центральной вены сетчатки и ее ветвей, ангииты, болезнь Ильса. У больных с приобретенным токсоплазмозом могут наблюдаться парезы и параличи глазных мышц. Многие авторы полагают, что токсоплазмоз служит одной из причин развития осложненной близорукости.
Таким образом, клинические проявления приобретенного токсоплазмоза глаз многообразны и не имеют строго специфических черт.
Диагностика токсоплазмоза глаз
Токсоплазмозную этиологию поражения глаз можно установить лишь на основании тщательного клинико-лабораторного обследования больных: с учетом анамнеза жизни и заболевания, эпидемиологического и акушерского анамнеза, изучения клинических проявлений поражения всего организма и органа зрения, результатов паразитологических и иммунологических методов исследования, дифференциального диагноза заболевания, эффективности химиотерапии.
Клиническая диагностика токсоплазмоза глаз
Трудность клинической диагностики заключается в том, что во многих случаях токсоплазмозная инфекция протекает латентно, при клинически выраженных формах симптомы заболевания многообразны и не имеют строго специфических черт. Следует также подчеркнуть, что для всех клинических проявлений этой инфекции характерно хроническое, рецидивирующее течение и одновременное поражение нескольких органов и тканей.
При сборе эпидемиологического анамнеза следует выяснить возможный источник инфекции и пути заражения токсоплазмами. При изучении акушерского анамнеза обращают внимание на течение и исход беременности, течение родов и послеродового периода.
У женщин с токсоплазмозной инфекцией могут наблюдаться различные виды акушерской патологии: патология беременности и ее исходов (токсикоз, угроза прерывания беременности, самопроизвольные выкидыши, преждевременные или запоздалые роды, мертворождения, фетопатии), патология родов и послеродового периода (раннее отхождение околоплодных вод, слабость родовых сил, кровотечение в послеродовом периоде).
Обследование больных с клиническими проявлениями токсоплазмозной инфекции должно включать рентгенологическое исследование черепа, органов грудной клетки и, по показаниям, мягких тканей нижних конечностей. У больных с токсоплазмозной инфекцией рентгенологически могут определяться изменение формы ц размера черепа и орбит (гидро- или микроцефалия, анизо- или микроорбита), внутримозговые кальцификаты, а также обызвествление швов черепа, оболочек мозга, сосудистых сплетений боковых желудочков мозга, легочной ткани, мягких тканей нижних конечностей.
Поражение органа зрения при врожденном токсоплазмозе отмечается главным образом при хроническом течении заболевания. В значительном числе случаев наблюдается сочетанное поражение органа зрения и головного мозга (микро- или гидроцефалия, внутримозговые кальцификаты, нарушение психики).
Наиболее характерное клиническое проявление заболевания глаз — двусторонний центральный очаговый хориоретинит в стадии Рубцовых изменений (по форме и строению напоминающий в одних случаях розетку, в других — псевдоколобому желтого пятна). Могут наблюдаться рецидивы очагового хориоретинита, которые, как правило, односторонние. Рецидивы хориоретинита чаще всего встречаются в возрасте 10—30лет (в 71 % случаев рецидивов хориоретинита).
При врожденном токсоплазмозе возможно также позднее (во втором и третьем десятилетии жизни) первое клиническое проявление заболевания глаз (наиболее часто также в форме очагового хориоретинита), которое почти всегда бывает односторонним. В более редких случаях отмечается распространенный воспалительный процесс в глазу (эндофтальмит, генерализованный увеит) с исходом в псевдомикрофтальм. Могут развиться атрофия зрительного нерва, нистагм, косоглазие. Описаны случаи наружного экссудативного ретинита Коатса токсоплазмозной этиологии.
Заболевание глаз при приобретенном токсоплазмозе наблюдается, как правило, па фоне хронического или латентного его течения. Изолированное заболевание глаз встречается редко. Типично сочетание поражения органа зрения и головного мозга (чаще всего), лимфатических узлов, миокарда, скелетных мышц.
Наиболее частым клиническим проявлением поражения глаз является очаговый хориоретинит, как правило, двусторонний, чаще центральной, иногда околососочковой локализации. Очаговый хориоретинит может протекать в острой и хронической форме и характеризуется рецидивирующим течением (рецидив заболевания бывает, как правило, односторонним). Вследствие токсического поражения сосудов тканей глаза воспалительные гранулемы сетчатки и сосудистой оболочки нередко сопровождаются интра- и субретинальными, интрахориондальными кровоизлияниями.
Воспалительный процесс в глазу может иметь распространенный характер (генерализованный увеит). В редких случаях наблюдаются конъюнктивит, кератит, склерит, центральный серозный ретинит, экссудативная отслойка сетчатки, неврит зрительного нерва, перифлебит и тромбоз сосудов сетчатки.
Лабораторные методы диагностики токсоплазмоза
Для установления токсоплазмозной этиологии заболевания глаз офтальмологи, как и врачи других специальностей, широко используют лабораторные методы диагностики: паразитологические и иммунологические.
Паразитологические методы диагностики токсоплазмоза. Для обнаружения и выделения возбудителя применяют метод прямой микроскопии и метод биопроб.
Микроскопируют нативные препараты и препараты, окрашенные по Романовскому—Гимзе: мазки и отпечатки различных жидкостей, органов и тканей. Однако положительные результаты при этом получают редко. Можно исследовать гистологические срезы секционного или операционного материала. Окрашивание препаратов производят гематоксилин-эозином.
Для выделения токсоплазм прибегают к методу биопроб, заражая исследуемым материалом лабораторных животных (чаще всего белых мышей), иногда куриные эмбрионы или культуры клеток. При постановке биопроб с материалом, полученным прижизненно или посмертно, выделить токсоплазмы чаще удается при проведении нескольких пассажей на лабораторных животных. При этом в экссудате брюшной полости белых мышей обнаруживаются эндозоиты токсоплазм, имеющие типичную морфологию в виде полумесяца.
Материалом для исследований могут служить цереброспинальная жидкость, кровь, слюна, грудное молоко, менструальная кровь, выделения из влагалища, плацента, околоплодная жидкость, лохии, головной мозг и внутренние органы погибших эмбрионов и плодов, пунктам лимфатических узлов и костного мозга, материал биопсии (лимфатические узлы, скелетные мышцы), операции (миндалины, лппеидикс и др.) и секции. От трупов берут кусочки различных органов и тканей: головного мозга, миокарда, миометрия, скелетных мышц, печени, селезенки, легких и др.
Материалом для проведения паразитологических исследований при поражении глаз могут служить влага передней камеры глаза, субретинальный экссудат, отделяемое конъюнктивального мешка, гистологические срезы оболочек энуклеированного глаза и взвесь из тканей глазного яблока.
В гистологических препаратах энуклеированного глаза форма обнаруженных токсоплазм может быть различной, что зависит от плоскости среза исследуемых тканей и стадии жизненного цикла паразита. Эндозоиты токсоплазм могут иметь округлую, овальную или полулунную форму. В гистологических препаратах возбудитель имеет меньшие размеры, чем в мазках и отпечатках исследуемых органов и тканей.
Эндозоиты, расположенные внеклеточно, необходимо дифференцировать от других микроорганизмов и разрушенных ядер клеток изучаемых тканей. Цисты имеют округлую, овальную, иногда неправильную форму. Многие исследователи полагают, что при гистологическом исследовании лишь обнаружение токсоплазм в инцистированной форме является убедительным критерием их идентификации.
Таким образом, паразитологический метод диагностики токсоплазмоза является наиболее достоверным, но и весьма сложным. Изучение гистологических препаратов проводится в клинических учреждениях. Постановка же биопроб на экспериментальных животных, куриных эмбрионах и в культурах клеток может быть осуществлена только в условиях паразитологической лаборатории.
Идентификация токсоплазм требует четкой микроскопической дифференциации от некоторых простейших и грибков, сходных по морфологии. В клинических условиях офтальмологи применяют преимущественно иммунологические методы диагностики TOKCO- плазмоза.
Иммунологические методы диагностики токсоплазмоза.
Целью иммунологических исследований при токсоплазмозе является изучение реакций гуморального и клеточного иммунитета у обследуемых больных. Для определения в сыворотке крови больных специфических антител к токсоплазменному антигену используют ряд серологических реакций: реакцию с красителем Сейбина—Фельдмана, реакцию лизиса, реакцию связывания комплемента, реакцию непрямой гемагглютинации, реакцию непрямой иммунофлгооресненции, тест Ремингтона, реакцию агглютинации, реакцию агглютинации с латексом, реакцию микропрецинитации в агаре, непрямую иммунопероксидазную пробу, реакцию энзиммеченных антител и др.
Реакция с красителем Сейбина—Фельдмана (Р С Ф)
предложена для диагностики токсоплазмоза в 1948 г. А. Sabin и Н. Feldman. В настоящее время чаще применяют микрометод постановки РСФ, предложенный Н. Feldman и J. Lambis 1966 г. В качестве антигена в реакции используется взвесь живых токсоплазм.
Сущность РСФ заключается в том, что живые токсоплазмы под воздействием иммунной сыворотки утрачивают присущую им способность прижизненно окрашиваться метиленовым синим. Учет реакции производят в световом микроскопе (объектив 40). Реакцию считают положительной, если более 50% токсоплазм остаются неокрашенными.
Результаты всех серологических реакций, в том числе и РСФ, необходимо оценивать также по титру специфических антител в исследуемых сыворотках. Титром сыворотки называется то максимальное ее разведение, при котором реакция считается еще положительной. В настоящее время считают, что наиболее точно оценить серологические реакции можно по концентрации в сыворотке специфических иммуноглобулинов. Полученные цифры следует выражать в международных единицах (ME).
Антитела, выявляемые с помощью РСФ, появляются в конце 1-й недели после заражения токсоплазмами. Затем в течение нескольких недель титр антител нарастает и, достигнув максимальных величин, сохраняется на одном уровне в течение нескольких месяцев. В дальнейшем титры специфических антител постепеннее снижаются и остаются на низком уровне в течение многих лег„ иногда пожизненно.
РСФ специфична и считается самым чувствительным методою серологической диагностики токсоплазмоза, выявляющим специфические антитела в исследуемых сыворотках крови.
В 1955 г. G. Desmonts предложил модификацию классической методики РСФ — реакцию лизиса, сущность которой заключается в том, что под воздействием иммунной сыворотки живые токсоплазмы частично лизируются и изменяют свою морфологию» Учет реакции лизиса производят в световом микроскопе с фазово- контрастным устройством (объектив 40).
Постановка РСФ и ее варианта в модификации Десмона сложна и трудоемка, так как в реакции используются в качестве антигена живые паразиты и требуется присутствие активатора (неспецифического термолабильного фактора), содержащегося лишь в 5—10% нормальных сывороток крови человека. В связи с технической сложностью постановки РСФ и реакции лизиса и некоторым риском заражения персонала при их постановке эти реакции не столь широко, используются в клинической практике для диагностики токсоплазмоза.
Реакция связывания комплемента (PCК)
для диагностики токсоплазмоза предложена S. Nicolau и A. Rovello (1937), усовершенствована J. Warren и А. Sabin (1942). Для постановки реакции применяют растворимый антиген, приготовленный из перитонеалъного экссудата белых мышей.
Сущность РСК заключается в выявлении специфических антител в исследуемой сыворотке с помощью токсоплазменного антигена, комплемента и гемолитической системы. При наличии в исследуемой сыворотке специфических противотоксоплазменных антител образуется комплекс антиген—антитело, который связывает используемый в реакции дополнительный фактор — комплемент, получаемый из свежей сыворотки крови морских свинок. Образование в реакции трехкомпонентной системы (антиген—антитело— комплемент) внешне не проявляется. В реакцию с целью ее индикации вводят гемолитическую систему, состоящую из эритроцитов барана и гемолитической сыворотки кроликов, иммунизированных эритроцитами барана. Реакция гемолиза эритроцитов может произойти только в присутствии свободного комплемента. Следовательно, при задержке гемолиза эритроцитов результат реакции определяется как положительный, при полном гемолизе эритроцитов — как отрицательный.
Учет реакции производят визуально и в зависимости от степени задержки гемолиза эритроцитов результат ее обозначают 4+, 3 + , 2+ и 1 + . Реакция считается положительно при задержке гемолиза не менее чем на 2+ в титре 1:5. Для количественной оценки положительных сывороток определяют титр специфических антител.
Антитела, определяемые в РСК, появляются через 10—12 дней после заражения токсоплазмами и сохраняются в течение 2—4лет, иногда дольше. РСК специфична, однако она менее чувствительна, чем РСФ и реакция непрямой иммунофлюоресценции (РНИФ). Антитела, определяемые в РСК, появляются позже и исчезают раньше, чем антитела, выявляемые в РСФ и РНИФ, и уступают последним в титрах.
РСК с токсоплазменным антигеном наиболее широко используется в нашей стране для серологической диагностики токсоплазмоза, в том числе и для диагностики токсоплазмозной инфекции глаз. Для постановки реакции выпускается отечественный коммерческий антиген.
Для диагностики токсоплазмоза, кроме общепринятой методики РСК, применяют микрометод, предложенный F. Fulton и К. Dumbell (1949), в модификации J. Pokorny и соавт. (1972). По наблюдениям JI. И. Грачевой (1980), капельный метод РСК обладает высокой чувствительностью, позволяет экономить антиген и время и может быть рекомендован для широкого использования в эксперименте и в клинике.
Реакция непрямой иммунофлюоресценции (РНИФ)
для диагностики токсоплазмоза предложена J. Kramar (1961). В качестве антигена в реакции используют убитые эндозоиты токсоплазм.
Сущность РНИФ состоит в выявлении специфических антител в исследуемой сыворотке с помощью токсоплазменного антигена и маркированных флтооресцоином антител к иммуноглобулинам человека. При наличии в испытуемой сыворотке специфических противотоксоплазменных антител образуется комплекс антиген— антитело, который адсорбирует меченные флюоресцеином антитела к гамма-глобулинам человека.
Образование в реакции трехкомпонентной системы сопровождается появлением по периферии токсоплазм яркого зелено-желтого свечения, хорошо контрастирующего» с телом возбудителя. Такой результат реакции определяется как положительный. При полном отсутствии флюоресценции токсоплазм результат реакции расценивается как отрицательный.
Учет реакции производят под иммерсионной системой (объектив 90) в люминесцентном микроскопе. В зависимости от интенсивности свечения токсоплазм результат реакции обозначают 4+, 3 + , 2+ и 1 + . Положительной считают реакцию при интенсивности свечения токсоплазм на 4+ и 3+. Для количественной оценки положительных сывороток определяют титр специфических антител.
Антитела, определяемые в РНИФ, появляются к концу 1-й недели после заражения токсоплазмами и сохраняются длительное время. РНИФ специфична и по чувствительности приближается к РСФ. По уровню титров она уступает РСФ лишь на 1—2 порядка и значительно превосходит РСК. Однако необходимо учитывать, что у больных системной красной волчанкой, ревматоидным артритом и другими заболеваниями, при которых наблюдается образование антиядерных антител, РНИФ с токсоплазменным антигеном может давать ложноположительные результаты, так как антинуклеарные антитела могут фиксироваться на токсоплазмах.
РНИФ с токсоплазменным антигеном является одним из основных методов серологической диагностики токсоплазмоза в нашей стране. В настоящее время выпускаются отечественные стандартные унифицированные компоненты, необходимые для постановки РНИФ.
J. Remington (1968) разработал тест, позволяющий в РНИФ выявлять антитела класса IgM. Для их обнаружения используют токсоплазменный антиген (формалинизированные токсоплазмы) и маркированную флюоресцеином антисыворотку, содержащую антитела к IgM человека.
Реакция непрямой гемагглютинации (РНГА)
для диагностики токсоплазмоза предложена L. Jacobs и М. Lunde (1957). Для постановки реакции используют растворимый антиген, фиксированный на эритроцитах барана.
Сущность РНГА заключается в выявлении специфических антител в исследуемой сыворотке с помощью токсоплазменного антигена, сорбированного на эритроцитах барана. При наличии в исследуемой сыворотке специфических противотоксоплазменных антител происходит взаимодействие между токсоплазменным антигеном и специфическими к нему антителами и наступает агглютинация эритроцитов.
Такой результат реакции определяется как положительный. При полном отсутствии агглютинации эритроцитов реакция расценивается как отрицательная.
Результат реакции учитывают визуально и в зависимости от степени агглютинации эритроцитов обозначают 4 + , 3 + , 2+ и 1 + . Положительной считают реакцию на 2-К. Для количественной оценки положительных сывороток определяют титры специфических антител.
Антитела, определяемые в РИГА, обнаруживаются несколько позже, чем антитела, определяемые в РСФ (на 11—18-й день после заражения токсоплазмами). Их титр постепенно нарастает, некоторое время остается на одном уровне, а затем снижается. Низкие титры специфических противотоксоплазменных антител могут сохраняться несколько лет. РНГА специфична и не уступает по чувствительности РНИФ. Титры сывороток в РНГА значительно выше, чем в РСК, и в среднем на 2—3 разведения выше, чем в РНИФ.
Техника постановки реакции и учет ее результатов просты. Основным затруднением для широкого использования РНГА является отсутствие стандартного токсоплазменного эритроцитарного диагностикума (ТЭД). В настоящее время проведена лабораторная апробация отечественного ТЭД, в котором использованы формалипизированные таннизированные эритроциты барана, сенсибилизированные токсоплазменным антигено.
Все описанные выше методы серологической диагностики токсоплазмоза являются общепринятыми и широко используются в клинике и эксперименте. Продолжается разработка и апробация новых серологических тестов для иммунодиагностики токсоплазмозной инфекции.
При этом большое внимание уделяется изучению иммуноферментных серологических методов исследования, которые являются наиболее перспективными для выявления специфических противотоксоплазменных антител. В последние годы испытаны следующие серологические тесты: реакция агглютинации, реакция агглютинации с латексом, реакция микропреципитации в агаре, непрямая иммунопероксидазная проба, реакция энзиммеченных антител.
Реакция агглютинации (РА)
для диагностики токсоплазмоза предложена J. Fulton и J. Turk (1959). В качестве антигена в реакции используют убитые эндозоиты токсоплазм. Техника постановки реакции несложна, однако в связи с трудностью получения чистого антигена (токсоплазм, освобожденных от балластных клеток) РА ь настоящее время еще не получила широкого применения.
Реакция агглютинации с латексом (РАЛ)
для диагностики токсоплазмоза разработана J. Siim и К. Lind (1960). В реакции используют растворимый антиген, сорбированный на частицах латекса. Метод в нашей стране не апробирован.
Реакция микропреципитации в агаре (МПА)
для диагностики токсоплазмоза глаз впервые предложена G. O'Connor (1957), разработана и рекомендована для широкого применения J. H?bner и М. Uhlikowa (1969). В реакции используют растворимый антиген. Реакция МПА позволяет выявлять антитела главным образом в острой фазе токсоплазмозной инфекции. В нашей стране реакцию МПА с токсоплазменным антигеном апробировала Л. И. Грачева (1980).
Непрямая иммунопероксидазная проба
для диагностики токсоплазмоза предложена D. Ourth и соавт. (1974) и разработана Dugimant и соавт. (1975), J. Kramar (1977) и др. В реакции используют отечественный сухой антиген, выпускаемый для постановки РНИФ (формалинизированные эндозоиты токсоплазм).
Сущность НИПП состоит в выявлении специфических антител в исследуемой сыворотке с помощью токсоплазменного антигена, маркированных пероксидазой хрена антител к иммуноглобулинам человека и субстратной смеси на пероксидазу. При наличии в испытуемой сыворотке специфических противотоксоплазменных антител образуется комплекс антиген—антитело, который присоединяет к себе коньюгат-меченные пероксидазой антитела к гамма-глобулинам человека.
Образование в реакции четырехкомпонентной системы не имеет внешнего проявления. В реакцию с целью ее индикации БВОДЯТ субстратную смесь, состоящую из раствора перекиси водорода и 3,3-диаминобензидина тетрагидрохлорида. Пероксидаза, взаимодействуя с перекисью водорода, освобождает из нее активный кислород, который окисляет диаминобензидин, в результате чего образуется соединение коричневого цвета, окрашивающее токсоплазмы.
Таким образом, при положительном результате реакции токсоплазмы окрашиваются в коричневый цвет, при отрицательном остаются серыми или серо-белыми. Учитывают реакцию в световом микроскопе.
НИПП с токсоплазменным антигеном специфична, высокочувствительна и позволяет определять классы специфических иммуноглобулинов (G и М). Как показали наблюдения JI. И. Грачевой и соавт. (1979), А. Я. Лысенко и соавт. (1980), Б. В. Мороза и соав г. (1980), В. И. Боришполец и Б. В. Мороза (1983), по чувствительности НИПП не уступает РНИФ.
Техника постановки НИПП несложна и не требует дорогостоящего оборудования. Этот иммуноферментный тест серологической диагностики токсоплазмоза весьма перспективный.
Реакция энзиммеченных антител (РЭМА)
или enzyme-linked immunosorbent assay (ELISA), для диагностики токсоплазмоза предложена A. Voller (1976). В реакции используют растворимый антиген, фиксированный на полистироле.
Сущность этой реакции заключается в выявлении специфических антител с помощью токсоплазменного антигена, сорбированного на полистироле, маркированных пероксидазой хрена антител к иммуноглобулинам человека и субстратной смеси па пероксидазу.
При добавлении к четырёхкомпонентной системе субстратной смеси (раствор перекиси водорода и 5-аминосалициловая кислота) образуется соединение коричневого цвета. Таким образом, при положительном результате реакции субстратная смесь окрашивается в коричневый цвет, при отрицательном — сохраняет светло-желтую окраску.
Качественную оценку реакции производят визуально, количественную — с помощью специального спектрофотометра, измеряя оптическую плотность окрашенной субстратной смеси.
Реакция энзиммеченных антител с токсоплазменным антигеном — специфичный, высокочувствительный серологический тест, позволяющий определять не только суммарные специфические иммуноглобулины, но и их классы (О и М). По предварительным наблюдениям Б. В. Мороза и А. М. Пономаревой (1981), по чувствительности эта реакция с токсоплазменным антигеном практически не отличается от РНИФ.
Это один из наиболее перспективных вариантов иммуноферментных методов серологической диагностики токсоплазмоза. Для широкого использования иммуноферментных методов в лабораторной диагностике токсоплазмоза требуется производственное получение необходимых для их постановки ингредиентов.
Дальнейшее изучение и внедрение в практику иммуноферментных методов диагностики токсоплазмоза согласуется с приказами Министерства здравоохранения СССР о разработке методов медицинского микроанализа (иммуноферментные, радиоиммунологические, фотометрические и экспресс-тесты на твердофазных носителях реактивов) для диагностики и индикации вирусных, бактериальных и паразитарных инфекций, в том числе токсоплазмозной, а также для эпидемиологического обследования и обоснования назначения иммуномодулирующей терапии.
Многочисленные экспериментальные и клинические исследования свидетельствуют, что все перечисленные серологические реакции, применяемые для диагностики токсоплазмоза, специфичны и высокочувствительны. Однако их положительные результаты требуют правильной интерпретации.
Как отмечалось выше, поражение глаз наблюдается, как правило, при хроническом токсоплазмозе. В связи с этим специфические антитела в сыворотке крови больных с токсоплазмозом глаз определяются чаще в низких титрах. При этом специфические антитела во влаге передней камеры больного глаза имеют более высокие титры, значительно превышающие титры антител в сыворотке крови.
Определение специфических антител во влаге передней камеры пораженного глаза не нашло широкого применения в клинической практике, так как это исследование сопряжено с техническими трудностями и риском ухудшения воспалительного процесса в глазу. Следовательно, офтальмолог, как правило, располагает сведениями о содержании специфических антител только в сыворотке крови обследуемого.
В методических рекомендациях «Клиника, диагностика и лечение токсоплазмоза» (1981) предлагаются следующие градации оценки титров специфических антител: высокие, средние и низкие. Высокие титры антител: для РНИФ 1: 640 и выше; для РСК 1: 160 и выше. Средние титры: для РНИФ 1:80 — 1: 320; для РСК 1: 20—1: 80. Низкие титры: для РНИФ 1:10—1: 40; для РСК 1:5 — 1:10.
Для правильной интерпретации результатов иммунологических обследований на токсоплазмоз следует учитывать все уровни специфических антител. Нельзя ограничиваться однократным исследованием сыворотки крови. Серологическое обследование больных необходимо производить 3 раза и более с интервалом в 3—4нед.
В период обострения инфекционного процесса может наблюдаться повышение титров антител. При бессимптомном токсоплазмозе в начальной фазе инвазии и в фазе генерализации титры антител имеют тенденцию к нарастанию и могут достигать среднего уровня. В фазе персистенции возбудителя (в форме тканевых цист) титры антител низкие, что, по всей вероятности, можно объяснить слабой антигенностью цист. При носительстве титры специфических антител постоянно низкие.
Анализ серологических исследований в эксперименте и клинике показал, что результаты различных серологических реакций могут не совпадать, что объясняется образованием антител различного типа (время появления и длительность циркуляции в крови которых неодинаковы).
С целью выявления антител различных типов исследование сывороток крови больных целесообразно проводить одновременно в двух и более серологических реакциях, при постановке которых используют разные антигены (цельные токсоплазмы и растворимые антигены).
Такая методика иммунологического обследования больных помогает определить период инфекционного процесса у них (начало, развитие и пик заболевания, угасание инфекции). Повторное серологическое исследование, если позволяют условия, рекомендуется проводить в тех же лабораториях с применением одних и тех же реакций.
При серологической диагностике токсоплазмоза в настоящее время рекомендуют выявлять в сыворотке крови больных не только общий уровень специфических антител, по и их классы. Основную часть сывороточных антител (70—80%) составляют иммуноглобулины класса О, наличие которых свидетельствует о длительно протекающей инфекции.
Крупномолекулярные иммуноглобулины (М) связаны с ранними стадиями развития гуморального иммунитета и обнаруживаются главным образом в остром периоде инфекции. Установлено также, что М не проходят через плацентарный барьер, и их обнаружение в сыворотке крови новорожденного свидетельствует о его внутриутробном заражении токсоплазмами.
Таким образом, изучение соотношения классов О и способствует диагностике врожденного токсоплазмоза и определению стадии инфекционного процесса при врожденном и приобретенном токсоплазмозе.
Как показали наши клинические наблюдения, при одновременном исследовании в РСК с токсоплазменным антигеном сыворотки крови и цереброспинальной жидкости больных, у которых поражение глаз сочеталось с различной неврологической симптоматикой, отмечалось полное совпадение результатов исследования (как положительных, так и отрицательных).
Спинномозговая пункция производилась с целью уточнения неврологического диагноза у больных. Эти данные свидетельствуют о частом сочетании при токсоплазмозе поражения органа зрения, а центральной нервной системы.
Из изложенного следует, что серологические методы исследования при токсоплазмозной инфекции глаз достоверны. При правильной их оценке и сопоставлении с клиническими проявлениями заболевания и результатами дифференциальной диагностики можно определить этиологию заболевания.
С целью определения специфической сенсибилизации организма к токсоплазменному аллергену наиболее часто применяют внутрикожную аллергическую пробу.
Статья из книги: Терапевтическая офтальмология | Краснов М.Л.; Шульпина Н.Б..


Комментариев 0