Классификация, клинические формы, диагностика и лечение хориоретинальных дистрофий и атрофии (Часть 2)

Описание
КЛАССИФИКАЦИЯ ПЕРВИЧНЫХ И ВТОРИЧНЫХ ДИСТРОФИЙ ЖЕЛТОГО ПЯТНА
- I. Склеротические (старческие и предстарческие) дистрофии желтого пятна:
1. Ранние: «сухая» (преддисковидная), серозная хориоретинопатия, кисты желтого пятна.
2. Поздние: геморрагически-экссудативная и псевдотуморозная фазы дистрофии Кунта — Юниуса, ложные и истинные разрывы сетчатки в макуле, разлитой хориоваскулосклероз Шерера.
- II. Семейные наследственные (абиотрофические) дистрофии желтого пятна:
1. Ранние (детского и юношеского возраста) с первичным поражением нейрорецепторов, пигментного эпителия или ганглиозных клеток сетчатки:
- сочетающиеся с поражением центральной нервной системы или другими нарушениями (болезнь Тея — Сакса, Ниманна — Пика, Билыновского, синдром Амальрика и др.);
- без поражений центральной нервной системы или др. общих проявлений (желточная дистрофия Веста, дистрофия Штаргардта, прогрессивная колбочковая дистрофия, прогрессивная фотопическая дисфункция, желто-пятнистое глазное дно, бабочковидная дистрофия, сетевидная дистрофия Шегрена).
2. Поздние (проявляющиеся в полной мере у лиц зрелого возраста) с первичным поражением:
- мембраны Бруха (коллоидные дистрофии Дойна, левантинская болезнь, дистрофия Кендори);
- хориоидальных сосудов (ареолярный и диффузный хориосклероз Сорсби, ползучая перипапиллярная атрофия, извилистая атрофия).
- III. Вторичные поствоспалительные, посттравматические и постинтоксикационные дистрофии желтого пятна с преимущественным поражением:
- нейрорецепторов и пигментного эпителия;
- мембраны Бруха;
- собственно хориоидеи.
Склеротические (старческие и предстарческие) дистрофии желтого пятна
Возраст лиц, у которых обнаруживаются так называемые старческие и предстарческие дистрофии желтого пятна, колеблется от 35—40до 80 и более лет. Дистрофии такого рода составляют 45,9% макулодистрофий, а в возрастной группе старше 50 лет частота их возрастает до 76,5%.
Бесспорна ведущая роль атеросклероза в развитии старческих макулодистрофий. Так, Т. И. Селицкой гистологически и гистохимически подтверждены атероматозные изменения мембраны Бруха и хориоидеи в заднем полюсе глаза у больных атеросклеротической болезнью. Патология в 20% наблюдений сочеталась со страданием ретинальной ткани.
У больных старческими и предстарческими дистрофиями желтого пятна прослежены свойственные атеросклерозу диспротеинемия, высокий уровень липидов и наклонность к гиперкоагуляции крови.
Безусловно, имеет значение известная генетическая предрасположенность к атеросклерозу.
Ранняя сухая склеротическая дистрофия желтого пятна
(полиморфная склеротическая дистрофия) известна также как начальная центральная склеротическая хориоретинопатия. Определение «ранняя сухая склеротическая дистрофия макулы» дает качественную характеристику процесса и с этих позиций представляется более удобным. По нашим данным, эта форма составляв 27,2% макулярных дистрофий и служит самым ранним проявлением атеросклеротических изменений желтого пятна.
Заболевание обычно протекает с небольшими видимыми и функциональными нарушениями. У большинства больных сохраняется высокая острота зрения (0,5 и выше), а центральные скотомы, в том числе микроскотомы, определяются только у 1/3—1/4больных. Несколько чаще имеют место извращения цветовосприятия, патология феномена Гайдингера, снижение частоты воспроизведения светового ритма в красном свете, изменения электроокулограммы.
Офтальмоскопически обнаруживаются лишь исчезновение макулярных рефлексов, крапчатость, небольшие друзы, иногда одиночные мелкие кровоизлияния.
При биомикроскопии хорошо видны мелкие круглые желтоватые друзы, которые нередко расположены вблизи концевых отделов перимакулярных капилляров. Возникает деструкция пигментного эпителия с появлением точечной насыпи пигмента и отдельных незначительных глыбок, что нагляднее при последовательном осмотре в свете красного и синего фильтров. Желтое окрашивание центральной ямки в бескрасном свете нивелируется или полностью отсутствует.
При более выраженной патологии нарастает деструкция пигментного эпителия и крапчатость в заднем полюсе глаза. Друзы увеличиваются в числе и размерах, местами конфлюируют. На уровне сосудистой определяются плоские желтоватые, нечетко контурированные пятна — очаги липоидоза мембраны Бруха, усиливается хориосклероз.
Острота зрения у таких больных снижается до 0,2—0,4. Чаще обнаруживаются центральные скотомы, нарушения цветовосприятия и другие функциональные сдвиги.
Примерно у 1/3 больных ранней сухой склеротической дистрофией желтого пятна склероз ретинальных сосудов не улавливается и патология макулы наряду с биохимическими нарушениями является единственной клинической манифестацией атеросклероза.
Гистологически и гистохимически уже в этой фазе болезни выявляется отложение липидов и формирование суданофильных друз в стекловидной пластинке хориоидеи. Начинается деструкция пигментного эпителия и мембраны Бруха в зонах липоидоза, хориокапилляры облитерируются.
Патология стекловидной пластинки хориоидеи сопровождается нарушением ее проницаемости и отложением под мембраной суданофильных масс, что провоцирует ухудшение трофики и способствует субретинальной неоваскуляризации. Нарастающая патология стекловидной пластинки сосудистой оболочки завершается серозной отслойкой пигментного эпителия. Выраженность субретинальной транссудации варьирует, но, как показывают морфологические исследования, серозная отслойка пигментного эпителия постоянно сопутствует развитию дисковидной дистрофии.
Клинически такая транссудативная декомпенсация знаменуется снижением остроты зрения и появлением положительной, иногда относительной центральной скотомы. В макуле возникает сероватый диск отечной сетчатки, окруженный ложным ареолярпым рефлексом. Биомикроскопически ретинальный срез отчетливо расширен и приподнят, иногда с конверсирующим передним профилем.
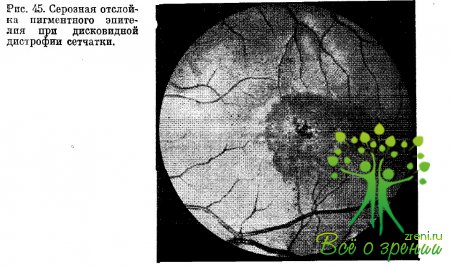
От серозной хориоретипопатии другого генеза патология отличается сероватой опалесценцией сетчатки, наличием всех элементов ранней сухой макулодистрофии перифокально и более значительным снижением зрения (рис. 45).
Флуоресцентная ангиография, выявляющая в ранней сухой фазе лишь свечение друз на протяжении 2—12 мин и более, а иногда и более разлитую и длительную флюоресценцию в зонах липоидоза, при серозной отслойке уже в ранней артериальной фазе демонстрирует яркие флюоресцирующие пятна — участки просачивания элементов плазмы через мембрану Бруха и дефекты пигментного эпителия. Затем свечение становится более диффузным. Обнаруживается также субретинальная неоваскуляризация в виде отдельных петель или сплошного ярко светящегося уже в артериальной и артериовенозной фазе полусерна на более темном фоне. В последнем случае предполагают существование субретиналькой неоваскулярной мембраны. Отсутствие фонового свечения прилежащей хориоидеи должно быть связано со склеротической облитерацией хориокапилляров, что, вероятно, и провоцирует новообразование сосудов.
Подобная серозная хориоретинопатия может претерпеть обратное развитие, но чаще осложняется появлением массивных геморрагий, исходящих из новообразованных субретинальных сосудов или самой хориоидеи. Иначе говоря, через суадию серозной отслойки ранняя сухая склеротическая макулодистрофия переходит в следующую фазу — дисковидную дистрофию Кунта—Юниуса.
Дисковидная дистрофия Кунта—Юниуса.
Описана как самостоятельная нозологическая единица в 1920 г. Не вызывает сомнений ее развитие из более ранней сухой (полиморфной) хорио-ретинопатии. Это подтверждается выявлением всех элементов ранней сухой фазы — друз, диспигментации, хориосклероза вокруг дисковидного очага и наличием ранней сухой макулодистрофии на «здоровом» парном глазу. При динамическом наблюдении неоднократно прослежено превращение ранней сухой фазы в дисковидную.
Более того, биоморфоз мембраны Бруха, детально изученный W. Lerche (1972), свидетельствует о неизбежных возрастных изменениях мембраны по типу ранней сухой склеротической дистрофии даже у клинически здоровых людей 30—35 лет. Процесс начинается с деструкции эластических волокон и формирования друз. В возрасте 40—45 лет при исчезновении фовеального рефлекса патология мембраны нарастает и сопровождается накоплением в макулярной зоне сетевидных структур — продуктов деградации коллагена в полисахаридной матрице.
В60 лет и старше в мембране обнаруживаются отложения кислых мукоидов, липидов, включения осмофильных элементов, дающих окраску на кальций, возникает се набухание и отторжение клеток пигментного эпителия. Патология достигает максимума при наличии офтальмоскопически видимых изменений.
Собственно дисковидная фаза болезни чаще наблюдается у лиц в возрасте 60 лет и старше, причем со временем поражение становится билатеральным.
Клиника дисциформной дистрофии характеризуется возникновением обширных (4—6 PD) кровоизлияний в заднем полюсе глаза приподнимающих и расслаивающих сетчатку. Острота зрения падает до сотых, реже — 0,1—0,2. В поле зрения определяется положительная абсолютная центральная скотома.
Биомикроскопически в этой геморрагически-экссудативной стадии процесса выявляется отечная сетчатая оболочка, которая серовато опалесцирует. На поверхности и в толще ретинального среза, а также субретинально просматриваются кровоизлияния различной величины. Оптический срез сетчатки неравномерно расширен с волнообразным передним и неотчетливым задним; контуром. В зоне мутного отека нередко возникают кистозные полости в сетчатке.
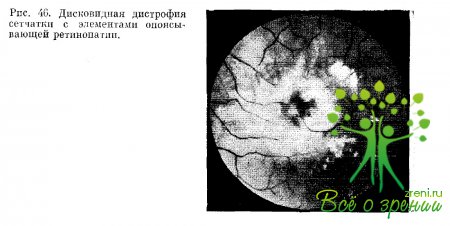
Сосуды сетчатки склерозированы. Примерно у 1/4больных дис-ковидная дистрофия сочетается с опоясывающей ретинопатией, а у 22,6 % — со склеротической атрофией диска зрительного нерва (рис. 46).
Рецидивы геморрагий и частичное их рассасывание дают чрезвычайно пеструю картину, которая дополняется отложением глыбок пигмента и образованием субретинальных пигментированных: шварт.
Заболевание завершается организацией крови и экссудата с образованием плотного бугристого проминирующего очага размером 2—5 РD, пронизанного новообразованными сосудами. Острота зрения необратимо падает, обычно до малых сотых. Большое сходство видимых изменений с опухолью побудило А. Еlsching (1919) назвать такой фокус «псевдотумором». Сходство с опухолью может быть настолько велико, что возникает необходимость в специальных методах дифференциально-диагностического, в том числе радиологического, исследования.
Флуоресцентная ангиография свидетельствует о большей тяжести поражения при дистрофии Купта—Юннуса по сравнению с ранней сухой хорноретинопатией. Наблюдается нарастание времени «рука—сетчатка», выраженное замедлением ретиналыюй циркуляции, длительное (30 мин и более) свечение зоны серозной и экссудативной отслойки, очагов липоидоза и кальциноза.
Гистологически имеет место липоидоз сосудистой и мембраны Бруха, ее кальциноз, фрагментация. Обнаруживаются пролиферация и отторжение клеток пигментного эпителия, появление суб- и интраретинальных шварт, глиоз сетчатки, неоваскуляризация .
[banner_centerrs]
{banner_centerrs}
[/banner_centerrs]
Таким образом, течение дисциформной дистрофии складывается из:
- сухой (преддисковидной) хориоретинопатии;
- экссудативно-геморрагической фазы;
- стадии псевдотуморозного пролиферата.
В исходе отечных и экссудативно-геморрагических изменений возможно развитие макулярной фиброплазии, что сопровождается возникновением плоских бликовых рефлексов и формированием характерной «целлофановой» макулы.
Поздний разлитой хориоваскулосклероз в заднем полюсе глаза
(дистрофия Шерера) проявляется в полной мере у лиц в возрасте 70 лет и старше. Является одной из поздних форм склеротических дистрофий желтого пятна.
Развитие подобной патологии, по-видимому, связано с преимущественными атеросклеротическими изменениями собственно сосудистой оболочки в заднем полюсе глаза. Фиброз и облитерация хориоидальных сосудов при этом несколько тормозят липоидное перерождение мембраны Бруха. Не исключено, что известную роль в преимущественном склерозировании собственно сосудов сосудистой играет интенсивный атероматоз офтальмической артерии с адаптационным склерозом ее конечных веточек и выраженным их сужением.
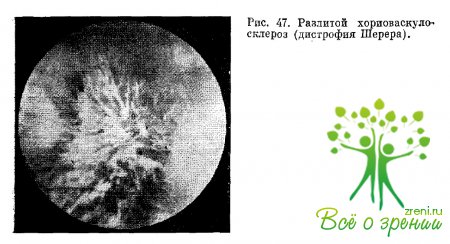
В заднем полюсе глаза у таких больных возникает обширная, выходящая за пределы височных сосудов зона депигментации пигментного эпителия, где отчетливо просматриваются склерозированные хориоидальные сосуды и белые очаги фиброзной ткани. Обнаруживаются отдельные скопления пигмента, геморрагии. Участок поражения имеет нечеткую фестончатую границу (рис. 47).
Сосуды сетчатки резко сужены, ветвятся под острым углом, как правило, имеет место частичная склеротическая атрофия диска зрительного нерва. Определяются грубая липоидпая дуга в роговице, атрофия радужной оболочки, начинающиеся катаракты. Острота зрения снижается до 0,02—0,03, возникает отрицательная центральная скотома.
Кисты желтого пятна при атеросклерозе.
Относятся к ранним склеротическим макулодистрофиям и обычно развиваются на фоне гипертонической или гипотонической ангиопатии сетчатки, т. е. в связи с отчетливыми циркуляторными нарушениями.
Жалобы больных сводятся к искажению формы предметов и некоторому их затуманиванию. Острота зрения колеблется в зависимости от величины кисты и сопутствующих склеротических изменений от 0,6—0,8до 0,1—0,2. Возникает центральная относительная положительная скотома.
Размеры кисты варьируют от 1/5 до 1/3, реже 1/2 РD. Офтальмоскопически выявляется небольшое красное пятно в макуле, очерченное дуговым рефлексом. Перифокально могут наблюдаться легкая диспигментация, друзы и даже мелкие складки натяжения сетчатки.
При биомикроофтальмоскопии хорошо улавливается расширение оптического среза сетчатки над областью кисты с конвексированием его переднего профиля.
Со временем возможно превращение кисты в ложный (эрозия) или истинный разрыв сетчатки.
Ложные и истинные разрывы сетчатки в желтом пятне.
Возникают в исходе более ранней кистозной склеротической дистрофии макулы (вначале рвется передняя стенка кисты) или в результате ишемических инфарктов ретины. По наблюдениям М. Маldencoznи N. Lipton(1977), эрозии и разрывы сетчатки в макуле при атеросклерозе наблюдаются чаще у женщин в возрасте старше 60 лет и нередко располагаются у концевых отделов перимакулярпых капилляров. Возможно сочетание с интенсивным хориосклерозом.
Как сквозной, так и несквозной дефект сетчатки офтальмоскопически представляется ярко-красным пятном размером от 1/8 до 1/2 РD. Характерным признаком несквозного разрыва (эрозии) является исчезновение только переднего контура среза сетчатки над патологическим фокусом. Иногда наблюдается уплотнение края дефекта с появлением отдельных белесоватых точек, что лучше видно в бескрасном свете.
Сквозной разрыв сетчатки в макуле осложняется вначале ограниченной перифокальной отслойкой с сероватым набуханием сетчатки вокруг разрыва. Полоса оптического среза сетчатки в области разрыва полностью исчезает.
Сквозные разрывы и эрозии сетчатки в желтом пятне, как правило, вызывают снижение зрения до 0,1—0,2 и даже до сотых. Обнаруживается центральная отрицательная скотома.
В отдельных случаях при точечных дефектах может сохраниться высокая острота зрения (0,8 и даже 1,0), но возникают искажение формы предметов и микроскотомы, определяющие «выпадение» отдельных букв или их деталей при чтении.
Кольцевидная (опоясывающая) ретинопатия.
Описана J. Hutchinson в 1876 г. Процесс связан с нарушенной проницаемостью сосудистой стенки, что весьма свойственно атеросклерозу, но может иметь место и при диабете, непроходимости ретпнальных сосудов, в том числе васкулитах и пр.
Нередко кольцевидная ретинопатия сочетается с различными формами склеротических макулодистрофий, чаще всего с дисковидной дистрофией Кунта—Юниуса.
Изменения при опоясывающей ретинопатии локализуются в парамакулярных отделах сетчатки и представляют собой белые, с серебристым блеском, неправильной формы очажки, образующие скопления в форме кольца, полукольца или лишь отдельные, идущие по радиусам, элементы. В зависимости от большей или меньшей компактности этого полукольца, отличающегося четким, но неровным фестончатым контуром, различают «сливную» и «порозную» формы. Последняя отличается своеобразным ажурным рисунком, напоминающим скопления чешуек или иногда отдельные штрихообразные лучи.
Процесс может быть одно- и двусторонним. Изменения, как правило, асимметричны.
В поле зрения возникает кольцевидная скотома. Острота зрения зависит от состояния макулы, склеротических изменений зрительного нерва и других сопутствующих поражений.
Морфологически обнаруживаются скопления белкового выпота: пенистые клетки, макрофаги, отложения гиалина.
Возможны та или иная степени обратного развития кольцевидной ретинопатии, если последняя зависит от временной сосудистой дизории (например, в случае непроходимости ретинальных сосудов, особенно при ретиноваскулитах).
Лечение склеротических дистрофий желтого пятна и опоясывающей ретинопатии
как и лечение атеросклеротической болезни, пока недостаточно эффективно.
Важнейшим моментом црофилактики и лечения атеросклероза является, как известно, рациональный диетический режим с ограничением калорийности суточного рациона, особенно жиров и легкоусваиваемых углеводов. Чрезвычайно важна физическая активность людей пожилого и старческого возраста.
Отчетливым гипохолестеринемическим действием обладают, в частности, атромид, атромид С (клофибрейт) и их венгерский аналог мисклерон, которые одновременно повышают фибринолитическую активность кровь и уменьшают склеивание тромбоцитов. Препарат применяется в капсулах по 0,25 г 2—3 капсулы 3 раза в сутки после еды в течение 20—40 дней. Курс повторяют несколько раз. Эффективность мисклерона при атеросклеротических хориоретинопатиях подтверждают К. В. Трутнева и соавт. (1973), М. Г. Марголис (1976) и др.
Рекомендуется цетамифен, предпочтительно в больших дозах (до 0,75 г 3 раза в день) на протяжении 1—3 мес. Рациональна комбинация цетамифена по 0,5 г 3 раза в сутки с восходящими дозами никотиновой кислоты сразу после еды, начиная с 0,03 г на прием, в течение 20—25дней. Длительное применение никотиновой кислоты внутрь показано для активации фибринолизина.
Широко используют препараты йода, отличающиеся, несмотря на слабый липотропный эффект, достаточно выраженным в течение нескольких месяцев последействием.
Показаны линетол, диоспонин или полиспонин в обычных терапевтических дозах и другие липотропные средства.
Рационально назначение витамина Е в форме токоферола до 100 мг в сутки или левита по 1мл подогретого раствора внутримышечно; на курс 20 инъекций. Полезен витамин В6 по 1 мл 5% раствора в течение 10—15дней.
Большую роль играют ангиопротекторы, улучшающие состояние сосудистой стенки. Так, пармидин (продектин) применяют по 0,25г, а затем по 0,75 г 3—4 раза в сутки; курс лечения от 2 до 6 мес. Препарат препятствует отложению холестерина в интиме артерий, снижая агрегацию тромбоцитов и нормализуя состояние эндотелия, улучшает микроциркуляцию. Показан трентал по 200 мг или 2 драже 3 раза в сутки при длительном приеме (30— 40 дней и более); затем назначают поддерживающую дозу (1 драже 2—3 раза в сутки). Применяют также компламин или теоникол в обычных терапевтических дозах.
Назначают биостимуляторы, в том числе анаболические стероиды. Так, неробол назначают по 4 мг 1 раз в сутки (на курс 20—25приемов) или по схеме: 10 дней по 2,5 мг 2 раза в сутки, 10 дней по 2,5 мг 1 раз и 5 дней по 1 мг 1 раз в сутки. Через 4— 6мес курс повторяют.
Весьма положительно оценивается роль малых доз гепарина (по 5000—8000 ЕД в сутки, на курс 15—20инъекций) парентерально. Е. Л. Смидович (1978) предпочитает субконъюнктивальное введение гепарина по 0,2—0,3 мл ежедневно или через день (на курс 10инъекций). Полезен электрофорез гепарина (5000— 10 000 ЕД на ванночку, с анода, при силе тока 0,5—1 мА, продолжительность процедуры 15—20 мин, на курс 10—20сеансов).
Перечисленные средства должны широко использоваться для «фонового» лечения склеротических хориоретинопатий. В остальном показан дифференцированный подход в зависимости от характера возникающих изменений. Так, при ранней сухой склеротической дистрофии желтого пятна с субклиническими нарушениями достаточно проведения общей липотропной терапии, назначения ангиопротекторов, контроль за кровяным давлением.
Центральная серозная хориоретинопатия требует добавления дегидратирующей и рассасывающей терапии. Рекомендуются форез с алоэ, 3% раствором калия йодида, фибринолизином, назначение рутина, левита. Наилучший эффект дает фотокоагуляция участка просачивания при условии, что последний находится не ближе 450—500 мкм от фовеолы. Фотокоагуляция проводится на основании данных флуоресцентной ангиографии.
При использовании аргонового лазера мощность составляет 150—400 мВт, экспозиция до 0,2с, диаметр пятна 50—200 мкм. Проводится также барраж по краю выявленного очага неоваскуляризации с последующей более энергичной коагуляцией неоваскулярного фокуса, мощность до 500 мВт, экспозиция до 0,5 с.
Появление обширных кровоизлияний в заднем полюсе мотивирует необходимость применения дицинона внутрь в сутки до 3—6таблеток по 0,25 г и парабульбарно по 0,3—0,5 мл 12,5% раствора в течение 10—12 дней. Применяется энергичная рассасывающая терапия: лидаза под кожу виска по 16—32 ЕД, трипсин внутримышечно по 5—10 мг (на курс 15инъекций). Показаны фибринолизин под конъюнктиву по 800—1000 ЕД (на курс 15— 20инъекций), а также папаин, применяемый путем электрофореза или парабульбарно.
Л. В. Зобина (1976) проводит электрофорез путем биостимуляторов, фибринолизина или лидазы эндоназально в комбинации с микроволновой терапией местно (на курс 15— 20 сеансов). Эффективность микроволновой терапии отмечает И. Н. Абрамова (1974) (аппарат «Луч-58», диаметр излучателя 9 см, расстояние от глаза 10 см, интенсивность 20 Вт, продолжительность процедуры 15—20 мин).
Для борьбы с дистрофией и улучшения микроциркуляции применяют никотиновую кислоту, или компламин, гепарин в липотропных дозах, витамин В6, АТФ и др. Необходимо нормализовать кровяное давление.
Активную терапию продолжают до исчезновения мутного отека сетчатки и стабилизации остроты зрения. Липотропная терапия и лечение антиопротекторами проводятся не менее 4—6 мес.
Возможность фотокоагуляции при выраженных геморрагически-экссудативных изменениях дискутабельна. А. С. Акопян пользуется коагуляцией с первоначальной демаркацией геморрагической отслойки. A. Bird и К. Grey (1979) применяют криптоновый лазер, преимущественно воздействующий на субретинальные структуры.
Склеротические эрозии и разрывы подлежат коагуляции. Применяют малые энергии: 0,54—2,0 Дж («Opton»), 0,32—0,54 Дж (УЕВ-5000) и 0,05—0,11 Дж (ОК-1), аппликации непосредственно по краю или вокруг отверстия, исключая зону папилломакулярного пучка. При малых дефектах можно нанести один коагулят на дно разрыва так, чтобы его край чуть захватил прилежащую сетчатку. Повреждения папилломакулярного пучка при этом не отмечено, острота зрения закономерно повышается до 0,2—0,4.
Разлитой хориоваскулосклероз в заднем полюсе требует интенсивной сосудорасширяющей и дедистрофической терапии. Показаны препараты, избирательно влияющие на сосуды мозга (стугерон, галидор, эуфиллин), и средства, улучшающие микроциркуляцию (трентал, компламин и пр.). Не исключена попытка реваскуляризирующих операций.
М. М. Краснов и соавт. (1976) разработали оригинальный метод фотостимуляции при склеротических и вторичных макулодистрофиях. Авторы относят лечебный эффект за счет повышения фагоцитарной активности пигментного эпителия сетчатки.
По экспериментальным данным Н. И. Усова и соавт. (1981), облучение аргоновым лазером на 135 % повышает содержание РНК в нейрорецепторах сетчатой оболочки, что улучшает механизмы их защиты и адаптации.
При применении рубинового и неодимового лазера излучение составляет от 0,0001 до 0,001 Дж. Аппликации наносят в 2ряда в виде полудуги, открытой к диску зрительного нерва. Улучшение при применении рубинового лазера отмечено у 48,8%, неодимового — 71,7%и аргонового — у 63 % больных склеротическими макулодистрофиями.
Наследственные центральные дистрофии (абиотрофии)
Наследственные центральные тапеторетинальные дистрофии возникают в связи с генетическим дефектом, определяющим несостоятельность ферментативных систем и связанных с ними обменных процессов. Наблюдаются свойственные абиотрофиям закономерности: семейный тип поражения, заболевание в определенной возрастной группе и «зеркальный» характер видимых на глазном дне изменений. Патология может касаться строго желтого пятна или выходить за его пределы.
В целом наследственные макулодистрофии составляют, по нашим данным, до 38%общего числа дистрофий желтого пятна.
Впрочем, выявление наследственного характера болезни удается далеко не всегда. Возможно возникновение фенокопии наследственного процесса при различных эмбриопатиях, наблюдаются и спорадические случаи.
Ниже представлена характеристика частных форм макулярных абиотрофий, за исключением болезни Ниманна—Пика и Тея—Сакса, которые освещены в группе липоидозов.
Желточная (вигеллиформная) дистрофия желтого пятна
была описана еще в 1905 г. Вестом, который проследил у 8 маленьких детей образование в макуле очага в форме четко ограниченного овала или диска. Автор отметил благоприятное течение болезни с длительным сохранением высокой остроты зрения и отсутствием центральной скотомы.
В отличие от других абиотрофий процесс может проявиться в широком возрастном диапазоне (от новорожденных до лиц в возрасте 30 лет и старше).
Поражение наследуется аутосомно-доминантно, отличается определенной стадийностью течения и может быть монолатеральным.
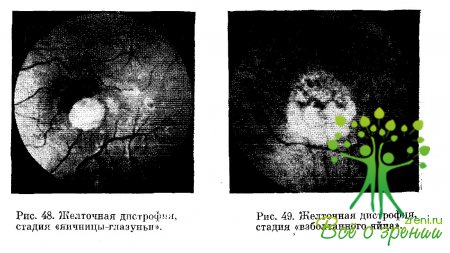
В первой фазе («яичницы-глазуньи») в макуле возникает крупная киста с прозрачным или гомогенно-желтоватым содержимым, размером 1—1,5 PD (рис. 48). В одной семье возможны оба варианта изменений, причем крупные кисты с бесцветным прозрачным содержимым определяются у самых молодых членов семьи. В этой стадии болезни центральная скотома отсутствует и сохраняется нормальная или субнормальная острота зрения.
Вторая фаза («взболтанного яйца») отличается развитием отека и агрегацией комков экссудата в очаге, не исключено появление кровоизлияний. Острота зрения надает до сотых, реже 0,1—0,2. Постепенно отек и геморрагии исчезают, и на месте кисты формируется плоский атрофический желтоватый фокус размером от 0,5 до 1,5 РD, присыпанный мелким пигментом (рис. 49).
Морфологически в стадии «взболтанного яйца» в макуле определяется деструкция пигментного эпителия, атрофия хориокалилляров, истончение мембраны Бруха, отчасти гибель иейрореценторов.
Полагают, что своеобразное течение заболевания объясняется первичным страданием клеток пигментного эпителия, а не нейрорецепторов сетчатки.
Закономерна патология электрокоокулограммы со снижением коэффициента Ардена (140%и менее) при нормальной ЭРГ или тенденции к исчезновению волны «с». Изменения электроокулограммы нередко рассматриваются как специфическая особенность желточной дистрофии, отличающая ее от псевдовителлиформных процессов, в том числе спорадических случаев болезни. Отмечают изменение электроокулограммы у кровных родственников больного, даже при нормальном глазном дне.
Представляется, однако, что электроокулограмма сама по себе не может быть решающим критерием, позволяющим дифференцировать наследственный и приобретенный характер болезни. Как справедливо подчеркивает J. Fran?ois (1979), этот показатель отражает скорее степень и протяженность изменений в макуле на уровне пигментного эпителия и мембраны Бруха при самых различных поражениях (например, миопическая болезнь). Более того, описано сохранение нормальной электроокулограммы у девочки с желточной дистрофией, в семье которой это заболевание разной степени выраженности имело место в трех поколениях.
Лечение желточной дистрофии малоперспективно. А. С. Новохатский и Е. Л. Стародубцева (1971) отмечают стабилизирующий эффект биостимуляторов. При появлении крови и экссудата применяется рассасывающая, дегидратирующая и неспецифическая дедистрофическая терапия. Необходимы исключение и санация очагов фокальной инфекции.
Дистрофия, описанная К. Stargardt в 1909—1913 гг. у детей и подростков как «семейная прогрессивная дегенерация желтого пятна», является одной из самых частых форм макулярных абиэтрофий.
Заболевание проявляется между 8 и 16 годами, чаще носит рецессивный характер и к 20—25 годам обычно приводит к падению зрения вплоть до сотых. Процесс, как подчеркивал еще К. Stargardt, частично или полностью захватывает желтое пятно и даже распространяется за его пределы.
Вариабельность видимых изменений, как и нарастание патологии, адекватно давности болезни приводят к известным расхождениям в описании офтальмоскопической картины. Ряд исследователей отмечают две принципиальные возможности: патология ограничена областью желтого пятна или вовлечены и парамакулярные отделы.
Статья из книги: Терапевтическая офтальмология | Краснов М.Л.; Шульпина Н.Б..


Комментариев 0