Наш опыт применения биоматериала для послойной кератопластики
Содержание:
Описание
↑ Наш опыт применения биоматериала для послойной кератопластики
Автор: P. 3. Кадыров
ФГУ Всероссийский центр глазной и пластической хирургии Росздрава, Уфа
Проанализированы результаты применения биоматериала алпопланта (БМА) для послойной кератопластики (ПКП) во Всероссийском центре глазной и пластической хирургии. Наиболее часто ПКП с применением БМА производили у пациентов с послеожоговыми поражениями органа зрения (40,2%), т. е. у наиболее тяжелого контингента больных.
Рассмотрены варианты комбинаций БМА для ПКП с другими аллоплантами. Чаще всего встречались комбинации алпопланта для ПКП с аллоплантом для пластики конъюнктивы и аллосухожильньши нитями (24,5%), что позволяло закрыть трансплантатами обширные операционные раны роговицы и конъюнктивы.
Анализ остроты зрения в отдаленный периоду 241 пациента показал достоверное улучшение зрительных функций. Описаны осложнения при ПКП с применением БМА.
Рассмотрены варианты комбинаций БМА для ПКП с другими аллоплантами. Чаще всего встречались комбинации алпопланта для ПКП с аллоплантом для пластики конъюнктивы и аллосухожильньши нитями (24,5%), что позволяло закрыть трансплантатами обширные операционные раны роговицы и конъюнктивы.
Анализ остроты зрения в отдаленный периоду 241 пациента показал достоверное улучшение зрительных функций. Описаны осложнения при ПКП с применением БМА.
Офтальмологи часто сталкиваются с проблемой наличия пересадочного материала для кератопластики. Как правило, с трансплантационной целью используют донорскую роговицу, свежую или консервированную разными методами (силиковысушенная, консервированная в меде и т. д.). Забор донорского материала, доставка его в клинику, исследование на различные инфекции возможны лишь в крупных офтальмологических клиниках при наличии специальных служб и лабораторий.
Кроме того, большая часть донорского материала непригодна для кератопластики, так как инфицирована или качество роговицы ухудшается после забора трупного материала. В результате пациенты вынуждены длительное время ждать трансплантат для кератопластики. В связи с этим ведется поиск пересадочных материалов, альтернативных донорской роговице.
Так, в качестве трансплантационного материала для кератопластики были предложены обезвоженная роговица [2], амнион [4, 6] и твердая мозговая оболочка [6], хрящ трахеи и бронхов мертворожденных [5], аутохрящ уха [3]. Эффективность лечебной кератопластики донорским материалом, консервированным в меде, изучали В. Г. Абрамов и Н. А. Маркичева [1]. Несмотря на разнообразие предлагаемых для кератопластики материалов, они не получили широкого применения в клинике.
↑ Материал и методы
В ФГУ Всероссийский центр глазной и пластической хирургии Росздрава для послойной кератопластики (ПКП) предложен биоматериал аллоплант (БМА), который представляет собой участок ткани сухожилия белого цвета округлой формы диаметром от 5 до 11 мм или неправильной формы для барьерной кератопластики; толщина биоматериала 100 и 200 мкм.
[banner_centerrs] {banner_centerrs} [/banner_centerrs]
БМА выпускают во флаконах готовым к применению (ТУ 42-2-537—2006); срок хранения — до 5 лет при комнатной температуре. Трансплантат легко моделируется по форме дефекта, что позволяет во время операции сохранить прозрачные участки роговицы. Эффективность операций оценивали с помощью современных средств математико-статистической обработки данных [7].
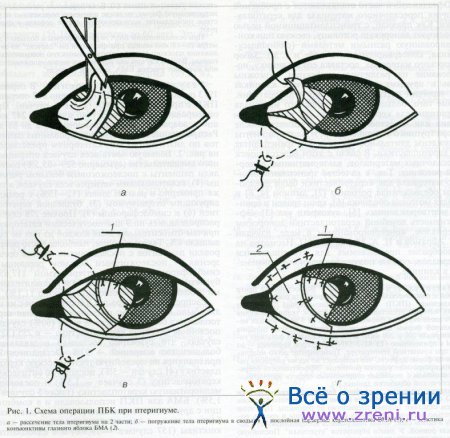
↑ Техника операции послойной барьерной кератопластики (ПБК) с применением БМА при птеригиуме
Кератотомическим лезвием отделяют головку птеригиума от роговицы. При этом желательно достичь прозрачных слоев роговицы и срезать роговицу в одном слое, чтобы поверхность воспринимающего ложа была ровной. У лимба образуется "ступенька". Послойную барьерную кератопластику производят в том случае, когда срезан слой роговицы толщиной более 150 мкм.
Аллотрансплантат в форме дугообразной полосы или трапециевидной формы накладывают на дефект роговицы вдоль лимба и фиксируют двумя или четырьмя узловыми швами 8:0, 10:0. Внутреннюю прямую мышцу берут на шов-держалку. Тело птеригиума рассекают на 2 части и погружают в своды. Крупные кровеносные сосуды эписклеры у лимба коагулируют. Производят аутопластику конъюнктивы, но, если дефект конъюнктивы был большим, используют БМА для пластики конъюнктивы глазного яблока (рис. 1).
↑ Техника операции послойной барьерной кератопластики с применением БМА при бельме
Трепаном делают насечку на роговице на глубину поражения (до 2/3 толщины роговицы). Мутные слои роговицы иссекают по возможности до прозрачных слоев. На дефект укладывают БМА для ПКП таким образом, чтобы его поверхность была ниже уровня роговицы для "наползания" роговичного эпителия. Фиксацию трансплантата осуществляют узловыми швами 8:0. Если поражение роговицы имеет неправильную форму, то после иссечения пораженных ее участков трансплантат моделируют по форме дефекта и фиксируют.
При использовании БМА округлой формы и большого диаметра (9—11 мм) иногда при фиксации он "парусит" из-за наложения плоского трансплантата на выпуклую поверхность роговицы. В таких случаях или применяют частое наложение швов или вырезают участок БМА, который "парусит".
↑ Результаты и обсуждение
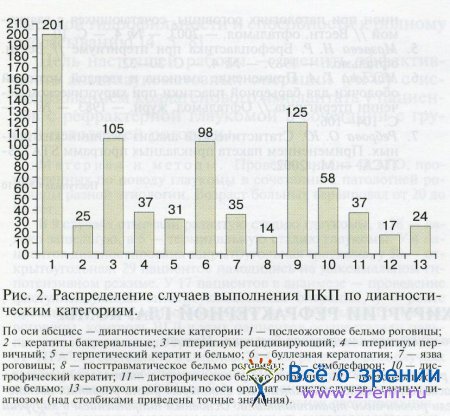
В период с 1973 по 2009 г. в ВЦГиПХ проведено 807 операций ПКП с применением БМА (далее — случаи). Прооперировано 693 человека (446 мужчин и 247 женщин), возраст которых варьировал от 2 до 88 лет. Распределение количества оперированных пациентов по диагностическим категориям представлено на рис. 2.
Большую часть всех случаев операционного вмешательства (суммарно 529—65,5%) составляли пациенты с послеожоговым бельмом роговицы (1), охватывающим четверть всех случаев, а также примерно в равных долях (12—15%) с рецидивирующим птеригиумом (3), буллезной кератопатией (6) и симблефароном (9).
Прочие 278 случаев распределились по 9 диагностическим категориям, причем относительная доля каждой из них не превышала 8%. Таким образом, наиболее часто оперировали пациентов с последствиями ожогов органа зрения — послеожоговым бельмом роговицы и симблефароном (40,2%), птеригиумом (17,6%), буллезной кератопатией (12,1%) и воспалительными заболеваниями роговицы (суммарно 11,1%).
Распределение операций в соответствии с их целью было следующим: послойная барьерная кератопластика была произведена в 488 (60%) случаях, послойная лечебная кератопластика — в 255 (32%) случаях, что суммарно составило подавляющее большинство операций — 92%. Оставшиеся 8% приходились на послойную тектоническую кератопластику (41 случай — 5%), послойную оптическую кератопластику (5 случаев — 1,5%) и послойную мелиоративную кератопластику (также 5 случаев — 1,5%).
БМА для ПКП использовали и в комбинации с другими аллоплантами (51,7% случаев), наиболее часто — с аллоплантом для пластики конъюнктивы (157 случаев — 19,5%) и с аллоплантом для пластики конъюнктивы и аллосухожильными нитями (198 случаев — 24,5%). Гораздо реже использовали комбинации с ауто конъюнктивой (2,8%), аутослизистой оболочкой губы (1,1%), аллосухожильными нитями (0,9%), диспергированным аллоплантом (0,7%). Менее чем в 0,5% случаев имели место комбинации с донорской роговицей, аллоплантом для реваскуляризирующих операций, для каркасной пластики век, для склеропластики и спонч-дренирования.
Предварительный анализ показал, что из-за широкого спектра патологических состояний роговицы, резких различий глубины нарушения зрения, многообразия вариантов применения ПКП и практически необъятного числа сочетаний этих явлений и факторов детальный анализ последствий ПКП для восстановления важнейшей функции зрения — остроты зрения (03) потребует применения специальных методов математико-статистической обработки, подробное изложение результатов которых явно выходит за пределы одной журнальной статьи.
В силу этого пока мы ограничимся описанием некого "валового" результата применения ПКП без учета особенностей диагностических групп, методов лечения и исходного состояния зрительных функций. При этом сразу следует подчеркнуть, что исходно (при поступлении) зрение наших пациентов варьировало в чрезвычайно широких пределах — от полной слепоты до тех показателей ОЗ, которые в клинике принято считать нормой.
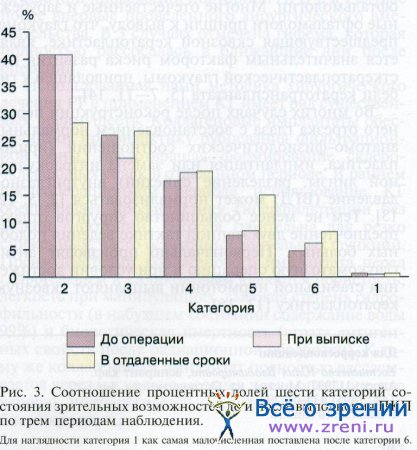
Рассмотрение таких случаев в рамках единого массива данных представляет существенную проблему, так как при потере предметного зрения оценка ОЗ в классическом понимании невозможна и в целом корректно говорить об уровне зрительных возможностей. В силу этого мы решили провести частотный анализ зрительных возможностей, разделив их уровни на 6 категорий: 1 — слепота; 2 — светоощущение; 3 — остаточное зрение (сотые доли); 4 — низкое предметное зрение (от 0,1 до 0,5 по таблице), 5 — субнормальное зрение (от 0,5 до 0,9 по таблице), 6 — нормальное зрение (более 0,9 по таблице). Соотношение процентных долей этих категорий по трем периодам наблюдения представлено на рис. 3.
Число случаев, когда оценка зрительных возможностей вообще и ОЗ в частности в каждый из периодов наблюдения была возможной, составило 380 до операции, 332 при выписке и 241 в отдаленные сроки наблюдения, которые в зависимости от сочетания разных обстоятельств варьировали от 1 мес до 15 лет. В 86% случаев, однако, "отдаленные сроки наблюдений" укладывались в интервал от 3 мес до 3 лет. В результате итоговая оценка зрительных возможностей в подавляющем большинстве случаев приходилась на сроки после замещения БМА для ПКП прозрачной тканью (от 3 до 6 мес).
Как видно, до операции и при выписке основную часть (41,8 и 42,2% соответственно) всех случаев составляют светоощущения. В отдаленные сроки доля этой категории заметно уменьшается (28,6%). Проверка при помощи критерия t? (угловое преобразование Фишера) показала, что уменьшение доли этой категории по отношению к дооперационному уровню и уровню при выписке оказалось статистически высокозначимым (р < 0,001 и р < 0,002 соответственно).
Наряду с этим следует отметить диаметрально противоположную тенденцию для категории 5 (субнормальное зрение). Если до операции и при выписке доля ее составляла 7,6 и 8,7% соответственно, то в отдаленные сроки она увеличивалась почти вдвое — до 15,3%, причем статистически достоверно (р 0,50 соответственно). По остальным категориям заметных и, главное, достоверных изменений долевых соотношений в разные периоды наблюдений не выявлено, в частности доля категории 1 (слепота) постоянно не превышала 1%.
Таким образом, выполнение ПКП приводит к достоверному повышению уровня зрительных возможностей безотносительно ко всем прочим внешним и внутренним факторам. Эта тенденция, однако, заметно проявляется лишь в отдаленные сроки после операции и реализуется, прежде всего, за счет уменьшения доли категории 2 (светоощущения) при явном нарастании доли категорий 5 и 6 (субнормальное и нормальное зрение).
Кроме того, высокая внутригрупповая вариабельность результатов измерения ОЗ по всем срокам наблюдения наводит на мысль о существенной неоднородности группы не только по исходному уровню зрительных возможностей, но и по путям их изменения в разные сроки после операции.
Выявление этих "типологических вариантов" требует применения особых форм анализа данных, что и будет осуществлено в последующих публикациях.
Осложнения после ПКП мы наблюдали в 47 случаях. В 27 случаях это было частичное или полное расплавление БМА. Зависимости лизиса трансплантата от степени воспалительной реакции со стороны роговицы не отмечено, однако при кератитах перед ПКП с применением БМА мы проводили предварительное консервативное противовоспалительное лечение.
При ожогах ПКП желательно было выполнять в экстренном порядке в течение суток с момента ожога или через 1 год после ожога (в период ремиссии ожоговой болезни). Лизис аллопланта в одном случае наблюдался при развитии аллергического конъюнктивита. При хирургическом лечении птеригиума осложнения мы наблюдали в виде рецидива заболевания (12 случаев). Все эти пациенты были прооперированы повторно по описанной методике. В одном случае через 8 мес после повторной операции наступил второй рецидив.
Еще один вид осложнения в виде отторжения трансплантата (4 случая) наблюдали, когда аллоплант был неправильно фиксирован и эпителий врастал под БМА. При этом он выполнял лишь роль биологической повязки и через 10—20 дней отпадал. В 2 случаях наблюдали микроперфорацию роговицы во время расслаивания мутных слоев или при наложении швов.
Для профилактики этого осложнения нежелательно расслаивать роговицу на глубину более чем 2/3 ее толщины. В 2 случаях наблюдали осложнение в виде образования фистулы роговицы на 12-й и 18-й дни после операции; произведено закрытие фистулы аутоконъюнктивальным лоскутом.
Таким образом, БМА для ПКП является одним из пересадочных материалов, альтернативных донорской роговице. Он позволяет иметь достаточное количество трансплантатов в экстренных ситуациях (стихийные бедствия, катастрофы, военные конфликты), сокращает сроки пребывания пациентов в стационаре (экономический эффект) и обеспечивает существенное повышение зрительных возможностей пациента (социальный эффект).
---
Статья из журнала: "Вестник Офтальмологии | Том 127. №1 2011"



Комментариев 0