Использование S-антигена (арестина) для диагностики глазных патологий

Содержание:
Описание
Одним из ключевых белков участников процесса усиления сигнала в зрительной клетке является арестин. Подробно его свойства и роль в механизме деактивации сенсорного сигнала описаны в первых главах настоящей книги. Однако, как оказалось, арестин участвует и в других процессах, протекающих в сетчатке. Еще в 70-е годы прошлого века было установлено, что введение кролику водорастворимой фракции, полученной из сетчатки, индуцирует аутоиммунный увеит. Фактор, вызывающий аутоиммунный увеит, был назван S-антиген. Позже было установлено, что S антиген и арестин это один и тот же белок. Дальнейшие исследования показали, что у многих животных, включая приматов, вызванный S-антигеном экспериментальный увеит по своим клиническим проявлениям и гистологически похож на некоторые формы увеита у людей. Известно, что в индукции этого заболевания ключевую роль играет иммунная Т-система. Это позволяет предположить, что S-антиген играет определенную патогенную роль в индукции увеита. При некоторых формах увеита наблюдался как гуморальный, так и клеточный ответ на S-антиген.
Совместно с МНИИ глазных болезней им. Гельмгольца мы попытались системно подойти к исследованию корреляции между общими и местными иммунными реакциями и различными проявлениями увеита. Искали корреляцию между содержанием S-антител в крови и слезной жидкости у пациентов с клинической формой увеита. В ходе многолетнего исследования был собран большой клинический материал, который позволяет предложить исследование слезной жидкости пациента на наличие S-антител и S-антиге- на как перспективную форму диагностики.
↑ Выявление S-антител в крови и слезной жидкости больных различными формами увеита
В ходе исследования было обследовано 630 пациентов (средний возраст 29,5 лет): 197 мужчин (31%), 257 женщин (41%), 176 подростков (28%). Обследовались пациенты со следующими заболеваниями: двусторонние увеиты (298), односторонние увеиты (332). 928 глаз было обследовано на кератоувеиты (27), переднекамерные увеиты (83), промежуточные увеиты (331), заднекамерные увеиты (78), хориоретиниты (140), панувеиты (287). 450 пациентов обследовались в течение длительного времени (от 6 мес. до 8 лет). В качестве контрольной группы обследовалось 68 здоровых мужчин в возрасте от 10 до 60 лет (средний возраст - 28 лет). Клеточный ответ на S-антиген исследовался в реакции торможения миграции лейкоцитов (TMJ1) в периферической крови в присутствии 20 мг/мл S-антигена. Учитывалось как ингибирование (индекс миграции ИМ меньше 0,8), так и стимулирование (ИМ больше 1,2) реакции.
S-антитела определялись в реакции пассивной гемагглютинации (РПГА). Первичное разведение слезной жидкости составляло 1 : 8, сыворотки крови -1:2.
Для обнаружения S-антител, связанных в иммунный комплекс с S-антигеном в крови (S-ИКК), сыворотку обрабатывали ультразвуком.
Т-субпопуляцию СД4 (хелпер/индуктор) и СД8 (супрессор/цитотоксин) определяли с помощью цитофлуориметра, используя моноклональные антитела ОКТ4 и ОКТ8.
Обследование показало, что наибольший иммунный ответ на антиген наблюдался при увеитах, сопровождавшихся дегенерацией сетчатки.
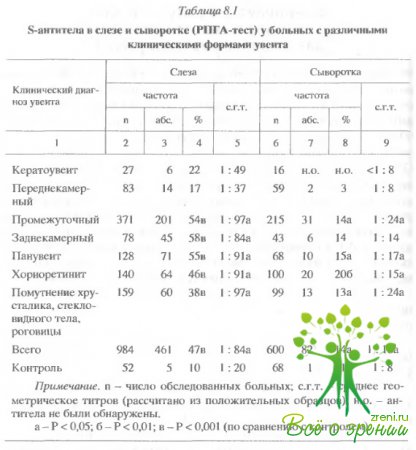
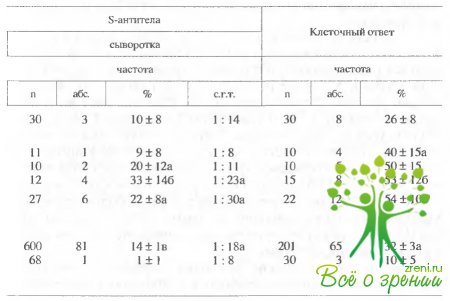
Для кератоувеитов и переднекамерных увеитов наблюдался достаточно слабый ответ (наблюдался редко) (табл. 8.1 и 8.2). В целом S антитела обнаруживались в слезной жидкости значительно чаще (47%), чем в крови (14%). В 25% случаев в крови больных S-антитела находились в виде циркулирующих иммунных комплексов, т.е. в латентной форме.
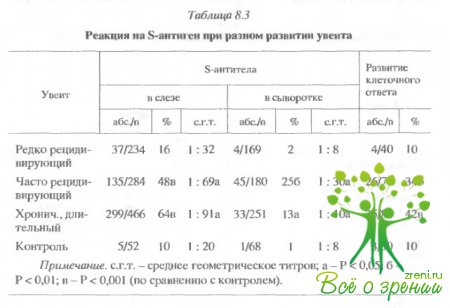
Обследование показало, что реакция на S-антиген обычно значительно сильнее у пациентов с часто рецидивирующими и хроническими формами увеита. Наблюдение в динамике выявило три типа иммунограмм, которые типичны для заболеваний на различных стадиях (табл. 8.3).
Для редко рецидивирующих увеитов с благоприятным прогнозом титр антител в слезе был обычно выше, чем 1 : 256, на начальной стадии заболевания и затем падал до среднего уровня (1 : 32-1 : 128).
В случае подстрой часто рецидивирующей формы относительно высокий гипрантител (выше чем 1 : 256) наблюдался в течение достаточно длительного периода. Низкий титр антител в слезе (меньше 1 : 16) и сильная реакция в крови были типичны для наиболее тяжелых форм с неблагоприятным исходом.
При длительной ремиссии уровень S-антител в слезе достигал 1 : 132-1 : 128 у 75% больных. S-антитела в крови отсутствовали или их уровень приближался к 1 : 16. Клеточный ответ не регистрировался или наблюдалась стимуляция I МЛ, т.е. средняя местная реакция и ослабление реакции в крови.
Положительная реакция на s-антиген при длительной ремиссии отсутствовала. Увеличение титров s-антигел в слезе и/или в сыворотке крови и ингибирование I МЛ происходили за 1-2 недели до появления признаков рецидива увеита.
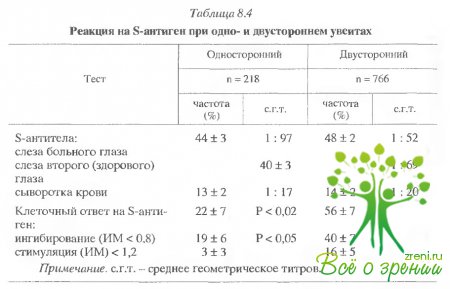
Частота определения s-антител в слезе и их уровень были одинаковы при одно- и двусторонних увеитах, однако клеточный ответ и результаты определения ИКК были типичны для двустороннего увеоретинита (табл. 8.4).
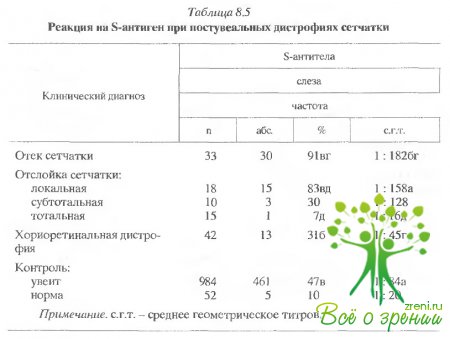
При обследовании больных с постувеальными нарушениями оказалось, что развитие вторичной хориоретинальной дистрофии, отслойка и отек сетчатки коррелируют с иммунным ответом на s-антиген (табл. 8.5). Отек и локальная отслойка сетчатки коррелировали с увеличением титровs-антител в слезе. s-антитела в сыворотке и клеточный ответ регистрировались не всегда, т.е. преобладал местный иммунный ответ. Напротив, общая дистрофия и отслойки сетчатки были связаны с падением титров s-антител в слезе и с увеличением титров в сыворотке и сильным клеточным ответом.
Клеточный ответ на s-антиген (ингибирование ТМЛ), накопление s-антител в слезе и сыворотке могли бы быть свидетельством дистрофии сетчатки при увейте, как это и было продемонстрировано в настоящем исследовании при сравнении больных с тяжелыми формами увеитов и здоровых людей. Положительные реакции на s-антигек также могли бы быть использованы как диагностический тест при помутнении хрусталика, стекловидного тела и роговицы, т.е. когда исследование глазного дна затруднено. Это согласуется с высокой тканеспецифичностью s-антигена. Было высказано предположение, что только s-антиген человека может быть использован для диагностики заболеваний, однако наши данные свидетельствуют о возможности применения для этих целей s-антигена из сетчатки быка, что существенно облегчает задачу.
Нами впервые показано, что при хроническом увейте, отеке сетчатки и ограниченной отслойке сетчатки преобладает местный иммунный ответ. По-видимому, это объясняется локальным выделением иммуноглобулинов и специфических антител в глазу. С другой стопоны, для большинства тяжелых увеитов, хорио-peтинaльныx дистрофий и полной отслойки сетчатки характерны низкие титры или отсутствие s-антител в слезе и усиление как гуморального, так и клеточного ответов в крови. Это означает, что необходимо исследовать как местные, так и системные реакции, непременно включая тестирование слезы.
Средние титры S-антител в слезе (1 : 32-1 : 128; при отсутствии S-антител в сыворотке (1 : 8) и слабый клеточный ответ (стимуляция ТМЛ), по-видимому, связаны с благоприятным прогнозом течения увеита, и это следует рассматривать как нормальную специфическую тканевую реакцию защитного свойства. Нормальный тип такой реакции сочетаемся также с нормальным уровнем иммунорегуляторной субпопулящ.и Т- лимфоцитов крови.
Усиление реакций ь крови, т.е. ингибирпвание ТМЛ, накопление s-антител в сыворотке (больше 1 : 16), циркуляция 8-ИКК отражают генерализацию аутоиммунного процесса. Все это указывает на развитие двустороннего рецидивирующего увеита и постувеальных осложнений.
Наиболее интересно отсутствие S-антител в слезах больных с наиболее тяжелыми симптомами увсоретинитов и хориоретинальных дистрофий. Мы предполагаем, что дефицит антител при заболеваниях сетчатки можно считать парадоксальным состоянием, причиной которого является слабый местный иммунный ответ. Однако необходимо принять во внимание и некоторые другие возможные объяснения: образование специфических иммунных комплексов, антиидиотипические антитела и блокирующие факторы.
Иммунопатологическая важность как роста титров s-антител в слезе или сыворотке, так и дефицита s-антител слезе подтверждается существенным дисбалансом уровня лимфоцитов СД4 и СД8 в крови. Усиление реакций в слезе и сыворотке связано с низким уровнем Т-супрессоров (СД8). Слабый ответ на антиген, по-видимому, вызван дефицитом Т-хелперив (СД4) и увеличением уровня Т-супрессоров. Такое состояние можно определить как состояние общего Т-зависимого иммунодефицита и свидетельство "вязи тканеотецифических реакций (включая и местные реакции; с дисбалансом иммунорегуляторов клеток крови
Таким образом, наличие антител в слезе больных увеитом указывало на наличие сильной аутоиммунной компоненты заболевания. В этом случае применение иммунодепрессантов оказывается очень эффективным.
Действительно, лечение больных с дефицитом s-антител в слезе кортике/стероидами, особенно в комбинации с цитостатиками, было, как правило, неэффективным. Эти наблюдения позволяют понять, почему малоэффективна иммунодепрессивная терапия увеитов.
В целом, как это следует из вышеизложенного, использование такого теста, как определение титра S-антител, оказалось очень эффективным как для определения характера увеита и прогноза течения заболевания, так и для определения метода лечения.
↑ Применение метода выявления S-антител при диагностике и прогнозе развития диабетической ретинопатии
Еще более интересными для перспективы использования выявления 8-антител для диагностики и прогноза глазных патологий представляются результаты исследования больных диабетической ретинопатией Для ранней диагностики ДР применялся как метод выявления антител, так и метод электроретинографии. В данном разделе представлены результаты, полученные при применении иммуно-ферментного анализа (ИФА). В этом случае антитела – иммуноглобулины IgG иIgM– выявлялись в крови и слезной жидкости с использованием античеловеческих антител, конъюгириванных с пероксидазой хрена.
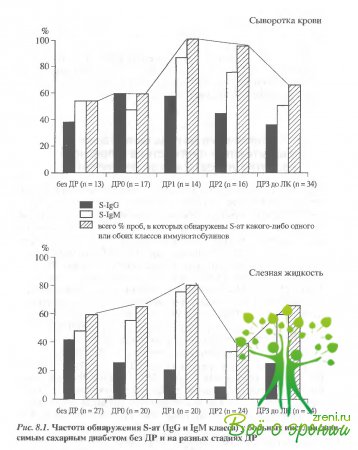
Исследованыs-антителa (S-ат) в сыворотке крови (СК) и слезной жидкости (СЖ) у больных инсулинзависимым сахарным диабетом (ИЗСД) без диабетической ретинопатии (без ДР) на разных стадиях диабетической ретинопатии (ДРО - субклиническая стадия; ДР1 - манифестная стадия, ДР2 - предрофилеративная стадия; Др3 - прелиферативная стадия). Для субклинической стадии характерно то, что явные клинические признаки заболевания еще отсутствуют, однако возможны некоторые изменения в электроретинограмме и ангиограмме. Манифестная стадия - начало заболевания, сопровождающееся появлением клинически выраженных изменений глазного дна; предпролиферативная и пролиферативная стадии сопровождаются тяжелым поражением сетчатки. Результаты исследования представлены на рис. 8.1.
Анализ полученных данных показал, что приблизительно у половины пациентов с ИЗСД гуморальный иммунный ответ на S-АГ как в крови, так и в слезе обнаруживался до развития клинически явных признаков ДР. Пик выявления s-ат ассоциировался с манифестацией ДР: на этой стадии (ДР1) s-ат обнаруживались в 100% проб в сыворотке крови (Р < 0,01 по сравнению с больными без признаков клинически явной ДР) и в 80% проб слезной жидкости. При развитии ДР8-ат обнаруживались в делом реже, чем в период манифестации. Причем, частота их выявления в СК снижалась постепенно, приближаясь на пролиферативной стадии (ДРЗ) к исходным показателям (у больных без ДР). В слезной жидкости минимальное число положительных результатов отмечалось на предпролиферативной стадии - ДР2, стадия пролиферации - ДРЗ характеризовалась возвратным повышением частоты обнаружения s-ат. Надо полагать, что на доклинических стадиях отрицательные результаты свидетельствовали об отсутствии s-аутоиммунизации, тогда как при развитой ДР они могли быть следствием образования специфических иммуноциркулирующих комплексов (ЦИК) или антиидиотипических антител.
Таким образом, выявление s-антител оказывается удобным диагностическим методом именно на тех стадиях заболевания, когда клинические признаки отсутствуют.
Дифференцированный анализ частоты выявления s-атIgGи/или IgMкласса показал, что в отсутствие каких-либо признаков ДР (клинических, функциональных, биохимических - группа "без ДР") оба класса антител выявлялись примерно с одинаковой частотой. При развитии ДР, начиная с манифестной стадии (ДР1) - в сыворотке крови, а в слезе - раньше (ДРО), S-IgМ обнаруживались в обеих пробах примерно на 30% чаще, чем S-IgG, в СЖ в период манифестации - на 56% чаще. Возможно, что явное доминирование s-ат IgМ-класса, особенно в слезе при развитой ДР связано с образованием патологических иммунных комплексов, в состав которых- как известно, чаще входят С-антитела.
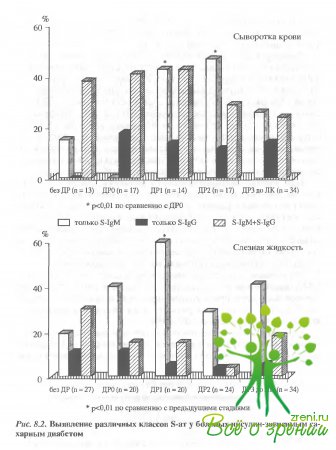
При оценке патогенетического значения каждого из двух классов s-ат был проведен анализ их сочетанного или селективного накопления в разных группах больных (рис. 8.2). У пациентов "без признаков ДР" в сыворотке крови отмечался селективный синтез только S-IgM-ат (15%), что, вероятно, отражало первичность аутоиммунного ответа на S-АГ.
Функциональная стадия (ДРО) характеризовалась селективным накоплением только S-IgG, что, возможно, указывало на стабилизацию процесса.
На манифестной стадии вновь преобладают антитела класса IgМ. Аналогичная тенденция была отмечена и при исследовании слезной жидкости, причем, доминирование селективной продукции S-IgМ-ат проявлялось раньше, чем в сыворотке крови (уже на функциональной стадии ДР-ДРО).
Одновременное накопление s-ат обоих классов было обнаружено и при исследования внутриглазных жидкостей (ВПК), полученных во время операций по поводу отслойки сетчатки у больных с ДРЗ (табл. 8.6). В стекловидном геле - в 100% и в субретинальной жидкости (СРЖ) - в 87,5% проб выявлялись S-IgG. S-IgМ были обнаружены у половины пациентов в СРЖ и в 13% случаев в стеклосидном теле. Следует отметить, что и в СРЖ и в СТ.Т. выявлялись достоверно чаше (100%), чем в пробах СЖ (24%; Р < 0,01) и СК (35%; I < 0,01); тогда как IgМ в СРЖ - примерно с той же частотой, а в СТ.Т. реже, чем в СК и СЖ.
Неблагоприятная роль аутоиммунизации S-антигеном была подтверждена и при исследовании пациентов с различными исходами лазеркоагуляции (ЛК)
Использование метода обнаружения s-антител оказалось удобным и для прогноза результатов оперативного лечения ДР методом лазеркоагуляции (ЛК).
Анализ показал, что неизменные показатели S-ат наблюдались при благоприятном течении послеоперационного периода; в случае дальнейшего прогрессирования ДРЗ после ЛК сетчатки s-ат обоих классов как в крови, так и е слезе наблюдались значительно чаще, причем, наиболее значимым показа гелем явилось одновременное накопление S-IgG иS-IgМ антител. Эти данные
согласовались и с результатами индивидуального анализа. Так, из 14 пациентов, обследованных в динамике до и после ЛК, у 8 человек с успешным исходом лечения существенных сдвигов в характере местного и/или системного иммунного ответа на S-АГ после ЛК не отмечалось. У 6 пациентов с осложнениями после ЛК наблюдалось двукратное усиление синтеза S-ат обоих классов как в СК. гак и в СЖ
Таким образом, обнаружение s-антител различного класса оказалось удобным прогностическим признаком как при ранней диагностике диабетической ретинопатии, так и при прогнозе результата лечения.
↑ Иммуноферментный метод и набор реагентов для определения антител к S-антигену сетчатки глаза в сыворотке крови человека
Опираясь на изложенные выше результаты, нами был разработан метод и набор реагентов для определения антител к S-антигену сетчатки глаза в сыворотке крови человека методом иммуноферментного анализа для:
- ранней диагностики вовлечения в патологический процесс сетчатки глаза;
- диагностики поражений сетчатки у больных с помутнениями оптических сред глаза, когда офтальмоскопия глазного дна невозможна или затруднена (катаракта, бельма, помутнение стекловидного тела);
- диагностики и прогнозирования течения аутоиммунных увеитов;
- прогнозирования развития и прогрессирования диабетической ретинопатии;
- прогнозирования осложнении и быстрого прогрессирования близорукости.
Метод и набор прошли все необходимые технические и медицинские испытания и рекомендован к широкому применению МЗ РФ.
В обоих случаях критерием обнаружения иммуноглобулиноз в (IgG) или иммуноглобулинов М (IgM) служила разность оптической плотности сыворотки крови нормальных доноров и исследуемой сыворотки при исследовании их методом иммуноферментного анализа. Если эта разность превышала 0,2, то присутствие IgGили IgМ считалось установленным.
Испытание набора показало, что наиболее интересные и значимые для широкого применения результаты получены при исследовании больных монолатеральными увеитами и диабетической ретинопатией. При исследовании более 130 больных было установлено, что обнаружение в крови больных одновременно обоих иммуноглобулинов свидетельствовало о скором вовлечении в патологический процесс второго глаза. Так, при обследовании 130 больных монолатеральным увеитом у 34 в крови были обнаружены одновременно IgG и IgM. У 32 больных в течение полугода при офтальмоскопии было отмечено начало воспаления на втором глазу.
Разработанный нами метод позволяет объективно предсказать переход монолатерального увеита в билатеральный.
При исследовании больных диабетической ретинопатией было установлено, что обнаружение в крови больных иммуноглобулинов обоих типов обычно коррелировало с резким обострением патологического процесса и таким образом явилось дополнительным диагностическим критерием наряду с ангиографией и офтальмоскопией.
В ряде случаев один из иммуноглобулинов обнаруживался в крови больных диабетической ретинопатией (ДР) на самой ранней стадии заболевания. Мы установили, что обнаружение одного из иммуноглобулинов IgG или IgМ в крови больных диабетом без видимой глазной патологии свидетельствовало о скором появлении признаков заболевания ДР. Так, нами было обследовано 140 больных инсулин-зависимым сахарным диабетом в течение 3 лет. У 34 в крови были обнаружены IgG или IgM. Пои последующем наблюдении у 32 больных были от мечены признаки ДР при офтальмоскопии или ангиографии.
Таким образом, обнаружение антител к s-антигену в крови больных диабетом оказалось объективным прогностическим критерием скорого наступления глазной патологии. Использование метода позволяет выявить группу риска глазных осложнений среди больных диабетом, что позволяет как проводить профилактику, так и своевременно начать лечение.
Статья из книги: Молекулярные механизмы зрительной рецепции | Каламкаров Г.Р., Островский М.А..




Комментариев 0