Болезнь Гиппеля и Гиппеля — Линдау

Описание
Болезнь Гиппеля — Линдау — наследственное мультисистемное заболевание, характеризующееся развитием кистоза и новообразований в различных органах. Заболевание впервые описано A.Z.Fuchs в 1882 г. В 1904 г. Е. von Hippel опубликовал результаты гистологических исследований глаза пациента с гемангиомами сетчатки. Спустя немногим более 20 лет невропатолог A.Lindau (1926) сообщил о результатах морфологических исследований головного мозга и органов брюшной полости больных с ангиоматозом сетчатки и впервые высказал предположение, что существует связь между поражениями глаз и центральной нервной системы. Благодаря работам этих авторов в литературе были представлены наиболее часто наблюдающиеся проявления заболевания. Другие органы поражаются значительно реже.Таким образом, диагноз «болезнь Гиппеля» устанавливают в том случае, если в ходе мультисистемного обследования пациента обнаружены только ретинальные поражения и нет анамнестических сведений о наличии у него близких родственников, у которых были бы гемангиобластома центральной нервной системы, кистоз почек или аденокарцинома и тд. Более чем у 25 % пациентов с ангиоматозом сетчатки имеются различные новообразования центральной нервной системы или внутренних органов. В этом случае заболевание обозначают эпонимом «болезнь Гиппеля — Линдау».
Эпидемиология и генетические исследования. Заболевание наследуется по аутосомно-доминантному типу с неполной пенетрантностью. Спорадические случаи составляют около 20 %. Ген, ответственный за развитие болезни Гиппеля — Линдау, картирован на 3-й хромосоме в интервале Зр26—р25. Частота развития заболевания в популяции приблизительно 1 : 36 000.
Диагностические критерии болезни Гиппеля - Линдау
Болезнь Гиппеля — Линдау может быть диагностирована при наличии не менее одного из перечисленных ниже симптомов у пациента, в семье которого хотя бы один из членов имел гемангиобластому центральной нервной системы или сетчатки, кистоз почек и/или аденокарциному:
- гемангиобластома мозжечка или других отделов головного мозга, а также спинного или костного мозга;
- гемангиобластома сетчатки;
- кистоз почек или почечная аденокарцинома;
- кисты поджелудочной железы, цистаденокарцинома или незвдиобла-сгоматш (?-клеточные опухоли);
- феохромоцитома;
- эпвдидимальная аденома.
Системные проявления и диагностические критерии. Ангиоматоз сетчатки выявляют примерно у 55—70 % пациентов с болезнью Гиппеля — Линдау, гемангиобластомы ЦНС — по крайней мере у 60 %, кисты почек и поджелудочной железы — у 33—54 %, феохромоцитому— у 7 %. Установлено, что средний возраст пациентов в момент появления гемангиобластомы сетчатки составляет около 18 лет (варьирует от 2,8 года до 67 лет), гемангиобластомы центральной нервной системы — 42 года (от 4 до 70 лет), почечной клеточной карциномы — 43 года (от 31 года до 69 лет) и феохромоцитомы — 25 лет (от 10 до 56 лет).
[banner_centerrs] {banner_centerrs} [/banner_centerrs]
Висцеральные поражения могут предшествовать изменениям заднего отрезка глаз. G.Browne и соавт. (1997) сообщили о 8 пациентах с болезнью Гиппеля — Линдау из трех поколений большой ирландской семьи, у которых единствен¬ным проявлением заболевания был поликистоз почек. Диагноз у этих больных был установлен путем идентификации мутации в локусе Зр25— р26 в холе анализа ДНК. B.U.Bender и соавт. (1997) описали двух пациентов, у которых болезнь Гиппеля — Линдау была верифицирована с помощью молекулярных генетических исследований. Единственным проявлением заболевания у этих больных была феохромоцитома.
Офтальмологические проявления. У большинства детей заболевание обнаруживают при обследовании по поводу косоглазия или диспансерном осмотре. Раннее выявление изменений на глазном дне возможно также в ходе профилактического осмотра детей, чьи родители или близкие родственники страдают болезнью Гиппеля — Лицдау. Пациенты старше 8 лет обычно предъявляют жалобы на затуманивание зрения или метаморфопсии.
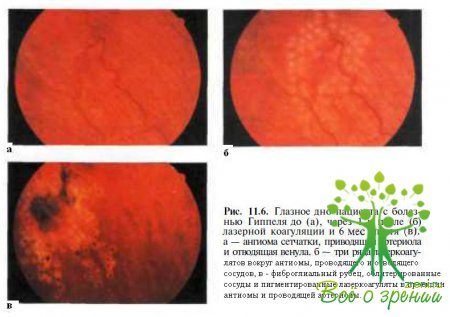
В ранних стадиях заболевания при офтальмоскопии может быть выявлено лишь аневризмоподобное расширение сосуда на периферии сетчатки. Позднее новообразование выглядит как маленькая ( около 0,3 ДР в диаметре) розовая, слегка проминирующая ткань (рис. 11.6)
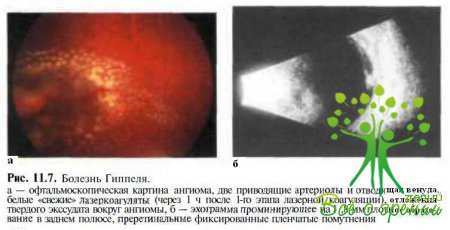
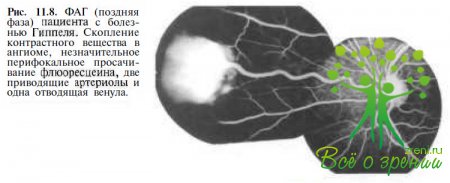
С опухолью связаны измененные сосуды: расширенная извитая приводящая артериола и дренирующая венула. Рядом, как правило, определяют развивающиеся в большинстве случаев артериовенозные шунты. Чаще ангиомы локализуются на средней периферии (более 90 % больных), но могут располагаться в любом месте сетчатки, в том числе юкстапапиллярно (около 8 %) или в заднем полюсе (приблизительно 1 %). Вследствие повышенной проницаемости капилляров опухоли вокруг ангиомы накапливается суб- и интраретинальный экссудат, содержащий липиды (рис. 11.7; 11.8).
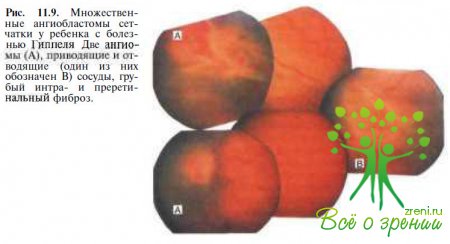
Размеры ангиом широко варьируют, в некоторых случаях они достигают 4—7 РД. На одном глазу могут быть несколько ангиом (рис. 11.9). В 50 % случаев поражаются оба глаза.
В поздних стадиях болезни развиваются экссудативная отслойка сетчатки, интра- и субретинальная фиброглиальная пролиферация, субретинальная неоваскуляризация (см. рис. 11.9;рис. 11.10),
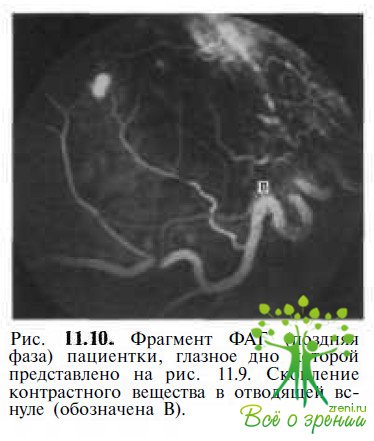
периферические и/или макулярные разрывы сетчатки, неоваскулярная глаукома. Описан случай, когда у пациентки с длительно (более 17 лет) существовавшей ангиомой развилась оссификация структур заднего отрезка глаза.
A.Fergusson и J.Singh (2002) обследовали 14-летнюю девочку с болезнью Гиппеля — Линдау, у которой первым проявлением заболевания была тотальная экссудативная отслойка сетчатки. При В-эхографии и КТ не было выявлено признаков ангиомы сетчатки. Диагноз был подтвержден при анализе семейного анамнеза и молекулярном генетическом обследовании девочки и 9 членов ее семьи (обнаружена мутаиия рамки считывания в 195-м ко- доне 3-го экзона гена болезни Гиппеля - Линдау).
Флюоресцентная ангиографии. В артериовенозной фазе отмечается накопление контрастного вещества ангиомой. В поздней фазе — повышенная проницаемость флюоресцеина, обусловленная неполноценностью стенок сосудов опухоли (см. рис. 11.7; 11.9; 11.10).
Лечение. В связи с прогрессирующим характером течения болезнь Гиппеля — Линдау представляет постоянную угрозу для пациентов. При отсутствии лечения поражение глаз почти во всех случаях приводит к слепоте, а нарушения со стороны центральной нервной системы и внутренних органов — к инвалидизации или даже летальному исходу.
Хирургическое лечение при гемангиобластоме центральной нервной системы дает оптимальные результаты в ранних стадиях заболевания. Полностью удалить гемангиобластому центральной нервной системы удается приблизительно у 90 % больных. У 7 % успешно оперированных больных опухоль рецидивирует в среднем в течение 5,7 года.
Основная цель лечения пациентов с ангиомой (или ангиомами) сетчатки — предотвратить развитие экссудативных ретинальных осложнений, приводящих к потере зрения. В связи с этим лечение пациентов с болезнью Гиппеля — Линдау необходимо начинать как можно раньше, так как терапия опухолей больших размеров малоэффективна.
При ангиомах сетчатки, диаметр которых не превышает 2,5 РД, обычно проводят лазерную коагуляцию. Наиболее часто с этой целью используют аргоновый зеленый и голубой-зеленый, неодим:ИАГ зеленый и криптоновый желтый лазеры. Экспозиция составляет 0,2—1,0 с, диаметр коагулятов — 200—500 мкм, мощность — 200— 800 мВт. При маленьких ангиомах наиболее эффективна прямая коагуляция опухоли, которую, как правило, проводят в несколько сеансов, чтобы избежать развития вторичной экссудативной отслойки сетчатки.
Как показывает наш опыт, при ангиомах, диаметр которых больше 3 мм, более эффективна лазерная коагуляция в виде последовательных серий: на первом этапе проводится барьерная коагуляция вокруг тела опухоли и питающих ее сосудов (см. рис. 11.6; 11.7), на втором — коагуляция приводящей артериолы, на третьем — коагуляция ангиомы в ходе нескольких сеансов. Приводящую артериолу необходимо коагулировать до полной облитерации се сегмента, когда становится невозможным спонтанное приоткрывание сосуда и восстановление кровотока по нему. Искусственно создаваемая в ходе лазерной коагуляции внутриглазная гипертензия снижает кровоток в артериолах и способствует облитерации питающих сосудов. Лечение необходимо повторять через каждые 2—8 нед до тех пор, пока не прекратится перфузия ангиомы. По мнению J.S.Shields (1994), после полной облитерации приводящих сосудов целесообразна коагуляция дренирующих вен.
При ангиомах юкстапапиллярной локализации разрушение опухоли, как правило, сопровождается выраженным снижением зрения, в частности, из-за непосредственного повреждения диска зрительного нерва в ходе лазерной коагуляции. В связи с этим некоторым больным с крупными юкстапапиллярными янгномами проводят только барьерную лазерную коагуляцию, позволяющую предотвратить или хотя бы отсрочить развитие экссудативной отслойки сетчатки в макуле. Коагуляты наносят в 2—3 ряда вдоль тела опухоли и приводящих сосудов. Параметры барьерной коагуляции: экспозиция 0,2—0,5 с, диаметр коагулятов 200—500 мкм, мощность 100—300 мВт.
Криотерапия эффективна как при ангиомах небольшого размера, так и при опухолях, диаметр которых составляет 2,5-3,0 РД. Кроме того, трансеклеральную криодеструкцию ангиом осуществляют в тех случаях, когда использовать лазеры невозможно (например, при нарушении прозрачности хрусталика или стекловидного тела). Сеанс криотерапии проводят в 2—3 приема по принципу «замораживание — размораживание». Температура рабочего наконечника достигает 80 ?С, экспозиция варьирует в зависимости от размеров опухоли. В некоторых случаях (при размерах ангиомы 3-4 РД) целесообразно комбинированное лечение — лазерная коагуляция в сочетании с криотерапией.
При неэффективности лазерной коагуляции и/или криотерапии у пациентов с ангиомами, размеры которых превышают 4 РД, может быть выполнена диатермия, которую иногда дополняют экстрасклеральным пломбированием.
G.A.Peyman и соавт. (1983) сообщили об успешном удалении ангиом, превышающих в диаметре 3 РД, у двух пациентов методом транссклеральной резекции.
Новые капиллярные ангиомы развиваются при болезни Гиппеля — Линдау приблизительно в 13 % глаз в среднем через 16 мес (3—235 мес). Наиболее часто они локализуются в верхневисочном квадранте.
При ведении пациентов с болезнью Гиппеля — Линдау или их детей необходимо выполнять следующие условия:
- информировать пациентов о возможных проявлениях и характере течения болезни;
- проводить офтальмологическое обследование пациентов каждые 6— 12 мес;
- периодически исследовать содержание катсхоламиноб в моче для исключения феохромоиитомы; повторять исследование в случае колебаний артернлльного давлении:
- больным старше 15 лет периодически проводить двустороннюю селективную ренальную ангиографию;
- всем пациентам в возрасте 13— 50 лет регулярно (приблизительно 1 раз в 3 года) проводить МРТ головного и спинного мозга;
- периодически (приблизительно каждые 3 года) проводить ультразвуковое исследование и КТ почек и органов брюшной полости; повторять ультразвуковые и нейрорадиологические исследования во всех случаях, когда появляется симптоматика, позволяющая предполагать поражение этих структур;
- проводить ДНК-анализ крови и ткани удаленных опухолей.
Статья из книги: Зрительные функции и их коррекция у детей | С.Э. Аветисов, Т.П. Кащенко, А.М. Шамшинова.


Комментариев 0