Врожденные глаукомы (Часть 2) | Руководство по детской офтальмологии

Описание
Но состоянию внутриглазного давления различают компенсированную, некомпенсированную и декомпенсированную врожденную глаукому.
При компенсированной глаукоме внутриглазное давление не превышает 26 мм рт. ст. в начальной стадии и 24 мм рт. ст. в более поздних стадиях заболевания; суточные колебания офтальмотонуса находятся в пределах 5 мм рт. ст.
Некомпенсированная глаукома характеризуется внутриглазным давлением выше 26 мм рт. ст. в начальной стадии заболевания и выше 24 мм рт. ст. в более поздних стадиях; размах «суточных колебаний более 5 мм рт. ст. Признаками некомпенси¬рованной глаукомы являются отек роговицы, застойная инъекция, изменения состояния передних ресничных сосудов в склеролимбальной зоне, свидетельствующие о затруднении тока крови (симптомы кобры, медузы, эмиссария).
Декомпепсированная глаукома — острый приступ.
В зависимости от динамики процесса различают стабильную, врожденную глаукому, характеризующуюся тем, что прекращаются увеличение глазного яблока и снижение зрительных функций, и прогрессирующую, при которой наблюдается дальнейшее увеличение глазного яблока, нарастание патологических симптомов, снижение зрительных функций.
По состоянию радужно-роговичного угла различают глаукому с наличием эмбриональной мезодермальной ткани, передним прикреплением радужки, отсутствием дифференцировки трабекул.
Значение классификации заключается в том, что определение формы врожденной глаукомы позволяет наметить план лечения, степень компенсации и динамики процесса - определить показания к операции и сроки ее выполнения, стадии процесса и состояния угла передней камеры — выбрать патогенетически обоснованное хирургическое вмешательство.
Диагноз и дифференциальный диагноз. Диагноз врожденной глаукомы устанавливают на основании анамнеза и результатов обследования, включающего наружный осмотр, кератометрию, биомикроскопию, гониоскопию, гониоскопию с корнеокомпрессией, офтальмоскопию, тонометрию, тонографию, исследование зрительных функций.
Важное значение имеет ультразвуковая биометрия как метод диагностики врожденной глаукомы и контроля эффективности лечения и стабилизации процесса по изменениям длины сагиттальной оси глаза и глубины передней камеры. Исследование органа зрения у детей младшего возраста (до 3—5 лет) проводят в условиях углубленного физиологического или наркотического сна.
При наличии выраженных характерных, признаков: увеличения глазного яблока и диаметра роговицы, растяжения лимба, разрывов задней пограничной пластинки, глубокой передней камеры, повышения внутриглазного давления, глаукоматозной экскавации диска зрительного нерва, диагностика врожденной глаукомы, как правило, не вызывает больших затруднений.
Значительные трудности в диагностике могут возникать в начальной стадии врожденной глаукомы, когда характерная симптоматика заболевания отсутствует или слабо выражена. В этих случаях внимание должно быть сосредоточено на выявлении ранних признаков заболевания.
Важное значение в раннем выявлении врожденной глаукомы имеет осмотр глаз у каждого новорожднного в родильных домах акушером и педиатром, которые должны знать начальные признаки заболевания. При подозрении на глаукому ребенка направляют на консультацию к офтальмологу, а при подтверждении диагноза проводят соответствующее лечение.
Врожденную глаукому следует дифференцировать от заболеваний глаз, при которых наблюдаются отдельные симптомы, характерные для глаукомы: конъюнктивита, кератита, дистрофии роговой оболочки, мегалокорнеа, кератоконуса, кератоглобуса, врожденной близорукости высокой степени, ретинобластомы.
Наблюдающиеся при врожденной глаукоме светобоязнь, блефароспазм, слезотечение характерны и для конъюнктивита, что может явиться причиной диагностических ошибок. Однако при конъюнктивите отмечаются обильное отделяемое и конъюнктивальная инъекция. При конъюнктивите роговица, как правило, гладкая, прозрачная и блестящая, а при глаукоме она чаще матовая вследствие отека.
Кератиты различной этиологии (паренхиматозный, герпетический и др.) могут симулировать врожденную глаукому в связи с наличием сходных признаков - - светобоязни, слезотечения, блефароспазма, помутнения роговицы. Однако при кератите наблюдаются перикорнеальная инъекция, васкуляризация лимба и роговицы, в процесс вовлекаются радужка н ресничное тело, суживается зрачок. В то же время у больных с кератитами отсутствуют такие характерные для глаукомы симптомы, как увеличение глазного яблока, повышение офтальмотоиуса и др.
[banner_centerrs] {banner_centerrs} [/banner_centerrs]
Относительно редко встречающаяся патология, которая может быть принята за врожденную глаукому, — врожденная наследственная дистрофия роговицы. Поражение обычно двустороннее и проявляется диффузным отеком и помутнением оболочки различной степени выраженности от легкого до густо-белого с вовлечением стромы.
Светобоязнь, увеличение глазного яблока и роговицы отсутствуют, внутриглазное давление нормальное. При наследственной эпителиальной дистрофии роговицы имеются мелкие точечные помутнения под эпителием, впереди передней пограничной пластинки (боуменова оболочка), более многочисленные в центре.
Помутнения роговицы, светобоязнь, появляющиеся, как правило, на 3—6-м месяце жизни, могут наблюдаться при таких системных заболеваниях, как липоидоз и цистиноз. Помутнения роговицы обусловлены отложением в ней липидов в первом случае и цистина во втором. Внутриглазное давление нормальное, характерные признаки врожденной глаукомы отсутствуют, что позволяет установить правильный диагноз.
Врожденную глаукому необходимо дифференцировать от мегалокорнеа. Эта относительно редко встречающаяся патология имеет ряд общих с гидрофтальмом симптомов: увеличение диаметра роговицы, который может достигать 13 —16 мм, глубокая передняя камера, гипоплазия радужки, иногда иридодонез.
Однако при мегалокорнеа отсутствуют другие признаки врожденной глаукомы, такие, как увеличение аксиальной оси глазного яблока, отек и помутнение роговицы, разрывы задней пограничной пластинки, повышение внутриглазного давления, экскавация и атрофия диска зрительного нерва.
Дифференциальная диагностика между врожденной глаукомой, кератоглобусом и кератоконусом обычно не вызывает затруднений. При кератоглобусе роговица увеличена, имеет форму полушария, истончена, особенно у лимба, передняя камера глубокая. При наличии этих признаков необходимо дифференцировать кератоглобус от гидрофтальма. Отсутствие других симптомов врожденной глаукомы и нормальное внутриглазное давление позволяют отличить кератоглобус от гидрофтальма.
Кератоконус характеризуется конусовидной формой роговицы и ее помутнением в области вершины конуса. Сходство с врожденной глаукомой заключается в наличии глубокой передней камеры. Однако характерная форма роговицы и отсутствие других симптомов гидрофтальма позволяют отличить кератоконус от врожденной глаукомы. Следует иметь в виду, что кератоконус проявляется чаще всего в возрасте 9—20 лет, а у детей младшего возраста встречается редко.
Гидрофтальм необходимо дифференцировать от врожденной близорукости высокой степени. Общим признаком этих заболеваний является увеличение глазного яблока. Однако для ранних стадий врожденной глаукомы характерно увеличение переднего отрезка глаза, в то время как для высокой миопии заднего. Другие признаки гидрофтальма при близорукости отсутствуют, внутриглазное давление нормальное, отмечаются характерные для миопии изменения глазного дна.
Следует иметь в виду, что наблюдавшаяся при гидрофтальме миопическая рефракция никогда не достигает высокой степени.
Увеличение глазного яблока и роговицы с наличием помутнений в глубоких слоях, чаще у лимба, могут наблюдаться при мукополисахаридозах. Заболевание проявляется уже у новорожденных и детей младшего возраста. В отличие от врожденных глауком внутриглазное давление нормальное, конъюнктива век и глазного яблока отечная и цианотичная, сосуды лимбальной области расширены и врастают в роговицу, на глазном дне часто отмечаются явления застоя с исходом в атрофию зрительного нерва.
Наличие этих признаков, а также общих проявлений системного поражения (деформация черепа, уродливые черты лица, широкий седлообразный нос, толстые губы, большой язык, дорсолюмбальный кифоз, тугоподвижность суставов, гепатоспленомегалия, пупочная и паховые грыжи и др.) позволяют дифференцировать заболевание от врожденных глауком. Установить правильный диагноз помогают биохимические исследования: экскреция кислых гликозаминогликанов увеличена в десятки раз по сравнению с нормой.
Гидрофтальм следует дифференцировать от вторичной глаукомы, развивающейся при ретинобластоме. Общими признаками этих заболеваний являются увеличение глазного яблока, отек роговицы, мидриаз, повышенное внутриглазное давление. Однако передняя камера при ретинобластоме чаще нормальная или мелкая, а при биомикроскопии и офтальмоскопии в стекловидном теле и на глазном дне выявляются характерные для опухоли изменения.
Результаты эхобиометрии и других исследований позволяют подтвердить или исключить наличие тумора. Следует иметь в виду, что в стадиях ретинобластомы, при которых развивается вторичная глаукома, могут наблюдаться изменения в переднем отрезке глаза - узелки опухоли в радужке, псевдогипопион и др.
Буфтальм у детей младшего возраста может развиваться при вторичной посттравматической и посгвоспалительной глаукоме. Дифференциальная диагностика с врожденной глаукомой в этих случаях обычно не вызывает затруднений и основывается на данных анамнеза, а также наличии признаков перенесенной травмы или воспалительного процесса.
Лечение. В связи с наличием препятствий оттоку внутриглазной жидкости лечение врожденных глауком хирургическое. Медикаментозная терапия является дополнением к операции.
Хирургическое лечение. Хирургическое вмешательство при врожденных глаукомах производят незамедлительно по установлении диагноза после проведенного в срочном порядке обследования ребенка в качестве подготовки к стационированию, проведения наркоза и операции. Следует иметь в виду, что возрастных противопоказаний к операции у детей с врожденными глаукомами нет. Чем раньше произведено хирургическое вмешательство, тем на больший эффект его можно рассчитывать.
В тех случаях, когда нормализация внутриглазного давления не достигнута или через какое-то время после эффективного хирургического лечения офтальмотонус повысился, требуется срочная повторная операция. Особое значение имеет своевременная повторная операция у детей младшего возраста, у которых под влиянием повышенного внутриглазного давления процесс быстро прогрессирует, увеличивается глазное яблоко.
На первых этапах хирургического лечения врожденных глауком применяли операции, использовавшиеся при первичной глаукоме взрослых (корнеосклеральная трепанация по Эллиоту, ириденклейзис и др.). Эти операции были малоэффективными и нередко приводили к осложнениям, в связи с чем их перестали применять. Начиная с 1936 г., когда Баркан ввел гониотомию — фактически первое микрохирургическое вмешательство, результаты лечения врожденных глауком существенно улучшились.
В 1952 г. Шайе предложил гониопунктуру, которую, как правило, используют не как самостоятельную операцию, а в сочетании с гониотомией. В последние годы в хирургии врожденных глауком широко применяют операции, которые производят при первичной глаукоме по предложению М. М. Краснова, А. П. Нестерова и др. Из этих хирургических вмешательств наиболее часто выполняют трабекулотомию, трабекулэктомию (синусотрабекулэктомия, секторная синусэктомия, трабекулканалэктомия), иридоциклоретракцию и др.
Перспективна лазерная гониопунктура — образование отверстия в трабекулярной зоне и вскрытие венозного синуса склеры путем лазерного воздействия с помощью модулированных («холодных») лазеров.
Современные операции при врожденных глаукомах производят под операционным микроскопом микрохирургическим инструментарием.
Современные операции при врожденных глаукомах производят под операционным микроскопом микрохирургическим инструментарием.
Специальные инструменты требуются для выполнения гониотомии, гониопунктуры (гониотом) и трабекулотомии (трабекулотом). Для разрезов используют осколок лезвия бритвы, укрепленный в лезвиедержателе. Используют микроиглы и шовный материал 8: 0 и 10: 0. При осуществлении многих операций требуется гониоскопический контроль.
Проекцию вершины угла передней камеры на склеру определяют с помощью диафакоскопии или гониоскопии в сочетании с вдавливанием склеры в области лимба. Хирургическое вмешательство производят при максимально сниженном внутриглазном давлении. С этой целью за несколько дней до операции назначают диакарб или глицерол.
Принципом хирургического лечения врожденных глауком является применение патогенетически обоснованных микрохирургических операций с учетом механизма повышения внутриглазного давления. Успех хирургического лечения врожденной глаукомы во многом определяется правильным выбором операции в зависимости от стадии заболевания и характера патологических изменений угла передней камеры, выявленных при гониоскопическом исследовании.
В ранних стадиях заболевания (начальная и развитая) производят операции, направленные на восстановление естественных путей оттока внутриглазной жидкости, или комбинируют их с хирургическими вмешательствами, цель которых создание дополнительных путей оттока.
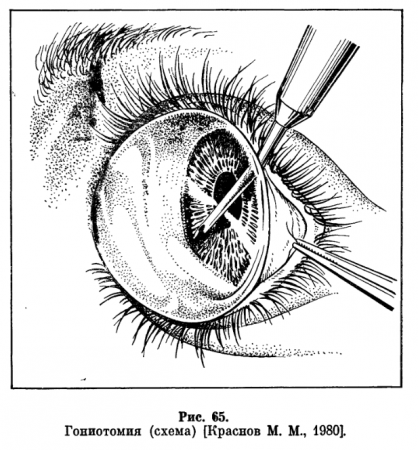
При наличии в углу передней камеры мезодермальной ткани патогенетически обоснованным хирургическим вмешательством является гониотомия (рис. 65). Сущность операции состоит в устранении претрабекулярного препятствия - удалении (соскабливание, рассечение) мезодермальной ткани, освобождение трабекулярной зоны и восстановление оттока внутриглазной жидкости через склеральный синус.
Гониотомию рекомендуют производить в начальной стадии заболевания, в развитой стадии более эффективным вмешательством является гониотомия в сочетании с гониопунктурой. Гониопунктуру нельзя считать патогенетически обоснованной операцией при врожденной глаукоме, так как с ее помощью не восстанавливают естественные пути оттока, как при гониотомии, а создают новые. Однако по клиническому применению и технике выполнения гониопунктура близка к гониотомии.
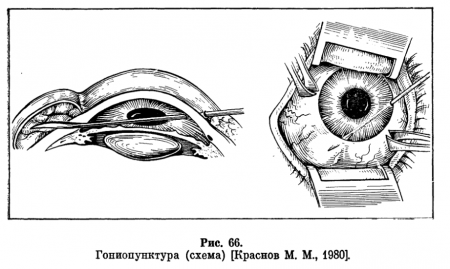
Суть гониопунктуры (рис. 66) заключается в создании фистулы для субконъюнктивальной фильтрации. Гониопунктура позволяет увеличить эффект гониотомии, что особенно важно в выраженной стадии глаукомы, при которой уже могут наблюдаться вторичные изменения путей оттока. Как самостоятельную операцию гониопунктуру применяют редко.
Гониотомию и гониопунктуру производят под контролем операционной гониолинзы специальным инструментом — гониотомом. Наиболее целесообразно применять канюлированный гониотом, позволяющий благодаря введению изотонического раствора натрия хлорида углублять переднюю камеру и поддерживать глубину ее постоянной в течение всей операции.
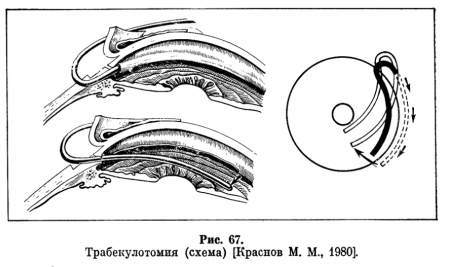
При наличии эмбриональной мезодермальной ткани в углу передней камеры как в начальной, так и в развитой стадии заболевания методом выбора может быть трабекулотомия. Операция состоит во вскрытии внутренней стенки склерального синуса с одновременным разрушением эмбриональной ткани специальным инструментом - трабекулотомом (рис. 67). В результате этого освобождается доступ камерной влаги в склеральный синус. Преимуществом трабекулотомии перед гониотомией является возможность выполнения ее при непрозрачной роговице.
В тех случаях, когда при гониоскопическом исследовании выявлено переднее прикрепление радужки, корень которой частично или полностью прикрывает фильтрационную зону, в начальной стадии целесообразно произвести гониотомию.
Эффект гониотомии в этих случаях обусловлен освобождением трабекулярной зоны в связи с оттеснением корня радужки, а также соскабливанием эмбриональной ткани, если ее при этом обнаруживают.
В начальной стадии методом выбора может быть трабекулотомия. В развитой стадии показаны гониотомия с гониопунктурой или иридоциклоретракция по Краснову.
При отсутствии в углу передней камеры мезодермальной ткани и переднего прикрепления радужки, когда при гониоскопическом исследовании выявляется недостаточная дифференцировка трабекулы, в начальной стадии заболевания наиболее показана трабекулотомия, в развитой методами выбора могут быть трабекулотомия и трабекулэктомия.
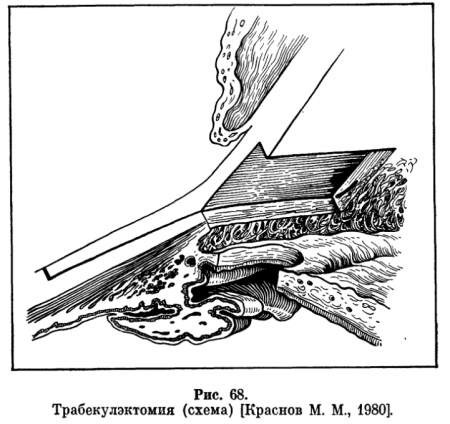
Принцип операции заключается в иссечении под склеральным лоскутом небольшого участка трабекулы и венозного синуса склеры (рис. 68). В результате этого дополнительный отток водянистой влаги происходит через перерезанные концы венозного синуса склеры по дренажной системе глаза и через фистулу и у краев склерального лоскута в субконъюнктивальное пространство. Предложен ряд модификаций этих операций (М. М. Краснов, А. П. Нестеров и др.).
В поздних стадиях глаукомы (далеко зашедшая, почти абсолютная и абсолютная) показаны операции, направленные на создание новых путей оттока внутриглазной жидкости. Восстановить естественные пути оттока в этих стадиях не представляется возможным из-за выраженных вторичных изменений, которые возникают в связи с увеличением глаза и растяжением оболочек.
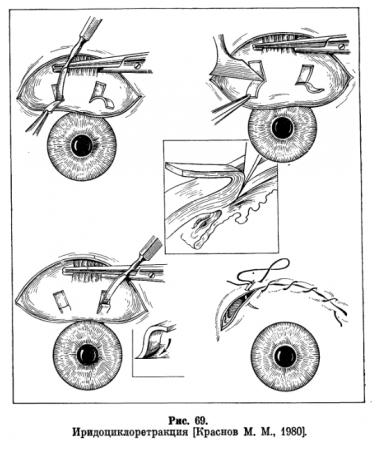
В далеко зашедшей стадии может быть применена трабекулэктомия. Методом выбора при наличии мезодермальной ткани или недостаточной дифференцировке трабекулы может быть проникающая гониодиатермия по Брошевскому, при переднем прикреплении радужки — иридоциклоретракция по Краснову (рис. 69). Операция направлена на открытие угла при узкоугольной глаукоме с органическим передним блоком.
Сущность операции состоит во введении в переднюю камеру одной или двух склеральных полосок, которые выполняют роль распорок, отделяющих корень радужки от внутренней поверхности глазного яблока в поддерживающих угол передней камеры в функционирующем состоянии.
В почти абсолютной и абсолютной стадиях производят проникающую гониодиатёрмию, фильтрующую иридэктомию по Шайе, склерогониоклейзис и др. В поздних стадиях заболевания, особенно у неоднократно оперированных больных в связи с опасноностью проведения полостных операций, могут быть применены хирургические вмешательства, направленные на уменьшение продукции внутриглазной жидкости.
При гидрофтальме производят циклодиатермокоагуляцию или циклокриоаппликацию склеры в области, соответствующей отросткам ресничного тела, в которых под влиянием высокой или низкой температуры происходит рубцевание.
Предпочтительнее использовать диатермокоагуляцию в связи с более глубоким воздействием ее по сравнению с криокоагуляцией. Принципом циклоанемизации является воздействие на сосуды, питающие ресничное тело. С этой целью производят диатермокоагуляцию длинной задней или передней ресничной артерии, в результате чего происходит облитерация сосуда. Добиться этого с помощью криокоагуляции практически невозможно.
Гипотензивный эффект операций, направленных на уменьшение продукции внутриглазной жидкости, при гидрофтальме, как правило, небольшой и часто нестойкий.
Медикаментозное лечение. Медикаментозное лечение врожденных глауком включает применение миотических средств, дегидрационной и отвлекающей терапии.
В связи с наличием при врожденных глаукомах грубых препятствий оттоку внутриглазной жидкости миотические средства, как правило, оказывают небольшое влияние на внутриглазное давление.
Вследствие этого медикаментозную терапию применяют не как самостоятельный метод, а как дополнение к хирургическому лечению. Пилокарпина гидрохлорид снижает офтальмотонус в среднем на 2—4 мм рт. ст., армин и ацеклидин — на 6- -7 мм рт. ст.
Учитывая способность миотических средств несколько снижать офтальмотонус, их следует назначать:
- сразу после установления диагноза в период подготовки больного к стационированию для выполнения операции;
- после операции в тех случаях, когда не достигнута нормализация внутриглазного давления, до решения вопроса о повторном хирургическом лечении.
При врожденных глаукомах применяют холиномиметические (1 - 2% раствор пилокарпина гидрохлорида, 2 -3% раствор ацеклидина) и антихолинэстеразные (0,005—0,01% раствор армина, 0,25—0,5% раствор тосмилена) миотические средства.
Перспективно использование глазных лекарственных пленок с пилокарпина гидрохлоридом.
Введение их в конъюнктивальный мешок 1 раз в сутки по терапевтическому действию выше 4— 5-кратных инсталляций 1—2% раствора пилокарпина.
Применяют симпатикотропные средства, чаще 0,1—1% раствор адреналина гидрохлорида, который суживает сосуды ресничного тела и снижает продукцию водянистой влаги. Используют также адренопилокарпин (0,1 г пилокарпина и 10 мл 0,1% раствора адреналина). Назначают также средства, уменьшающие продукцию внутриглазной жидкости, — ингибиторы карбоангидразы (диакарб внутрь), и препараты осмотического действия — глицерол внутрь.
Дети с врожденными глаукомами нуждаются в общеукрепляющей и десенсибилизирующей терапии, а также в лечении, направленном на улучшении трофики глаза (АТФ, витамины и др.).
Результаты лечения врожденной глаукомы и прогноз. Прогноз врожденных глауком значительно улучшился благодаря раннему выявлению заболевания, своевременному лечению, применению микрохирургических патогенетически обоснованных операций. В последние годы нормализации офтальмо- тонуса достигают более чем у 92 % больных в ранние сроки после операции и у 85% и более — в отдаленные.
После достигнутой в результате хирургического лечения стойкой нормализации внутриглазного давления зрительные функции могут не только сохраняться, но и повышаться. Зрение сохраняется в течение всей жизни у 75% своевременно оперированных детей, и только у 15-20% поздно оперированных.
Диспансерное наблюдение детей с врожденными глаукомами. Дети с врожденными глаукомами должны находиться под диспансерным наблюдением в поликлинике, их необходимо обследовать 1 раз в месяц. У этих детей определяют остроту зрения, исследуют поле зрения, проводят кератометрию, биомикроскопию, офтальмоскопию, тонометрию, эхобиометрию.
Детей до 3 лет, а также беспокойных, неконтактных детей и более старшего возраста, у которых не удается провести необходимые исследования в амбулаторных условиях, следует направлять для обследования в стационар. Это целесообразно делать не реже 1 раза в 3—4 мес.
В процессе диспансерного наблюдения за детьми с врожденными глаукомами после операции проводят медикаментозное лечение, назначают коррекцию аномалии рефракции, при наличии показаний назначают плеоптическое лечение.
Важная задача диспансерного наблюдения - выявление детей с некомпенсированной, прогрессирующей глаукомой, осложнениями и незамедлительное направление их в глазное отделение для детального обследования и хирургического лечения.
Критериями стабилизации глаукоматозного процесса являются нормальное внутриглазное давление, отсутствие светобоязни, блефароспазма, слезотечения, отека роговицы, стабильность зрительных функций, отсутствие патологического растяжения роговицы и увеличения глазного яблока, по данным кератометрии и эхобиометрии, отсутствие отрицательной динамики состояния глазного дна.


Комментариев 0